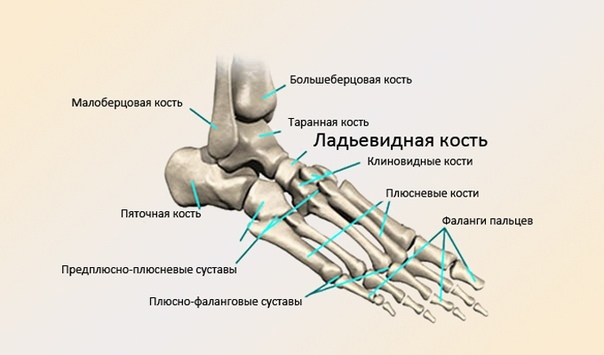
Клинический случай ревматоидный артрит
Статья посвящена ревматоидный артриту — клиническим ситуацииям и алгоритмам лечения

Ревматоидный артрит (РА) – хроническое системное иммуновоспалительное заболевание неизвестной этиологии, сопровождающееся развитием симметричного прогрессирующего эрозивно-деструктивного полиартрита и внесуставными проявлениями [1]. РА ассоциирован с высоким риском кардиоваскулярных событий, остеопоротических переломов, ранней инвалидизацией и преждевременной смертностью пациентов. Улучшить прогноз и исходы болезни способны только своевременная диагностика и раннее активное лечение больных РА.
Течение болезни складывается из нескольких последовательных стадий: ранней, развернутой и поздней, каждая из них имеет свои клинические особенности и подходы к терапии.
Базовые принципы терапии РА («Treat to target» или «Лечение до достижения цели») [2, 3]:
1. Достижение ремиссии (DAS28 (суммарный индекс (включает упрощенный счет из 28 суставов), позволяет многократно оценивать активность РА и может быть использован для контроля его активности в повседневной практике) <2,6) или как минимум низкой активности заболевания (DAS28 <3,2).
2. Ранняя активная терапия базисными противовоспалительными препаратами (БПВП), в первую очередь метотрексатом (МТ), не позднее первых 3 мес. от начала болезни.
3. Лечение должно быть максимально активным, с быстрой эскалацией дозы МТ и последующим изменением (при необходимости) схемы лечения в течение 3 мес. до достижения ремиссии (или низкой активности) болезни.
4. Тщательный контроль изменений активности заболевания и коррекция терапии не реже 1 раза в 3 мес. или ежемесячно у больных с высокой и умеренной активностью РА.
5. В случае недостаточной эффективности стандартной терапии БПВП показано назначение генно-инженерных биологических препаратов (ГИБП).
6. Определение тактики терапии должно быть согласовано с пациентом.
К факторам неблагоприятного прогноза (ФНП) у больных РА относятся [4]:
– молодой возраст;
– женский пол;
– высокие титры ревматоидного фактора (РФ) и/или антитела к циклическому цитруллиновому пептиду (АЦЦП);
– эрозивный процесс в суставах по данным рентгенографического исследования или магнитно-резонансной томографии (МРТ);
– повышение уровней острофазовых показателей: скорости оседания эритроцитов (СОЭ) или С-реактивного белка (СРБ);
– высокая активность заболевания согласно индексам DAS28, SDAI (Simplified Disease Activity Index) или CDAI (Clinical Disease Activity Index);
– внесуставные проявления (синдром Шегрена, поражение легких и т. д.).
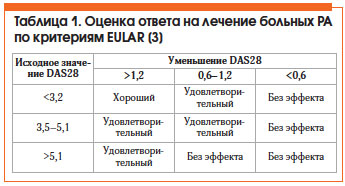
Оценка эффективности лечения РА по критериям Европейской антиревматической лиги (EULAR) представлена в таблице 1. Общепризнанным методом оценки активности РА является расчет индекса DAS28, который можно автоматически произвести на сайте www.das-score.nl.
Критерии эффективности терапии РА [5]:
• хороший клинический ответ (≈ ACR 70) (критерии Американской коллегии ревматологов);
• низкая активность болезни (DAS28 ≤ 3,2) или ремиссия (DAS28 ≤ 2,6);
• улучшение функции (HAQ (Health Assessment Questionare, опросник состояния здоровья, позволяющий оценить функциональные способности больных РА) <1,5) и качества жизни;
• предотвращение прогрессирования деструкции:
– замедление нарастания рентгенологических индексов (Sharp, Larsen);
– отсутствие появления новых эрозий;
– стабилизация или улучшение состояния по данным МРТ.
У пациентов, находящихся в состоянии ремиссии более 1 года после отмены глюкокортикостероидов (ГКС), следует рассмотреть вопрос о возможности прекращения лечения ГИБП, особенно если они применялись в комбинации с БПВП. Важное значение при определении тактики лечения имеет выбор пациентов.
Рассмотрим отдельные клинические ситуации и подходы к терапии при РА.
I. Пациент с впервые установленным ранним РА
Ранняя стадия РА – условно выделенная, клинико-патогенетическая стадия заболевания с длительностью активного синовита до 1 года, характеризуется преобладанием экссудативных изменений в пораженных суставах, частым атипичным течением и хорошим ответом на лечение. Выделение понятия «ранний РА» связано со сложившимися представлениями о патогенезе болезни и необходимости проведения ранней активной терапии РА. Ранний РА может дебютировать как недифференцированный артрит, что требует динамического наблюдения за больными и проведения тщательного дифференциально-диагностического поиска. На ранней стадии РА наиболее информативными являются диагностические критерии Американского и Европейского ревматологических сообществ, предложенные в 2010 г. (табл. 2).

Диагноз РА может быть установлен при общем счете не менее 6 баллов.
Доказано, что адекватная базисная терапия на ранней стадии РА позволяет предотвратить структурные повреждения, что способствует сохранению функциональной активности пациентов и улучшает отдаленный прогноз. БПВП необходимо назначать не позднее 3 мес. от начала РА с быстрой эскалацией дозы для достижения оптимального эффекта (DAS <2,4) и последующей заменой препарата в течение 3–6 мес. при его неэффективности [1]. Терапию БПВП следует продолжать даже при снижении активности заболевания и достижении ремиссии.
К БПВП первого ряда отнесены МТ, лефлуномид (ЛФ) и сульфасалазин (СС) (табл. 3), т. к. доказана их эффективность в отношении предотвращения деструктивных изменений суставов (уровень доказательности А). Препараты «второй линии» (гидроксихлорохин, препараты золота и др.) применяются при неэффективности препаратов первого ряда либо в комбинации с ними.
МТ – «золотой стандарт» терапии активного РА. При необходимости назначения МТ в дозе > 15 мг/нед. рекомендуется использовать парентеральный путь введения (в/м или п/к). Также с целью минимизации побочных явлений необходимо назначение фолиевой кислоты 1 мг/cут (5 мг/нед.), исключая дни приема МТ.

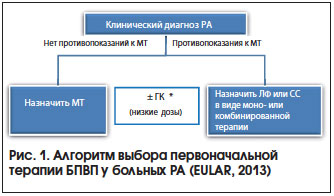
Основные стратегии лечения раннего РА (рис. 1) [7]:
1. Монотерапия МТ c последующей заменой на другие БПВП (ЛФ, СС) через 3–6 мес. в случае неэффективности или плохой переносимости).
2. Комбинированная базисная терапия, в т. ч. в сочетании с высокой дозой ГК. Используются комбинации БПВП как первого ряда (МТ + СС или МТ + ЛФ), так и второго ряда (МТ + Плаквенил) и т. д.
3. Комбинированная терапия синтетическими БПВП + ГИБП (в первую очередь ингибиторы фактора некроза опухоли (ФНО) при сохраняющейся > 3–6 мес. высокой активности РА, а также при наличии ФНП. Например, МТ 25 мг/нед. + Инфликсимаб 3 мг/кг массы тела.
II. Пациент с развернутым РА, не отвечающий на традиционные БПВП
Развернутая стадия РА – заболевание с отчетливо выраженной симптоматикой и длительностью болезни более 1 года. Суставной синдром имеет стойкий, симметричный и полиартикулярный характер с преимущественным поражением суставов кистей и стоп, выявляются признаки высокой или умеренной лабораторной активности, серопозитивность по РФ, эрозивный процесс в суставах по данным рентгенографии. Если диагноз устанавливается впервые, то стратегия ведения больного та же, что и при раннем РА. В случае уже проводившегося лечения с недостаточным эффектом или непереносимостью синтетических БПВП (как в виде монотерапии, так и при комбинированном их использовании), а также наличием ФНП прибегают к назначению ГИБП (рис. 2). Использование ГИБП позволяет максимально избирательно воздействовать на отдельные звенья иммунопатогенеза РА и существенно улучшить состояние больных РА, резистентных к стандартным БПВП и ГК [8]. Установлено, что комбинация традиционных БПВП с ГИБП более эффективна, чем монотерапия.
Назначение ГИБП показано:
– при длительно сохраняющейся (> 3–6 мес.) высокой активности РА;
– при высокой активности заболевания < 3 мес., только при наличии у больных ФНП.
Препаратами первого ряда среди ГИБП являются ингибиторы ФНО-α. Другие ГИБП назначаются больным РА с неадекватным ответом на блокаторы ФНО-α или при невозможности их применения (табл. 4).

Противопоказания к назначению ГИБП: отсутствие лечения одним или более БПВП (в первую очередь МТ) в полной терапевтической дозе; купирование обострений; тяжелые инфекционные заболевания (сепсис, септический артрит, пиелонефрит, остеомиелит, туберкулезная и грибковая инфекции, вирус иммунодефицита человека), злокачественные новообразования; беременность и лактация.
III. Пациент с поздним РА и остеопоротическими переломами
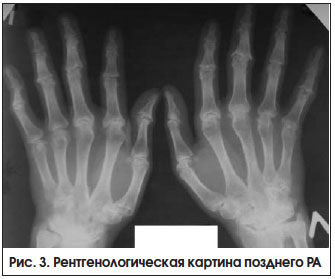
Поздняя стадия РА определяется как стадия необратимых структурных изменений (деформаций, подвывихов) суставов при длительности болезни > 2-х лет, с выраженными признаками активного воспаления или без них (рис. 3). Неуклонное прогрессирование болезни приводит к формированию различных видов подвывихов и контрактур суставов, в связи с чем возрастает роль реабилитационных и ортопедических мероприятий.
Развитие остеопороза (ОП) и ассоциированных с ним переломов является одним из наиболее тяжелых осложнений РА, определяющим неблагоприятное течение и прогноз болезни. Частота остеопоротических переломов среди больных РА в 1,5–2,5 раза выше, чем в общей популяции [9]. Предполагается, что развитие ОП и суставной деструкции при РА имеет единые патогенетические механизмы, в основе которых лежит цитокин-зависимая активация остеокластогенеза, приводящая к повышению костной резорбции [10]. Развитие ОП при РА определяется множеством общих и специфических, ассоциированных с заболеванием и лечением, факторов риска.
РА-ассоциированные факторы риска ОП и переломов [11]:
– активность воспалительного процесса,
– рентгенологическая стадия,
– тяжесть функциональных нарушений (HAQ > 1,25),
– длительность болезни,
– прием ГК,
– высокий риск падений.
У больных РА прием ГК в 4–5 раз повышает риск вертебральных переломов и удваивает риск переломов бедра. При этом доказано, что не существует безопасной дозы ГК. Также следует помнить, что развитие переломов у больных, получающих ГК, происходит при более высоких значениях минеральной плотности ткани (МПК), чем при первичном ОП, поэтому антиостеопоротическую терапию следует начинать при значениях Т-критерия < -1,5 стандартного отклонения от референсных значений.
Программа ведения больных РА и с остеопоротическими переломами включает контроль активности РА, коррекцию модифицируемых факторов риска ОП и переломов, предупреждение падений, антиостеопоротическую терапию, диету и физические упражнения. Всем больным РА необходимы проведение расчета абсолютного риска переломов (FRAX-алгоритм) (fracture risk assessment tool, 10-летний абсолютный риск перелома – инструмент оценки риска перелома ВОЗ) и профилактическое назначение препаратов кальция и витамина D. Назначение антиостеопоротической терапии без учета данных МПК проводится у пациентов в возрасте 65 лет и старше при наличии в анамнезе переломов при минимальной травме. Препаратами первой линии в лечении ОП у больных РА являются бисфосфонаты (БФ) и антитела к RANKL (лиганду рецептора активатора ядерного фактора каппа бета), обладающие антирезорбтивным действием (табл. 5). Привлекательность БФ при РА заключается еще и в том, что, по данным экспериментальных исследований, они могут оказывать благоприятное влияние на течение болезни. Установлено, что БФ способны ингибировать cинтез провоспалительных цитокинов и развитие костных эрозий при РА [12]. У пациентов с ранним артритом БФ в комбинации с МТ эффективно предотвращают развитие костной деструкции [13].

IV. Пожилой пациент с РА и НПВП-гастропатией
РА у лиц пожилого возраста характеризуется активным быстропрогрессирующим течением, высоким уровнем коморбидности и неблагоприятными исходами. Особое значение в структуре коморбидных состояний при РА имеют кардиоваскулярная и гастроинтестинальная патологии. По данным многочисленных исследований, сердечно-сосудистая заболеваемость и смертность у больных РА в 2–4 раза выше, чем в общей популяции, что диктует необходимость своевременного выявления и коррекции факторов кардиоваскулярного риска.
Рекомендации по снижению кардиоваскулярного риска у больных РА [14]:
• АСК следует принимать за ≥2 ч до приема нестероидных противовоcпалительных препаратов (НПВП).
• Не использовать НПВП в течение 3–6 мес. после острого сердечно-сосудистого события или процедуры.
• Регулярно контролировать артериальное давление.
• Использовать НПВП в низких дозах с коротким периодом полураспада (избегать назначения НПВП с пролонгированным высвобождением).
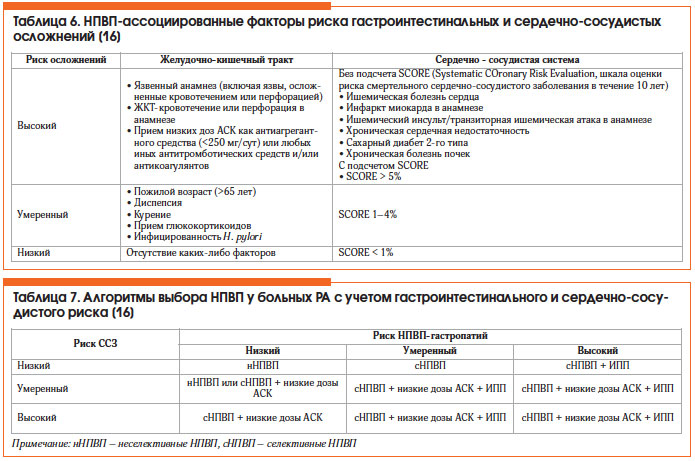
НПВП-гастропатия – одно из наиболее частых осложнений длительного приема НПВП, проявляющееся в виде эрозивного или язвенного поражения верхних отделов желудочно-кишечного тракта (ЖКТ) (преимущественно антральный и препилорический отделы желудка). Прием НПВП не влияет на прогрессирование РА, однако позволяет лучше контролировать симптомы заболевания на фоне терапии БПВП и ГИБП. НПВП-ассоциированные факторы риска гастроинтестинальных и сердечно-сосудистых осложнений представлены в таблице 6.
Экспертами EULAR разработан «калькулятор» для индивидуального подбора НПВП в зависимости от наличия факторов риска в отношении ЖКТ и сердечно-сосудистой системы [15]. К НПВП с наименьшим кардиоваскулярным риском отнесены напроксен, целекоксиб, кетопрофен, низкие дозы ибупрофена (<1200 мг/сут). Основные лекарственные средства, которые используют для лечения НПВП-индуцированных гастропатий, — ингибиторы протонной помпы (ИПП), Н2-блокаторы и мизопростол (синтетический аналог ПГ Е2). Алгоритмы выбора НПВП у больных РА с учетом гастроинтестинального и сердечно-сосудистого риска представлены в таблице 7 [16].
Не так давно появилась новая генерация НПВП, которые повышают активность оксида азота (NO) в слизистой желудка (NO-НПВП). Как известно, NO обладает гастропротективными свойствами: стимулирует секрецию слизи, бикарбоната, улучшает микроциркуляцию, ингибирует адгезию лейкоцитов к эндотелию, что и определяет фармакологические преимущества данной группы НПВП. Одним из представителей NO-НПВП является препарат Найзилат (амтолметин гуацил), который наряду с высокой анальгетической и противовоспалительной активностью обладает гастропротективными свойствами. В рандомизированных клинических исследованиях были продемонстрированы более низкие частота и тяжесть повреждений слизистой оболочки желудка после применения амтолметин гуацила по сравнению с таковыми других неселективных НПВП (диклофенак, индометацин, пироксикам), при сопоставимой противовоспалительной и анальгетической их эффективности [17]. Сравнительное исследование амтолметин гуацила 1200 мг/сут и целекоксиба 400 мг/сут у больных РА показало равнозначные эффективность и безопасность препаратов [18]. Терапевтическая доза амтолметин гуацила (Найзилат) составляет 600 мг 2 р./сут натощак, поддерживающая – 600 мг/сут.
Заключение
РА является гетерогенным заболеванием, исходы которого во многом определяются своевременной диагностикой болезни и правильно выбранной тактикой лечения. Ранняя стадия РА, особенно первые 3 мес. от начала заболевания, наиболее благоприятны для проведения эффективной базисной терапии. Основой ведения больных РА является тщательное мониторирование активности заболевания (не реже 1 р./3 мес.) с последующей коррекцией терапии при необходимости. Выбор терапии определяется стадией РА, активностью болезни, наличием ФНП, сосуществующими коморбидными состояниями, а также эффективностью предшествующего лечения.
Источник
1. АО «Медицинский университет Астана» Кафедра семейной и доказательной медицины Тема СРИ: Распространенные заболевания в терапии
Клинический случай
пациента Ахметова М.У
Клинический диагноз: Ревматоидный артрит, РФ(+), суставная форма. Активность III.
Рентгенологическая стадия III. НФС II.
• Основное заболевание:
• Осложнение: Вторичный остеопороз, нормаохромная анемия, гормонозависимость.
• Сопутствующие заболевания:
Подготовил врач-интерн:Сметуллаева Г.А
Группа 645
Преподаватель: Байтенова Л.Н
2. Информация о пациенте:
• ФИО пациента: Ахметова М.У
• Дата рождения: 01.08.1945ж (63л)
• Дом. адрес: Сейфуллин 9, кв51.
• Номер участка:
• Место работы: пенсионер
• Рост: 167
• Вес: 64
• t⁰ тела: 36,7
3. Жалобы при обращении в учреждение ПМСП:
• Боль, усиливающуюся утром, ограничение подвижности в мелких
суставах кистей, (межфаланговых, пястнофаланговых,
лучезапястных, плюснефаланговых), периодически в плечевых.
• утренняя скованность в суставах до 2часа
• выраженную общую слабость, вялость, быстрая утомляемость,
общее недомогание, потеря в весе, повышение температуры;
4. Проведите детализацию жалоб (сформулируйте вопросы) и напишите на них ответы данного пациента
№
п/п
Вопрос
1
Боли в суставах когда вас беспокоит? (утром, вечером
после работы, или не связаны с физ.нагрузком )
Болит в покое, особенно утром. Боли не связаны с
физ.нагрузком. сильные постоянные боли.
2
У вас ограничение движении бывает? Когда? На
сколько продлиться?
По утрам до 2 часов не могу встать с постели.
3
Есть у вас сопутствующие заболевании?
нет
4
Вредные привычки (курите? Алкоголь употребляете?)
нет
5
Как часто болеете ангиной?
В год 3-4 раза
6
7
Ответ
5. Данные объективного осмотра:
• Общее состояние: На момент курации состояние больной по заболеванию средней степени тяжести,
сознание ясное, положение вынужденное из-за ограничения движения в суставах, выражение лица
спокойное
• Кожные покровы и видимые слизистые: Кожные покровы бледные, влажные, на стопах и голенях
трофические нарушения. Ногти искривлены, слоятся, немного утолщены, жёлтого цвета; видимые
слизистые бледные. Подкожная клетчатка умеренно развита, неравномерна больше в области верхнего
плечевого пояса, отёки на ногах и руках.
• Периферические лимфоузлы: Лимфатические узлы не увеличены.
• Состояние мышц: Отмечается выраженная атрофия мышц рук и ног, больше вблизи поражённых суставов;
сила мышц снижена.
• Состояние костной системы: пальцы кисти отклонены в ульнарную сторону вследствие подвывихов в
пястно-фаланговых суставах с переразгибанием в проксимальном межфаланговом и сгибании в дистальном
межфаланговых. Суставы кисти немного гиперимированы, отёчны; при пальпации суставы болезненны,
температура повышена, отёчность периартикулярной ткани, положительный симптом бокового сжатия.
Движение в кисти болезненно и ограничено. Амплитуда пронации и супинации в правой руке полностью
сохранена, а в левой руке пронация 60 , супинация 60, с трудом производит неполное сжатие в кулак левой
и правой кисти. Мышечная сила – 3 балла. Суставы стопы: Деформация суставов, подвывихи в
плюснофаланговых суставах, 1 палец отклонён на правой и левой ноге латерально, а 2 и 3 в медиальную
сторону. На 1 пальце правой ноги ревматоидный узел – размер 1 см; кожа над суставами трофически
изменена, вены извитые, расширенные, пальпация суставов болезненна, выраженная отёчность
периартикулярной ткани, температура кожи повышена. Сгибание и разгибание в суставах отсутствуют.
• Органы дыхания: Дыхание свободное, тип дыхания смешанный, ЧД 18 , грудная клетка нормостенического
типа. Эластичность межрёберных промежутков снижена, резистентность снижена, при пальпации выявлена
болезненность рёбер и грудины. Голосовое дрожание равномерно снижено с обеих сторон в верхней части
грудной клетки. При сравнительной перкуссии отмечается укорочение звука над всей поверхностью лёгких
и притупление звука слева по задней поверхности. Аускультация: дыхание везикулярное, хрипов нет.
6. Данные объективного осмотра:
• Сердечно-сосудистая система: При пальпации верхушечный толчок определяется слева в 5 – ом межреберье
на 1 см кнаружи от серединоключичной линии, сила верхушечного толчка повышена, S=2,5см – 3см,
разлитой.
ЧСС = 78`, ритм правильный, пульс полный, малый. При перкуссии границы сосудистого пучка
соответствуют правому и левому краю грудины, ширина сосудистого пучка 5 см.
Границы относительной тупости: правая – 4 межреберье по краю грудины справа. Левая – соответствует
верхушечному толчку, верхняя граница – 3 межреберье по парастернальной линии.
Аускультация: тоны сердца ритмичные, приглушенные, шумов нет.
АД на правой руке – 120/90 мм.рт.ст
АД на левой руке – 110/85 мм.рт.ст
• Система пищеварения: Слизистая рта бледно-розового цвета, сосочки сглажены на языке, лаковый язык,
зубные протезы. Живот правильной формы, симметричен, мягкий при пальпации, отмечается
болезненность в эпигастральной области, симптом Щёткина-Блюмберга отрицательный. При глубокой
пальпации сигмовидная кишка расположена сверху вниз слева направо снаружи кнутри, толщиной 1 см,
гладкая, безболезненная, толщиной 2 см, урчит. Остальные отделы толстого кишечника – подвздошную
кишку, желудок пропальпировать не удалось из-за болезненности в эпигастральной области и выраженного
подкожно-жирового слоя. Печень не увеличена, край печени гладкий, ровный, мягкий, безболезненный.
Селезёнка не пальпируется.
• Система мочеотделения: Кожные покровы поясничной области не изменены, отёчности нет. Почки не
пальпируются, симптом Пастернацкого отрицательный. Пальпация мочеточковых точек безболезненна.
Мочеиспускание безболезненно.
7. Подведите итоги опроса и осмотра пациента (резюмируйте данные):
На основе жалоб и осмотра пациента можно выделить следующие синдромы:
• Суставной синдром ( Боль, усиливающуюся утром, ограничение подвижности в мелких суставах
кистей, (межфаланговых, пястнофаланговых, лучезапястных, плюснефаланговых), периодически
в плечевых. утренняя скованность в суставах до 2часа)
• Конституциональный синдром (выраженную общую слабость, вялость, ревматоидные узелки в
локтевых суставах)
• Анемический синдром (Кожные покровы бледные, ногти искривлены, слоятся, видимые слизистые
бледные)
Можно предположить диагноз: Ревматоидный полиартрит. Суставная форма с внесуставными
признаками. Стадия обострение. НФС3
8. С какими заболеваниями необходимо провести дифференциальную диагностику по основному синдрому, перечислите (минимум 3
заболевания):
1. Болезнь Бехтерева. Суставной синдром в отличие от ревматоидного артрита поражаются суставы
позвоночника. Характерны боли в пояснично-крестцовой области, поражение крупных суставов
вблизи позвоночника, окостенение боковых связок позвоночника – бамбуковая палка, на ранних
этапах слаженность всех отделов позвоночника.
2. Подагрический артрит. Суставной синдром в отличие от РА появление сильных болей в
суставах, покраснение кожи, отёк сустава. Поражается первый плюсневый сустав стопы, но могут
поражаться и другие суставы. Первый приступ заканчивается через 5-8 дней, может развиться
стойкая деформация, на рентгенограмме сужение суставной щели, краевые остеофиты и округлые
дефекты костной ткани в эпифизах, повышение мочевой кислоты; при осмотре – узелки тофусы в
ушных раковинах и околосуставных тканях.
3. Системная красная волчанка. Суставной синдром в отличие от РА в процесс вовлекаются
мелкие суставы, лучезапястный, голеностопный, характерны мигрирующие боли, образование
сгибательных контрактур, поражение кожи – волчаночная бабочка, много волчаночных клеток в
крови, поливисцелиты которые предшествуют поражению суставов, на рентгенограмме
воспалительные процессы только в периартикулярной ткани.
9. Какие лабораторные исследования проведены данному пациенту, их результаты и интерпретация
№
п/п
Анализ
Результат
Интерпретация
Эти данные свидетельствуют об анемии. Анемия
нормоцитарная, гипорегенераторная, нормохромная, в
результате нарушения эритропоэза из-за снижения синтеза
гемоглобина.
1
ОАК:
эритроциты 3,6;
Hb = 95 г/л;
Ретикулоциты- 2%
ЦП-0,88
Тромбоциты- 180/10*9/л
лейкоциты 9,3;
сегменты 54;
лимфоциты 23;
моноциты 7;
СОЭ – 49 мм/ч,
незначительное снижение количества
эритроцитов. снижения количества гемоглобина,
повышение СОЭ, лейкоцитоз
2
ОАМ:
плотность – 1016, среда кислая,
белок 0,33 г/л, сахара нет,
лейкоциты 0-1 п/з, клетки
эпителия единичные в п/з.
Без изменении
3
БХ:
глюкоза в крови 5 ммоль/л.
Дерматоловая проба «+»,
СРБ «++»,
Дерматоловая проба положительная, повышение
СРБ
Признаки активного воспалительного процесса
10. Какие инструментальные исследования проведены данному пациенту, их результаты и интерпретация
№
п/п
Исследование
Результат
1
ЭКГ
Синусовый ритм, ЧСС 85 уд в/мин. Отклонение
ЭОС влево. Высокий зубец R в отведениях V2- V3
3
Рентгенография ОГК
Без изменении.
4
Рентгенография кистей
определяется остеопороз, сужение суставной щели
ДМФС. Кисты основания и головок пястных
костей, дистальных, средниз, проксимальных
фаланг I-V пальцев с обеих сторон. Узура головки
III пястной кости справа. Сужение межзапястных
суставов с признаками анкилозирования. Резкое
сужение СЗС. Субкапсулярный склероз суставных
поверхностей МФС, ПФС.
5
УЗИ внутренних органов
без изменений
Интерпретация
признаки гипертрофии левого
желудочка.
Деструктивные изменения выраженные,
определяются во многих суставах
кистей. Преобладают в типичных для
РА суставах. умеренные и выраженные
деформации эпифизов костей,
подвывихи и вывихи в отдельных или
многих суставах.
Rtg картина РА III ст
11. Какие лабораторные и инструментальные исследования Вы бы назначили дополнительно для дифференциальной диагностики и постановки
заключительного клинического диагноза и почему?
№
п/п
Исследование
Обоснование
1
Исследование синовиальной Данная процедура проводится для диагностики различных воспалительных заболеваний суставов и
жидкости
дистрофических процессов. Она отражает процессы, происходящие в хрящевой ткани и
синовиальной оболочке, быстро реагирует при наличии воспаления в суставе. Синовиальная
жидкость является важным компонентом сустава и, в значительной степени, определяет его
морфофункциональное состояние. Важное диагностическое значение имеет подсчет числа клеток в
препарате (в норме до 200 клеток/мкл). Увеличение количества клеток (цитоз) позволяет
дифференцировать воспалительные и дистрофические заболевания и оценивать динамику
воспалительного процесса.
2
Исследование
антинуклеарных антител
Определение антител к нуклеарным антигенам в сыворотке — тест на системные
заболевания соединительной ткани. Основная цель исследования — исключить СКВ,
поскольку при этом заболевании АНА выявляются у 95% больных в течение 3 месяцев
после его начала.
3
МРТ кистей
выявить артрит или асептический невроз на ранней стадии. если есть подозрение на
контузии костей и мышц, а также на растяжения сухожилий. Полученные снимки
позволяют увидеть структуру хрящей и расположенных под ними костей, а также связок,
дисков, суставных капсул и сумок, менисков и внутрисуставных сосудов.
12. Проведите дифференциальный диагноз, последовательно исключая все заболевания, кроме одного:
1) Учитывая, что у пациента нет поражение суставы позвоночника, характерные боли в пояснично-крестцовой
области, поражение крупных суставов вблизи позвоночника, симптом сакроилеита, симптом спелого арбуза,
поражение грудино-ключичных и акромиально-ключичных сочленений, ирит. Нет специфические антигены HLB
B27, то диагноз болезнь Бехтерева исключается.
2) Учитывая, что у пациента нет поражение кожи – волчаночная бабочка, нет много волчаночных клеток в крови,
поливисцелиты которые предшествуют поражению суставов. РФ незначительно повышено,то диагноз СКВ
исключается.
3) Учитывая, что пациент женского пола, течение заболевания хроническая, ревматоидные узелки в локтевых
суставах, утренняя скованность (2ч) в крови ЦИК повышенный, АЦЦП+, РФ+ диагноз Подагрический артрит
исключается
4) Наиболее вероятным остается диагноз Ревматоидный артрит.
13. Сформулируйте заключительный диагноз согласно классификации и обоснуйте основное заболевание с осложнениями (см.пример в
таблице)
• Клинический диагноз: Ревматоидный артрит, РФ(+), суставная форма. Активность III. Рентгенологическая стадия III.
НФС II.
• Основное заболевание: Ревматоидный артрит, НФС II
• Осложнение: Вторичный остеопороз, нормаохромная анемия, гормонозависимость.
• Сопутствующие заболевания:
Пункт диагноза для
обоснования
Анамнез
Клиника
Лабор. данные
Инструм. данные
Ревматоидный артрит
Хронический
аутоиммунный
воспалительный
процесс
Суставной синдром
Конститутцинальный синдром
ОАК: Лейкоцитоз,
повышение СОЭ,
БХ: дерматоловая проба+,
СРБ +++
Иммунологические
исследование: РФ+, АЦЦП
+, ЦИК97
признаки предыдущей
стадии, множественные
эрозии, подвывихи в
суставах; Rtg картина РА III
ст
РФ(+), Серопозитивный
Иммунологические
исследования крови:
Положительная реакция РФ
Суставная форма
Поражение суставов
Активность III
сильные боли в покое, выражены
экссудативные явления, кожа над
суставами гиперемирована, местная
температура повышена;
скованность продолжается до
второй половины дня, глубокое
ограничение подвижности
Признаки активного
воспалительного процесса
14. Сформулируйте заключительный диагноз согласно классификации и обоснуйте основное заболевание с осложнениями (см.пример в
таблице)
Пункт диагноза для
обоснования
Анамнез
НФС II
Клиника
Лабор. данные
сохранены возможности
самообслуживания,
ограничены возможности
занятием
непрофессиональной и
профессиональной
деятельностью
Вторичный остеопороз
В рентгенограмме
определяется остеопороз
нормахромная анемия
гормонозависимость
Инструм. данные
Кожные покровы бледные,
ногти искривлены, слоятся,
видимые слизистые бледные
У пациента после
прекращение приема
ГКС появились
обострение заболевания
и суставной синдром
ОАК: Анемия,
незначительнаяэритроци
топния, нормохромия.
15. Опишите принципы лечения данного пациента:
№
п/п
Принцип лечения
Описание
1
Воздействие на факторы
риска
Избегать факторов, которые потенциально могут провоцировать обострение
болезни (интеркуррентные инфекции, стресс и др.); Поддержание идеальной
массы тела, Сбалансированная диета (рыбий жир, оливковое масло и др.), фрукты,
овощи.
2
Этиотропное лечение
следовательно необходимо выявить все хронические очаги и их устранение.
(лечить кариозные зубы и т.д)
3
Патогенетическое лечение
Препараты необходимо назначать на длительный срок до нескольких месяцев.
Базисными препаратами являются цитостатики и ГКС. Основной механизм
(цитостатик) выраженное иммуносупрессивное действие. ГКС оказывает
противовоспалительное, иммунодепрессивное действие.
Метотрексат 17,5мг 1 р в неделью
Метилпред 4 мг 2 таб в/д
16. План диспансеризации данного больного (приказ №885):
№
п/п
Мероприятие
Выполнение
1
Наименование и частота
лабораторных и диагностических
исследований
Общий анализ крови + число тромбоцитов, общий анализ мочи 2-4 раза в
год (при применении цитостатиков — ежемесячно). Определение РФ.
Рентгенография костей таза, позвоночника и грудной клетки 1 раз в год.
ЭКГ 1 раз в год
2
Медицинские осмотры СМР
Назначение и контроль за соблюдением частоты лабораторных и других
(среднего медицинского работника) диагностических исследовании. Действие по маршруту пациента, при
появлении признаков прогрессирования и изменения лабораторных
показателей направление к ВОП
3
Частота осмотра СМР
2-4 раза в год
4
Медицинские осмотры ВОП
Контроль за состоянием пациента. Действие по маршруту пациента, при
появлении факторов риска коррекция терапии. При появлении признаков
прогрессирования решение вопроса госпитализации. При отсутствии
эффективности и лечения в течение 1 мес. направление к ревматологу
5
Частота осмотра ВОП
4-6 раз в год
6
Консультация профильных
специалистов
Ревматолог — 4-6 раз в год. стоматолог, ЛОР, офтальмолог 1-9 раза в год (по
возможности)
Источник