Разминка при артрозе плечевого сустава
Острые респираторные вирусные инфекции (ОРВИ) в настоящее время являются, пожалуй, самыми распространенными и социально значимыми заболеваниями. Считается, что едва ли не каждый человек ежегодно переносит ОРВИ. Столь высокая заболеваемость ассоциируется со значительными экономическими потерями, прежде всего за счет большого числа нетрудоспособных пациентов. Другой проблемой является тот факт, что практически любой человек считает себя знатоком лечения ОРВИ, что в конечном итоге приводит к огромному числу ошибок и нежелательных явлений, сопровождающих терапию. До настоящего времени не существует каких-либо четких рекомендаций, касающихся фармакотерапии ОРВИ, и для лечения данного заболевания используются, как минимум, сотни препаратов из различных фармакологических групп. В связи с этим целью данной публикации явилась критическая оценка ряда лекарственных средств, применяемых для лечения ОРВИ с позиций доказательной медицины.
Заболевание вызывают различные респираторные вирусы, в первую очередь, это риновирусы, обуславливающие до 30–50% случаев во всех возрастных группах. Вирусы гриппа вызывают 5–15% случаев респираторных инфекций, коронаровирусы «забирают» до 15%, респираторно-синцитиальный вирус (РСВ), вирусы парагриппа, аденовирусы и энтеровирусы встречаются значительно реже (<5%). У 5% пациентов выявляется более двух респираторных вирусов, а в 20–30% случаев идентифицировать возбудителя не удается.
До настоящего времени клиническая практика располагает всего лишь двумя группами препаратов, активных в отношении гриппозной инфекции (блокаторы М2-каналов, ингибиторы нейроминидазы) и одним средством против РСВ. Препараты, активные в отношении риновирусов и коронаровирусов, находятся в стадии разработки или на этапе клинических исследований (плеконарил).
Из блокаторов М2-каналов наибольшее распространение получил римантадин, активный в отношении вируса гриппа А. Препарат позволяет предотвратить до 70% случаев гриппозной инфекции и до 25% случаев гриппоподобных заболеваний. С лечебной целью римантадин назначается не позднее 48 часов от появления первых симптомов заболевания у пациентов старше 14 лет по 100 мг по 2 раза в сутки; у лиц старше 65 лет по 100 мг в сутки. Рекомендуемая длительность терапии составляет 3–5 дней. Прием римантадина в ряде случаев сопровождается нежелательными явлениями: тошнота, снижение аппетита, раздражительность, нарушение концентрации внимания, бессонница.
Обеспокоенность вызывает развитие высокой резистентности к Римантадину, достигающей в некоторых странах (США, Канада) 90%. Однако в России по данным 2005 года резистентность к Римантадину составляла порядка 18%. В этой связи можно предполагать, что резистентность к блокаторам М2-каналов в нашей стране не достигает катастрофических значений, что связано в первую очередь с низким уровнем потребления противовирусных препаратов для лечения и профилактики ОРВИ. Напомним читателю, что в настоящее время наиболее часто используемым средством для лечения вирусных инфекций в России является Арбидол (индуктор эндогенного интерферона), «перспективы» использования которого будут рассмотрены нами ниже.
Новые противовирусные препараты— ингибиторы нейроминидазы (осельтамивир и занамивир) активны не только в отношении вируса гриппаА, но и B. Наибольшее распространение получил осельтамивир, доступный для перорального применения в форме капсул, обладающий высокой безопасностью терапии, что позволяет использовать его у детей с 1 года. Осельтамивир в терапевтических дозах (150 мг и 75 мг в сутки) способен сокращать частоту осложнений гриппа, продолжительность клинических симптомов и тяжесть течения заболевания. По некоторым данным, его применение сопровождается снижением частоты летальных исходов у пациентов с постгриппозной пневмонией. Профилактический прием осельтамивира в дозах 75 мг/сутки и 150 мг/сутки позволяет предотвратить до 61% и 73% случаев гриппа соответственно (действия на заболеваемость гриппоподобными инфекциями не зарегистрировано). Осельтамивир является одним из наиболее безопасных противовирусных препаратов, достаточно редко его прием сопровождает тошнота, рвота, редко головные боли, головокружение, слабость и бессонница, не требующие отмены терапии. Для лечения гриппа у пациентов старше 13 лет осельтамивир назначается по 75 мг два раза в сутки, у детей от 1 года до 12 лет доза зависит от массы тела (≤15 кг— 30 мг 2 раза в сутки; 16–23 кг— 45 мг 2 раза в сутки; 24–40 кг— 30 мг 2 раза в сутки; ≥40 кг— 75 мг 2 раза в сутки). Рекомендуемая продолжительность терапии составляет 5 дней. У пациентов с клиренсом креатинина менее 30 мл/мин доза снижается в два раза.
Другой представитель группы ингибиторов нейроминидазы— занамивир, обладает низкой биодоступностью, вследствие чего используется только в ингаляционной форме. Препарат позволяет сократить продолжительность симптомов заболевания и частоту осложнений гриппа; при профилактическом использовании занамивир способен предупредить развитие гриппа в 62% случаев. К числу нежелательных явлений, сопровождающих его прием, относят першение в горле, редко бронхоспазм, головные боли, головокружение. Занамивир рекомендуется для лечения гриппа у лиц старше 7 лет при сроке появления клинических симптомов не более 36 часов в дозе 10 мг 2 раза в сутки в течение 5 дней.
К сожалению, применение препаратов данной группы также характеризуется развитием высокой резистентности к ним вирусов гриппа. Если ранее (2001) частота резистентных штаммов вируса гриппа А к осельтамивиру не превышала 0,32% у взрослых и 4,1% у детей, то в сезонах 2007–2008 гг. эксперты подразделения ВОЗ (WHO Collaborating Center for Reference and Research on Influenza at CDC) предупреждают о развившейся резистентности к осельтамивиру и занамивиру до 64% в различных странах мира. Другой проблемой является экономический фактор— например, стоимость осельтавимивира составляет 1400–1600 рублей, в то время как терапия римантадином (30–70 рублей) признается наиболее рентабельной.
Рибавирин, активный в отношении РСВ-инфекции (тяжелая пневмония и бронхиолит у новорожденных и детей раннего возраста), применяется только в режиме небулайзерной терапии и только в случае положительного результата серологической диагностики, подтверждающей наличие РСВ. Рибавирин— высокотоксичный препарат, при его использовании отмечаются бронхоспазм, сыпь, раздражение глаз, причем не только у пациентов, но и у медперсонала; бессонница, раздражительность; возможно развитие лейкопении.
Упомянутый нами ранее плеконарил, активный против основного возбудителя ОРВИ— риновирусов, в настоящее время прошел этап клинических исследований, доказавший его эффективность (снижение длительности заболевания на 1 сутки), однако комитет по антивирусным препаратам Управления по контролю за пищевыми продуктами и лекарственными препаратами США (FDA) по ряду причин (нежелательные явления, высокая резистентность к препарату) отклонил санкцию на его применение в клинической практике.
Использование антибиотиков для лечения вирусной инфекции является грубой ошибкой, к сожалению, часто встречающейся в реальной практике. Единственным показанием к применению антибактериальной терапии является развитие бактериальных осложнений вирусной инфекции (острый средний отит, острый синусит, постгриппозная пневмония и пр.) и то только в четко определенных клинических ситуациях.
В настоящее время существуют данные плацебо-контролируемых исследований, доказавших эффективность интраназального применения интерферона для профилактики ОРВИ. При этом доказательств какой-либо действенности препарата для лечения респираторных инфекций не получено. Основным недостатком интраназальных интерферонов являются нежелательные реакции, в числе которых появление кровянистых выделений из носа, гриппоподобные симптомы, сонливость, аллергические реакции. Существует ряд лекарственных форм экзогенного интерферона в свечах, однако эффективность его не доказана в рамках контролируемых клинических испытаний.
Перспективным направлением профилактики ОРВИ является использование средств для активизации неспецифической резистентности организма. С этой целью в российской клинической практике широко используются индукторы эндогенных интерферонов— Тилорон, Арбидол, Циклоферон. К сожалению, их клиническое значение в лечении и профилактике респираторных вирусных инфекций до настоящего времени не определено ввиду непостоянства эффекта в плацебо-контролируемых исследованиях. По-видимому, их применение наиболее актуально у невакцинированных лиц в предэпидемический период, как дополнение к химиопрофилактике Римантадином, ингибиторами нейроминидазы (либо при их непереносимости) у пациентов с факторами риска развития осложнений (иммуносупрессии, сахарный диабет, сердечно-сосудистые и хронические легочные заболевания).
Для купирования лихорадки, головной боли и миалгии при ОРВИ широко применяются представители группы нестероидных противовоспалительных препаратов (НПВП), которые наряду с жаропонижающим действием обладают анальгетическим эффектом. Наиболее безопасным и рекомендуемым препаратом является парацетамол, реже (в случае выраженной головной боли или миалгии) может использоваться ибупрофен. Применение ацетилсалициловой кислоты (Аспирин) должно быть ограничено, а у пациентов младше 18 лет и вовсе исключено с целью минимизации риска развития синдрома Рея. Применение нимесулида в рамках лечения ОРВИ также не рекомендовано, а в педиатрической практике запрещено.
С целью устранения назальной блокады и ринореи применяются сосудосуживающие средства— деконгестанты. К местным деконгестантам относятся: нафазолин (Нафтизин), ксилометазолин (Галазолин), оксиметазолин (Називин). По продолжительности сосудосуживающего действия наиболее эффективным является оксиметазолин (до 12 часов), чуть короче эффект у ксилометазолина (8–10 часов), для нафазолина и других представителей данной группы (тетризолин и инданазолин) характерен самый непродолжительный эффект (не более 4–6 часов). Среди всех местных деконгестантов оксиметазолин является одним из самых безопасных, напротив, препараты короткого действия (нафазолина нитрат) характеризуются наибольшим токсическим действием на клетки реснитчатого эпителия слизистой носа. В настоящее время оксиметазолин является единственным топическим деконгестантом, разрешенным МЗ РФ к применению у новорожденных и детей грудного возраста. Все топические деконгестанты нельзя использовать более 5 дней из-за опасности развития медикаментозного ринита, для препаратов короткого действия оптимальным сроком лечения является 3 дня. При длительном и бесконтрольном использовании возможно развитие атрофии слизистой носа. К основным правилам применения местных деконгестантов относятся следующие мероприятия: туалет носовой полости, затем, запрокинув голову, провести инстилляцию (порядка 5 капель препарата в каждую половину носа) и оставаться в такой позе в течение 2–3 мин после процедуры.
Из системных деконгестантов рекомендован к клиническому применению только один— фенилэфрин, однако его применение в ряде случаев сопряжено с развитием головной боли, головокружения, раздражительности; также при приеме фенилэфрина отмечается артериальная гипертензия, боли в области сердца и аритмия. Таким образом, назначение препаратов, содержащих фенилэфрин, пациентам с патологией сердечно-сосудистой системы должно быть ограничено. У детей фенилэфрин разрешен к применению только с 15-летнего возраста.
Для купирования насморка также используются антигистаминные препараты I поколения, обуславливающие свой эффект за счет побочного антихолинергического действия. К серьезным недостаткам данной группы препаратов относят выраженный седативный эффект, что не позволяет их использовать у социальноактивных пациентов (в числе противопоказаний— недопустимость вождения автомобиля и выполнение работ, требующих концентрации внимания).
Необходимо отметить, что препараты, содержащие кодеин и декстрометорфан, малоэффективны для лечения острого кашля, возникшего на фоне ОРВИ. Более того, их применение не рекомендовано при гриппе, особенно на ранних стадиях заболевания. Муколитики (ацетилцистеин, амброксол) показаны только при кашле с отхождением вязкой мокроты. Некоторые препараты— фенирамин и хлорфенирамин— H1-гистаминоблокаторы, кроме антигистаминного, оказывают также противокашлевое действие, в основе которого лежит угнетение кашлевого центра. Данные средства обладают выраженным седативным эффектом, поэтому их применение должно быть ограничено у определенных категорий заболевших (автолюбители).
Перечень клинических проявлений ОРВИ разнообразен и может проявляться как общетоксическим синдромом, так и катаральным с поражением различных уровней респираторного тракта. Для купирования симптомов болезни могут вполне оправданно применяться несколько классов лекарственных препаратов. Столь широкий перечень средств, необходимых для лечения, является попросту неудобным для пациента, тем более ведущего активный образ жизни. Решением данной проблемы явилось создание комбинированных/мультисимптомных средств, позволяющих воздействовать на основные симптомы вирусной инфекции. Кроме удобства применения, комбинированные препараты обладают более низкой стоимостью, чем набор различных лекарственных средств.
В подавляющем числе случаев рецептура комбинированных средств стандартная, содержащая жаропонижающий компонент— НПВП, системный деконгестант, антигистаминные препараты, аскорбиновую кислоту. Некоторые препараты содержат также противокашлевые средства (терпингидрат, гвайфеназин). При этом основным недостатком комбинированных препаратов является отсутствие у них противовирусного действия. В этом отношении привлекательным является использование препарата, способного оказывать как этиотропное (в отношении вируса гриппа А), так и симптоматическое действие— Антигриппина-максимум. Противовирусный эффект данного комбинированного средства обусловлен наличием в рецептуре блокатора М2-каналов— римантадина.
К сожалению, многообразие серотипов риновируса делает маловероятной перспективу создания эффективной вакцины. В настоящее время практическому здравоохранению доступна лишь противогриппозная вакцина. Разработанные недавно РСВ и парагриппозная вакцины проходят клинические испытания.
А. А. Зайцев, кандидат медицинских наук
ГИУВ МО РФ, Москва
Источник

МИНИСТЕРСТВО ОБОРОНЫ РОССИЙСКОЙ ФЕДЕРАЦИИ
97 ГОСУДАРСТВЕННЫЙ ЦЕНТР
СУДЕБНО-МЕДИЦИНСКИХ И КРИМИНАЛИСТИЧЕСКИХ ЭКСПЕРТИЗ
ЦЕНТРАЛЬНОГО ВОЕННОГО ОКРУГА
Начальник 97 ГЦ СМи КЭ (ЦВО) — Пудовкин Владимир Васильевич.
Авторы-составители:
1. Филиппенкова Елена Игоревна, врач — судебно-медицинский эксперт отдела судебно-медицинской экспертизы 97 Государственного центра судебно-медицинских и криминалистических экспертиз (Центральный военный округ), стаж экспертной работы 11 лет, высшая квалификационная категория.
2. Ларина Татьяна Викторовна, заведующая патологоанатомическим отделением № 27 Самарской городской клинической больницы № 1 имени Н.И. Пирогова, главный нештатный специалист по патологической анатомии Департамента здравоохранения г.о. Самара
ОРВИ, ТОКСИЧЕСКАЯ ФОРМА, ТЯЖЁЛОЕ ТЕЧЕНИЕ.
Труп женщины, 33 лет. Страдала гипертонической болезнью (2 стадия), ожирением 3 степени. За 6 дней до смерти повышение температуры до 40°С в течение первых 2-х дней, затем последующие 5 дней 37,5-38°С с нарастающим явлением дыхательной недостаточности.
ДАННЫЕ ГИСТОЛОГИЧЕСКОГО ИССЛЕДОВАНИЯ
СЕРДЦЕ (3объекта) — неравномерная окраска кардиомиоцитов. Неравномерное кровенаполнение миокарда с преобладанием выраженного венозно-капиллярного полнокровия с эритростазами. Неравномерно выраженный отёк стромы в виде расширения межмышечных пространств. В строме миокарда немногочисленные мелкие скопления по 2-4 лимфоцита. Представлены небольшие коронарные артерии с практически неизменёнными стенками, отдельные сосуды в состоянии выраженного спазма. В единичных полях зрения слабо выраженный периваскулярный кардиосклероз. Цитоплазма кардиомиоцитов зернистого вида. Слабо выраженные признаки дистрофии миокарда: на фоне субтотальной преимущественно умеренно выраженной гипертрофии немногочисленные отдельные мышечные волокна и мелкие пучки волокон истончены за счёт слабо выраженной атрофии, слабо выраженный очаговый периваскулярный липоматоз. Тотальная резко выраженная фрагментация, мелкоочаговая волнообразная деформация мышечных волокон миокарда.
Рис. 1. Миокард. Выраженный спазм коронарных артерий. Слабо выраженный периваскулярный кардиосклероз. Окраска: гематоксилин-эозин. Увеличение х250.
Рис. 2. Миокард. На фоне преобладания слабой-умеренной гипертрофии кардиомиоцитов отдельные мелкие пучки мышечных волокон истончены за счёт слабой атрофии. Окраска: гематоксилин-эозин. Увеличение х250.
Рис. 3, 4. Миокард. Очаговое венозно-капиллярное полнокровие с эритростазами. Преобладают кардиомиоциты в состоянии слабой-умеренной гипертрофии. Выраженная тотальная фрагментация мышечных волокон миокарда. Окраска: гематоксилин-эозин. Увеличение х250.
ЛЁГКИЕ (4объектов) — выраженное и резко выраженное диффузное венозно-капиллярное полнокровие с эритростазами, в отдельных сосудах разделение крови на плазму и форменные элементы, короткие сладжи эритроцитов, фибриновые микротромбы. Слабо выраженные диапедезные микрогеморрагии насыщенно-красного цвета. Стенки ряда сосудов утолщены, разрыхлены, разволокнены за счёт отёка, варьирующего от слабого до выраженного. Вокруг отдельных сосудов слабо-умеренные периваскулярные полиморфноклеточные инфильтраты с преобладанием лимфоцитов. Воздушность лёгочной ткани на всей площади срезов отсутствует или резко снижена: на фоне выраженного распространённого (практически массивного) альвеолярного отёка более ½-2/3 просветов альвеол с наличием небольших и слабо-умеренных скоплений сегментоядерных нейтрофильных лейкоцитов с чёткими контурами (лейкоциты в состоянии распада не видны), рыхло расположенных тонких бледно-розовых нитей фибрина, немногочисленных макрофагов. В одном из объектов в просветах большого количества альвеол по ходу межальвеолярных перегородок, а также в виде «муфт» и полулуний вокруг сосудов расположены преимущественно нежные гомогенные розовые гиалиновые мембраны, в этом же объекте обнаружены многоядерные макрофаги. В просветах большого количества альвеол пласты слущенного бронхиального эпителия, слущенные альвеоциты. Представлены небольшие бронхи с тотальной десквамацией мерцательного эпителия, умеренно выраженными отёком и лейкоцитарной инфильтрацией, просветы бронхов содержат слущенный эпителий в виде пластов и отдельных клеток, большое количество отёчной жидкости, часть просветов бронхов полностью заполнено отёчной жидкостью. Лёгочная плевра утолщена, разрыхлена за счёт слабо выраженного и слабо-умеренного отёка, со слабо выраженным диапедезом частично гемолизированных эритроцитов, без признаков склероза и воспаления.
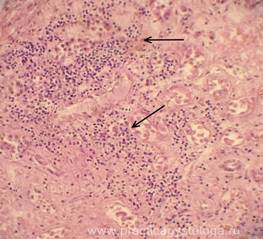
Рис. 5-12. Лёгкие. На фоне выраженного массивного альвеолярного отёка отдельные сосуды с картиной полиморфноклеточного васкулита, в просветах альвеол небольшое и умеренное количество сегментоядерных нейтрофильных лейкоцитов с сохранёнными ядрами, контурами, небольшое количество рыхло расположенных тонких нитей фибрина, немногочисленные многоядерные макрофаги. Окраска: гематоксилин-эозин. Увеличение х250.
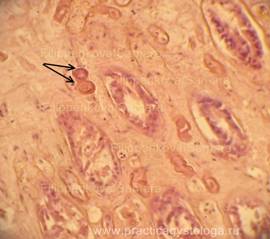
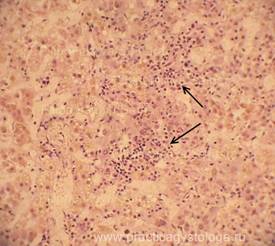
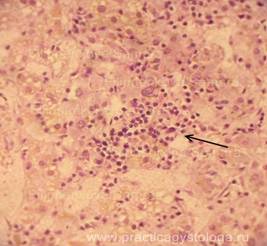
Рис. 13-20. Лёгкие. На фоне выраженного массивного альвеолярного отёка в просветах большого количества альвеол по ходу межальвеолярных перегородок, а также в виде «муфт» и полулуний вокруг сосудов расположены преимущественно нежные гомогенные розовые гиалиновые мембраны (стрелки). Окраска: гематоксилин-эозин. Увеличение х250. х400.
Рис. 21. Лёгкое. На фоне венозно-капиллярного полнокровия, выраженного массивного альвеолярного отёка немногочисленные многоядерные макрофаги.
Окраска: гематоксилин-эозин. Увеличение х250.
Рис. 22. Лёгкое. Картина полиморфноклеточного васкулита (стрелка).
Окраска: гематоксилин-эозин. Увеличение х250.
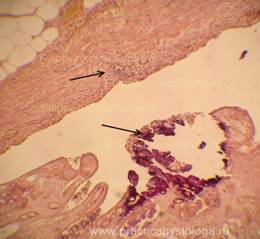
Рис. 23, 24. Лёгкие. Представлены небольшие бронхи с тотальной десквамацией мерцательного эпителия, умеренно выраженными отёком и слабо выраженной лейкоцитарной инфильтрацией, просветы бронхов содержат слущенный эпителий в виде пластов и отдельных клеток, большое количество отёчной жидкости, часть просветов бронхов полностью заполнено отёчной жидкостью. Окраска: гематоксилин-эозин. Увеличение х250.
ПЕЧЕНЬ (1объект) — в срезах неравномерный начальный аутолиз. На фоне умеренного кровенаполнения синусоидных капилляров диффузно расположены очаги умеренного их полнокровия. Центральные вены и вены портальных трактов либо с пустыми просветами, либо с заполнением просветов частично гемолизированной кровью. Балочно-радиарное строение печёночных долек чёткое. Цитоплазма гепатоцитов зернистого вида. До 15-20% гепатоцитов центролобулярно в различной степени подверглись мелко -, средне — и крупнокапельному ожирению. Незначительное очаговое явление холестаза. Портальные тракты практически не расширены. В строме отдельных портальных трактов и в строме единичных долек мелкие очаги полиморфноклеточной инфильтрации стромы с преобладанием лимфоцитов. Стенки артерий триад и желчных протоков не изменены.
Рис. 25, 26. Печень. До 15-20% гепатоцитов центролобулярно в различной степени подверглись мелко -, средне — и крупнокапельному ожирению. Незначительное очаговое явление холестаза. Окраска: гематоксилин-эозин. Увеличение х250.
Рис. 27. Печень. В строме долек, а также в строме портальных трактов мелкоочаговая слабо выраженная полиморфноклеточная инфильтрация с преобладанием лимфоцитов. Окраска: гематоксилин-эозин. Увеличение х250.
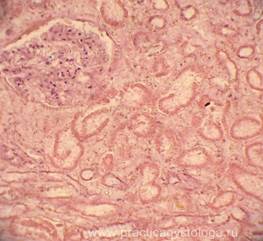
ПОЧКИ (3объекта) — в срезах диффузный аутолиз ближе к умеренному. Просветы ряда сосудов заполнены гемолизированной кровью. В отдельных полях зрения группы небольших сосудов с умеренным циркулярным утолщением стенок, их гомогенизацией, в строме очаговое и диффузное разрастание соединительной ткани со слабо-умеренной пролиферацией фибробластов. В подкапсульной зоне крупный очаг выраженной полиморфноклеточной инфильтрации стромы с преобладанием лимфоцитов. Единичные клубочки склерозированы. В одном из объектов более ½ канальцев с признаками их атрофии (снижена высота эпителия, просветы расширены). В другом объекте в толще склерозированной капсулы почки очаговая слабо-умеренная лимфогистиоцитарная инфильтрация, в подкапсульной зоне средней величины очаговый кальцинат.
|
|
Рис. 28. Почка. В подкапсульной зоне крупный очаг выраженной полиморфноклеточной инфильтрации стромы (стрелки) с преобладанием лимфоцитов. Окраска: гематоксилин-эозин. Увеличение х250. | Рис. 29. Почка. На фоне аутолиза крупная группа канальцев коркового вещества с признаками атрофии ближе к умеренной (эпителий истончён, просветы расширены). Окраска: гематоксилин-эозин. Увеличение х250. |
|
|
Рис. 30. Почка. На фоне аутолиза группа мелких сосудов со значительным циркулярным утолщением стенок, их гомогенизацией (стрелки). Окраска: гематоксилин-эозин. Увеличение х250. | Рис. 31. Почка. В капсуле почки очаговая полиморфноклеточная инфильтрация с преобладанием лимфоцитов (верхняя стрелка). В веществе почки в подкапсульной зоне средних размеров очаговый кальцинат (нижняя стрелка). Окраска: гематоксилин-эозин. Увеличение х100. |
СЕЛЕЗЁНКА (1объект) — в срезах аутолиз ближе к слабо-умеренному. Полнокровие и геморрагическое пропитывание красной пульпы. Слабо выраженная атрофия ряда фолликулов, стенки центральных артерий фолликулов практически не изменены. Трабекулы не утолщены.
НАДПОЧЕЧНИКИ (1объект) — в срезах неравномерный начальный аутолиз. Представлен практически только корковый слой надпочечника. На фоне преобладания слабо-умеренного кровенаполнения диффузно расположены единичные среднего сечения полнокровные венозные сосуды, а также небольшие группы полнокровных капилляров. Диффузная делипоидизация цитоплазмы клеток коркового слоя, варьирующая от умеренной до выраженной. В сетчатой зоне коркового слоя очаговая слабо-умеренная полиморфноклеточная инфильтрация стромы с преобладанием лимфоцитов, с немногочисленными лейкоцитами, макрофагами. Небольшие группы клеток коркового слоя со слабо выраженным липофусцинозом цитоплазмы.
|
|
Рис. 32, 33. Надпочечник (сетчатая зона коркового слоя). Очаговая слабо-умеренная полиморфноклеточная инфильтрация стромы (стрелки) с преобладанием лимфоцитов, с немногочисленными лейкоцитами, макрофагами. Выраженная делипоидизация цитоплазмы клеток коркового слоя. Окраска: гематоксилин-эозин. Увеличение х250, х400. | |
ПОДЖЕЛУДОЧНАЯ ЖЕЛЕЗА (1объект) — в срезах неравномерный (ближе к слабо-умеренному) аутолиз. Очаговое венозно-капиллярное полнокровие. Стенки артериол и мелких артерий слабо циркулярно утолщены, несколько разрыхлены. Неравномерное расширение междольковых пространств. Диффузно расположены крупные и средней величины очаги липоматоза. Инсулярные островки Лангерганса в данных срезах не видны.
ГИСТОЛОГИЧЕСКОЕ ЗАКЛЮЧЕНИЕ
Преобладает полнокровие внутренних органов. Нарушения реологических свойств крови в виде эритростазов (в срезах миокарда, лёгких), сладжирования эритроцитов (в срезах лёгких), разделения крови на плазму и форменные элементы (в срезах лёгких). Фибриновые микротромбы в срезах лёгких.
В сердце — слабо выраженный периваскулярный кардиосклероз, слабо выраженные признаки дистрофии миокарда, тотальная резко выраженная фрагментация, мелкоочаговая волнообразная деформация мышечных волокон миокарда (как признаки возможного нарушения ритма сердца).
В лёгких — картина острой сливной гнойно-фибринозной бронхопневмонии с признаками респираторного дистресс-синдрома, на фоне выраженного распространённого (вплоть до массивного) альвеолярного отёка.
В печени — до 15-20% гепатоцитов центролобулярно в различной степени подверглись мелко -, средне — и крупнокапельному ожирению, слабо выраженная картина хронического персистирующего гепатита.
В почках — картина полиморфноклеточного (преимущественно продуктивного) нефрита с формированием очагового нефросклероза, очаговыми кальцинатами, атрофией групп канальцев.
В селезёнке — слабо выраженная атрофия ряда фолликулов.
В надпочечниках — умеренная-выраженная диффузная делипоидизация цитоплазмы коркового слоя.
В поджелудочной железе — очагово-диффузный средне — и крупноочаговый липоматоз.
Сочетание в гистологической картине выраженного венозно-капиллярного полнокровия в лёгких с эритростазами, диапедезными микрогеморрагиями, фибриновых микротромбов, выраженного процесса десквамации бронхиального и альвеолярного эпителия, массивного альвеолярного отёка, наличия гиалиновых мембран (свидетельствующих о респираторном дистресс-синдроме), многоядерных макрофагов, а также полиморфноклеточных инфильтратов с преобладанием лимфоцитов в срезах миокарда, лёгких (периваскулярно), печени, почки, надпочечника свидетельствует об имевшейся у гр-ки Х., 1978г.р. острой респираторной вирусной инфекции с тяжёлым течением, осложнившейся развитием острой очаговой сливной гнойно-фибринозной вирусно-бактериальной пневмонии.
Источник