Ревматоидный артрит атланто аксиального сочленения
Более 85% пациентов с умеренным или выраженным ревматоидным артритом (РА) имеют рентгенологические признаки поражения шейного отдела позвоночника. О поражении верхних шейных позвонков. Ниже 2-го позвонка наиболее частым видом нарушений являются подвывихи.
Классификация степени неврологических нарушений, предложена Ранаватом с соавт., приведена в табл. 11-23. Она также используется и при других типах повреждений СМ.
Табл. 11-23. Классификация неврологических нарушений по Ранавату

Поражение верхнешейного отдела позвоночника
Поражение верхнешейного отдела при РА наблюдается в 44-88% случаев. Нарушение оси или нестабильность развиваются в результате разрушения кости и поддерживающих связок при синовиальной пролиферации. Степень поражения может быть от незначительной (несколько мм асимптомного подвывиха) до тяжелой (напр., компрессия ствола мозга).
Два типичных варианта поражения шейного отдела при РА (часто могут наблюдаться совместно):
1. передний атланто-аксиальный подвывих (ААП): наиболее частый вариант проявления РА в шейном отделе, встречается у 25% пациентов с РА
2. базилярная импрессия (БИ): смещение зубовидного отростка вверх, встречается приблизительно у 8% пациентов с РА
Более редкие варианты поражения шейного отдела при РА:
1. задний подвывих атланто-аксиального сустава: должны быть либо сопутствующий перелом, либо практически полное разрушение зубовидного отростка в результате артрита
2. субаксиальные подвывихи (подвывихи ниже С2)
3. вертебральная недостаточность в результате изменений в кранио-вертебральной области
Атланто-аксиальный подвывих при ревматоидном артрите
Воспаление атланто-аксильных синовиальных суставов вызывает эрозивные изменения зубовидного отростка, декальцификацию, ослабление фиксации поперечной связки к атланту. Это ведет к нестабильности и формированию переднего подвывиха атланта по отношению ко 2-ому позвонку. Существуют 2 механизма возникновения компрессии верхней части СМ: 1)»эффект ножниц» между С1 и С2, 2)образование паннуса грануляционной ткани вокруг зубовидного отростка.
Атланто-аксиальный подвывих (ААП) встречается приблизительно у 25% пациентов с РА294. Средний срок продолжительности симптомов РА и диагностики ААП составил 14 лет (15 пациентов).
Клинические проявления
Жалобы и симптомы ААП приведены в табл. 11-24.
Табл. 11-24. Жалобы и симптомы при атланто-аксиальном подвывихе (15 больных с ААП)

Боль бывает локальная (верхняя часть шеи, подзатылочная область, часто в результате компрессии корешка С2) или отдаленная (в сосцевидной, затылочной, височной или лобной областях).
Рентгенологическая диагностика
Боковые обзорные шейные спондилограммы
Расстояние между атлантом и зубовидным отростком
В норме расстояние между передним краем зубовидного отростка и выступом С1 на боковой шейной спондилограмме у взрослых должно быть <4 мм. Увеличение этого расстояния говорит о возможной несостоятельности поперечной связки.
МРТ
МРТ является оптимальным способом определения причин компрессии верхней части СМ и продолговатого мозга. При этом видны положение зубовидного отростка, степень паннуса, влияние подвывиха (для того, чтобы оценить это исследование следует проводить с согнутой вперед головой).
Лечение
Следует учитывать следующую информацию:
• естественное течение: у большинства пациентов ААП прогрессирует, только у небольшого числа из них наступает стабилизация или спонтанный спондилодез. В серии при среднем сроке наблюдения в течение 4,5 лет у 45% пациентов с подвывихом 3,5-5 мм наступило его увеличение до 5-8 мм, а у 10% даже >8 мм
• наступившая миелопатия является необратимой
• чем выраженнее миелопатия, тем выше риск внезапной смерти
• при подвывихе ≥9 мм шансы обнаружения миелопатии значительно возрастают
• сопутствующее оседание черепа еще больше снижает переносимость больным ААП
• летальность и осложнения при хирургическом лечении
В каких случаях показано лечение?
• симптоматические пациенты с ААП: практически все требуют операций (в большинстве случаев проволочная фиксация С1-2).
• некоторые хирурги не оперируют больных, если max расстояние между атлантом и зубовидным отростком <6 мм
• асимптомные пациенты: спорно
• некоторые авторы считают, что хирургический спондилодез не требуется у асимптомых пациентов, если расстояние между атлантом и зубовидным отростком меньше какой-то величины. При этом рекомендации о величине этого предельного расстояния разнятся от 6 до 10 мм (наиболее часто указывается 8 мм)
• больным часто назначают ношение стабилизирующего воротника, напр., вне дома, хотя большинство признает, что воротник вероятно не обеспечивает значительной поддержки или предохранения
• NB: в некоторых случаях у пациентов с РА в результате ААП может наступить внезапная смерть, что в дальнейшем может быть ошибочно расценено как следствие сердечной аритмии и т.д. Поэтому всех асимптомных пациентов с выраженной нестабильностью (что определяется расстоянием между атлантом и зубовидным отростком) надо оперировать
Тактика
Следует или уменьшить степень подвывиха или осуществить декомпрессию верхней части СМ до того, как производить С1-2 или затылочный-С1-2 спондилодез.
Менезес оценивал степень вправляемости подвывихов с помощью системы тракции за головной обруч, совместимой с МРТ, у всех пациентов следующим образом: начальное вытяжение 2,5 кг, которое в течение нед постепенно увеличивали. В большинстве случаев вправление наступало в течение 2-3 д. Если после 7 д вправление не наступало, то подвывих, по-видимому, был невправимым. Невправимые подвывихи наблюдались только приблизительно 20% случаев (в большинстве из них зубовидный отросток располагается на 15 мм выше БЗО).
В большинстве случаев требовалась стабилизация с помощью заднего спондилодеза С1 и С2 проволокой или даже затылочной кости и С2. К последней прибегали в тех случаях, когда спондилодез сочетался с декомпрессией (ламинэктомия С1 с задним увеличением БЗО).
При невправимых подвывихах или значительной компрессии паннусом операция заднего спондилодеза проволокой не является достаточной. В этих случаях может быть показано трансоральное удаление зубовидного отростка (одонтоидэктомия). Первоначальное осуществление задней стабилизации и декомпрессии позволяет некоторым пациентам избежать второй операции, а остальным – сохранить стабильность позвоночника при осуществлении переднего доступа. Тем не менее, некоторые хирурги все же сначала производят одонтоидэктомию.
Напоминание: для того, чтобы можно было осуществить переднюю одонтоидэктомию без распила нижней челюсти, пациент должен быть способен открыть рот >25 мм.
Задний спондилодез проволокой
При РА дужка атланта ослаблена в результате эрозии и остеопороза, поэтому требуется особая осторожность, чтобы избежать ее перелома.
Летальность и осложнения
В результате наличия сопутствующего поражения других систем (легочной, сердечной, эндокринной) п/о летальность составляет 5-15%.
Хотя есть сообщение о том, что частота неудачного спондилодеза С1-2 при фиксации проволокой может достигать 50%, в большинстве случаев она ниже (возможно формирование фиброзной мозоли, что в серии больных наблюдалось в 18% случаев).
Костное сращение чаще всего не наступало в промежутке между костным трансплантатом и задней дужкой С1.
Послеоперационное ведение
Пациента можно активизировать сразу же после операции в корсете «обруч-жилет», обеспечивающем тракцию. Некоторые хирурги сначала осуществляют тракцию в течение какого-то времени до мобилизации больного. В связи с нарушенным процессом заживления при РА пациент должен быть в этом корсете до тех пор, пока на спондилограммах не наступит сращение (обычно 8-12 нед). Соннтаг контролирует наступление сращения с помощью боковых шейных спондилограмм со сгибанием и разгибанием, для чего разъединяют головной обруч и жилет.
Базилярная импрессия при ревматоидном артрите
Эрозивные изменения боковых масс С1 → оседание атланта на тело С2 с вентральным смещением С1, что приводит к уменьшению передне-заднего диаметра СМК. При этом имеется сопутствующее смещение зубовидного отростка вверх. Задняя дуга С1 часто внедряется в БЗО. Все эти изменения приводят к компрессии моста и продолговатого мозга. Дополнительным фактором является разрастание ревматоидной грануляционной ткани позади зубовидного отростка. Также определенную роль играет закупорка ВА.
Степень эрозии С1 соответствует выраженности инвагинации зубовидного отростка.
Клинические проявления
См. табл. 11-25. Оценка двигательных нарушений затруднена в связи с выраженной полиартритной дегенерацией, сопровождающейся болью. Чувствительные нарушения (не позволяют локализовать патологию): понижение вибрационной, проприоцептивной и поверхностной чувствительности.
Табл. 11-25. Жалобы и симптомы при базилярной импрессии (45 больных с ревматоидным артритом)

Политомография: во многих госпиталях в настоящее время уже нет возможности ее проведения. Лучше всего показывает костные изменения. Для определения нестабильности оптимальными являются боковые политомограммы со сгибанием и разгибанием.
Миелография (с водорастворимым КВ) с последующей КТ: также хорошо показывает костные изменения.
МРТ: оптимально показывает сдавление ствола мозга, плохо костные изменения.
Лечение.
Шейное вытяжение
Можно осуществить скобой Гарднера-Уэллса. Начинают с 3,5 кг и медленно увеличивают до 8 кг. В некоторых случаях для вправления требуется несколько нед вытяжения.
Хирургическое лечение
Вправимые случаи: задний затылочно-шейный спондилодез ± декомпрессивная ламинэктомия С1.
Невправимые случаи: требуется трансоральная резекция зубовидного отростка. Ее можно осуществить до заднего спондилодеза (пациент должен оставаться на вытяжении до второй операции).
Гринберг. Нейрохирургия
Опубликовал Константин Моканов
Источник
Ревматоидный артрит шейного отдела позвоночника — методы диагностики, лечения по Европейским рекомендациям
а) Определение. Ревматоидный артрит (РА) — это заболевание синовиальных суставов. В основном поражается шейный отдел позвоночника. Хроническое воспаление с разрушением костных структур и связочного аппарата приводит к нестабильности и деформации.
б) Этиология/эпидемиология. Мнения о патогенезе ревматоидного артрита (РА) противоречивы. Предметом обсуждения является вопрос: с чего начинается процесс? С апофизарных суставов с последующей деструкцией фасеток и вторичной нестабильностью диска или с воспаления унковертебральных сочленений совместно с первичным разрушением диска и вторичной нестабильностью апофизарных суставов.
Подвывих может быть легким, без клинических симптомов или тяжелым, с компрессией ствола головного мозга и верхнего шейного отдела спинного мозга. Возможны два варианта типичного проявления, часто одновременно: передний атлантоаксиальный подвывих и базилярная импрессия. Подвывих в нижнем шейном отделе позвоночника встречается реже и может напоминать «лестничный» подвывих в результате слабости связочного аппарата и дегенеративных изменений фасеток.
1. Передний атлантоаксиальный подвывих: встречается у 74% пациентов с ревматоидным артритом (РА), поражающим шейный отдел позвоночника и у 25% пациентов с ревматоидным артритом (РА). Зубовидный отросток окружен двумя синовиальными суставами: вентральным между зубом и атласом и дорсальным между зубом и поперечной связкой.
Деструкция связки с развитием связочной слабости связана с воспалением и разрушением, заканчивающимся потерей целостности связки и передним смещением. Заднее смещение возможно при значительном поражении самого зуба. Участие С1/С2 суставов может привести к боковым смещениям. Формированние паннуса вокруг зуба в последующем дополнительно способствует компрессии ствола мозга и верхней части шейного отдела спинного мозга.
2. Базилярная импрессия: вовлечение атлантозатылочного сочленения может привести к уничтожению фасеток и прогрессивному смещению затылочной кости на С1 и перемещению зуба по вертикали. Иногда задняя арка С1 выступает вверх через большое затылочное отверстие приводя к дополнительной компрессии моста и продолговатого мозга.
в) Симптомы. Боль (местная), признаки миелопатии с гиперрефлексией, парезы, спастичность и сенсорные нарушения.
г) Диагностика ревматоидного артрита шейного отдела позвоночника:
• Обычная рентгенография: поиск атлантоаксиального подвывиха (передней интервал зубовидного отростка не должен превышать 4 мм).
• МРТ: необходимо искать изменения сигнала спинного мозга и подвывих. Иногда сгибание головы помогает увидеть компрессию спинного мозга, следовательно, нормальные данные МРТ могут имитировать достаточный диаметр позвоночного канала.
• КТ (осмотреть передней интервал зубовидного отростка, а при планировании трансартикулярной фиксации С1/С2 оценить анатомию позвоночной артерии).
д) Лечение ревматоидного артрита шейного отдела позвоночника. Почти у всех пациентов заболевание будет прогрессировать с течением времени, а затем разовьется миелопатия, которая может быть необратимой. Тяжелая миелопатия может привести к внезапной смерти, поэтому при симптоматическом течении требуется хирургическое лечение, а в бессимптомных случаях принятие решения проводится при оценке риска.
Учитываются тяжесть атлантоаксиального подвывиха, возраст, общее состояние здоровья пациента и любые сопутствующие заболевания. Тем не менее, бессимптомные пациенты со значительной нестабильностью нуждаются в хирургическом лечении. Оперативные методы:
• Пре- или интраоперационное сокращение подвывиха под контролем рентгенографии или нейрофизиологического мониторинга.
• С1/С2 фиксация или С0/С2 фиксация: последняя проводится при декомпрессии позвоночного канала (ламинэктомия).
• При субаксиальной нестабильности фиксация должна быть усилена.
• В редких случаях проводится трансоральная резекция зуба (одонтоидэктомия).
• Хирургические методы:
— С1/С2 фиксация с или без костного аутотрансплантата, трансартикулярная установка винтов С1/С2.
— Для затылочно-шейной инструментации доступны различные системы (Cervifix, Neon, петля Ransford, и т. п.).
• Послеоперационная иммобилизация с помощью жесткого воротника: некоторые авторы рекомендуют галофиксацию в течение 8-12 недель.
е) Прогноз ревматоидного артрита шейного отдела позвоночника. После операции у двух третей пациентов отмечено облегчение или уменьшение боли и улучшение функциональных способностей. Неврологические дефициты ослабляются у 53% пациентов. Помимо горизонтального подвывиха независимыми предикторами смертности и возникновения осложнений были возраст и атлантоаксиальный подвывих. После фиксации С1/С2 отмечена высокая частота развития последующей субаксиальной шейной нестабильности.
Ревматоидный артрит.
(а) Движения в шейном отделе позвоночника значительно ограничены, попытки повернуть голову приводят к усилению болевого синдрома и спазмированию мышц.
(б) Подвывихи в атланто-аксиальном сочленения встречаются достаточно часто: эрозивное поражение суставов этого сочленения и поперечной связки атланта создают условия для «соскальзывания» первого шейного позвонка кпереди до 2 см.
(в) Репозиция первого шейного позвонка и задний спондилодез с фиксацией проволочной петлей.
(г) У данного пациента наблюдаются подвывихи не только в атланто-аксиальном сочленении, но также и в двух сегментах средне-шейного отдела позвоночника.
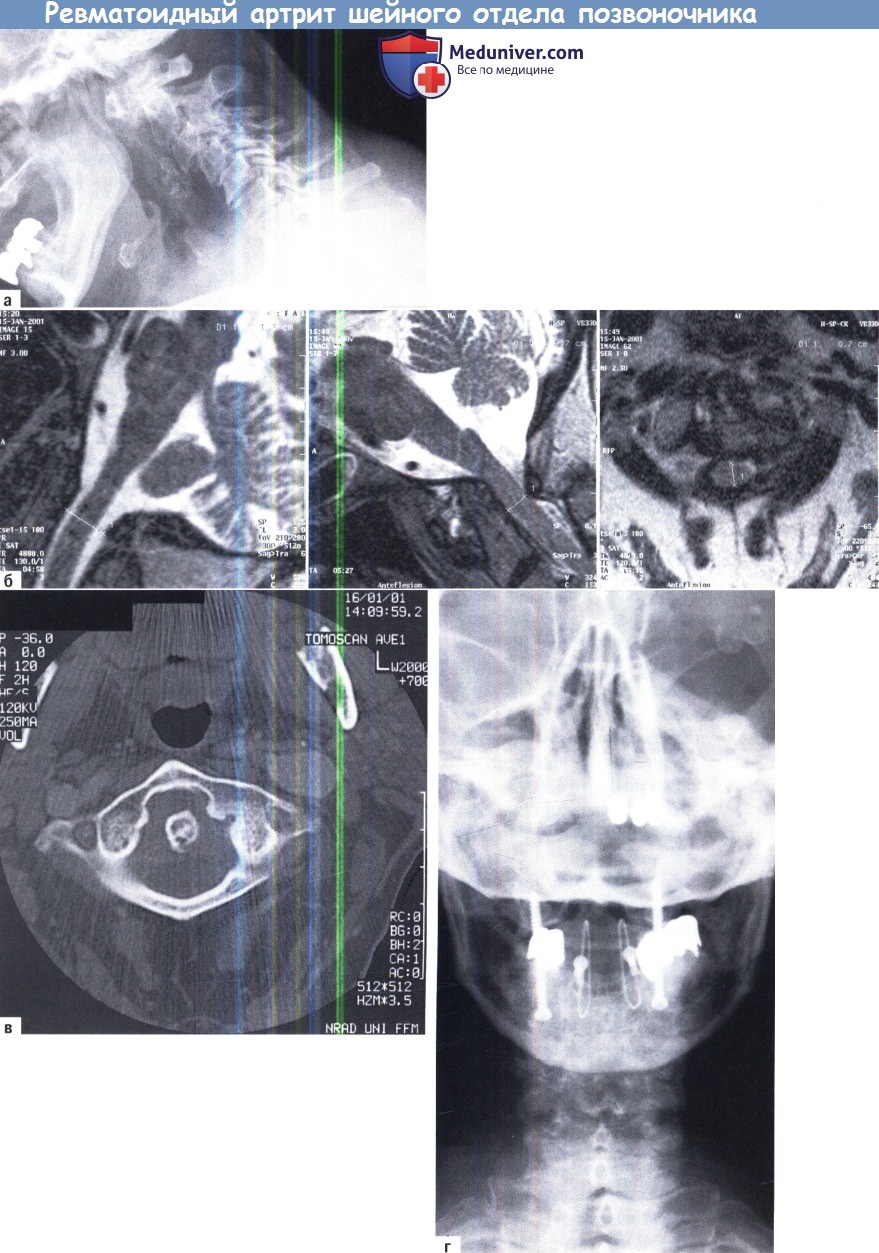
А. Обычная рентгенография (боковая проекция) у пациента с ревматоидным артритом (РА), С1/С2 нестабильностью и стенозом на уровне шейного отдела позвоночника.
Б. При МРТ измерен достаточный диаметр позвоночного канала при разгибании (слева) головы, но при сгибании (в центре) выявлена компрессия продолговатого мозга.
На аксиальном срезе МРТ (справа) подтверждается компрессия спинного мозга.
В. Аксиальный срез КТ (костный режим) показывает увеличение передней зубовидного интервала.
Г. Обычная рентгенография шейного отдела позвоночника (переднезадняя проекция) после двусторонней С1/2 трансартикулярной фиксации и С1/С2 субламинарной фиксации с аутологичным костным имплантом для слияния С1 и С2.
— Также рекомендуем «Анкилозирующий спондилоартрит (болезнь Бехтерева) — методы диагностики, лечения по Европейским рекомендациям»
Оглавление темы «Нейрохирургия дегенеративных болезней позвоночника.»:
- Грыжа шейного отдела позвоночника — методы диагностики, лечения по Европейским рекомендациям
- Шейный спондилез — методы диагностики, лечения по Европейским рекомендациям
- Стеноз шейного отдела позвоночника — методы диагностики, лечения по Европейским рекомендациям
- Шейная миелопатия — методы диагностики, лечения по Европейским рекомендациям
- Оссификация задней продольной связки — методы диагностики, лечения по Европейским рекомендациям
- Ревматоидный артрит шейного отдела позвоночника — методы диагностики, лечения по Европейским рекомендациям
- Анкилозирующий спондилоартрит (болезнь Бехтерева) — методы диагностики, лечения по Европейским рекомендациям
- Грыжа грудного отдела позвоночника — методы диагностики, лечения по Европейским рекомендациям
- Стеноз грудного отдела позвоночника — методы диагностики, лечения по Европейским рекомендациям
- Болезнь Шейерманна-Мау (ювенильный кифоз) — методы диагностики, лечения по Европейским рекомендациям
Источник
Overview of Rheumatoid Spondylitis
The most common sites of rheumatoid arthritis (RA) are the metatarsophalangeal joints, followed by the metacarpophalangeal joints and the cervical spine (ankylosing spondylitis, rheumatoid spondylitis). Much of the understanding of spinal afflictions in rheumatoid arthritis was advanced by studies published in the 1950s and 1960s.[1] In 1951, Davis and Markley detailed medullary compression as a cause of death in patients with rheumatoid arthritis.[2] In 1969, Mathews reported that 25-30% of patients with rheumatoid arthritis who were admitted to the hospital had radiographic evidence of cervical spine involvement.[3]
Rheumatoid spondylitis (ankylosing spondylitis) primarily affects the cervical spine. Affliction of the thoracic or lumbar spine is rare. The anatomic abnormalities occur as a consequence of the destruction of synovial joints, ligaments, and bone. Abnormalities of the rheumatoid cervical spine generally can be grouped into 3 categories that may be seen in isolation or combined involvement, of which atlantoaxial instability (AAI) or atlantoaxial subluxation (AAS) is the most common abnormality (see the image below). AAS can be a fixed deformity or can be partially or fully reducible.
Rheumatoid spondylitis. Depiction of anterior subluxation of C1 on C2, retrodental pannus, and osseous erosions; the spinal cord is compressed between the pannus anteriorly and the posterior arch of the atlas.
Superior migration of the odontoid (SMO) is the next most common abnormality and has alternately been referred to as cranial settling, pseudobasilar invagination, or vertical/upward translocation of the odontoid (see the following images).[4] The third and least common deformity is subaxial subluxation, which may be seen at multiple levels and produces a stepladder deformity.
Rheumatoid spondylitis. Depiction of superior migration of the odontoid into the foramen magnum with compression of the spinal cord.
Rheumatoid spondylitis. Pertinent measurements of superior migration of the odontoid; cranial migration distance (CMD).
For patient education information, see eMedicine’s Arthritis Center, as well as Rheumatoid Arthritis and Rheumatoid Arthritis Medications.
Go to Rheumatoid Arthritis and Ankylosing Spondylitis for more information on these topics.
Prevalence of Rheumatoid Spondylitis
Numerous investigators have attempted to elucidate the natural history of rheumatoid arthritis as it affects the cervical spine (rheumatoid spondylitis, ankylosing spondylitis), with wide variation in their findings.[5, 6, 7, 8, 9]
Of the 0.8% of the white population in the United States and Europe affected by rheumatoid arthritis, neck pain is reported in 40-88% of patients. The prevalence of cervical spine involvement (rheumatoid spondylitis, ankylosing spondylitis) in rheumatoid arthritis ranges from 25% to 80%, depending on the diagnostic criteria applied.[10] However, only 7-34% of patients with rheumatoid arthritis have a neurologic deficit. A substantial number of patients with radiographic instability or neck pain do not develop neurologic deficits.[11]
Involvement of the cervical spine typically begins early in the disease process and often parallels the extent of peripheral disease. Of the 3 types of involvement, atlantoaxial instability (AAI) is the most common, occurring in up to 49% of patients.[12] Whereas most of these subluxations are anterior, approximately 20% are lateral and approximately 7% are posterior. Superior migration of the odontoid (SMO) is seen in up to 38% of patients with rheumatoid arthritis. Subaxial subluxation is seen as a discrete pathologic entity in 10-20% of patients.
Subaxial subluxation also develops after previous upper cervical fusions.[13, 14] In one series of 79 patients, 36% developed subaxial subluxation at an average of 2.6 years following occipitocervical fusion, and 5.5% experienced subaxial subluxation an average of 9 years following atlantoaxial fusion.[13]
Pathophysiology of Rheumatoid Spondylitis
Recent theories on the pathogenesis of rheumatoid arthritis suggest that the synovial cells of these patients chronically express an antigen that triggers the production of rheumatoid factor (RF), an immunoglobulin molecule directed against other autologous immunoglobulins. An inflammatory response is initiated, involving immune complex formation, activation of the complement cascade, and infiltration of polymorphonuclear leukocytes. The proliferating fibroblasts and inflammatory cells produce granulation tissue, known as rheumatoid pannus, within the synovium. The pannus produces proteolytic enzymes capable of destroying adjacent cartilage, ligaments, tendons, and bone. The destructive synovitis results in ligamentous laxity and bony erosion with resultant cervical instability and subluxation.[15, 16]
Atlantoaxial subluxation results from erosive synovitis in the atlantoaxial, atlanto-odontoid, and atlanto-occipital joints and the bursa between the odontoid and the transverse ligament (see the image below).
Rheumatoid spondylitis. Depiction of anterior subluxation of C1 on C2, retrodental pannus, and osseous erosions; the spinal cord is compressed between the pannus anteriorly and the posterior arch of the atlas.
The superior migration of the odontoid is attributed to erosion and bone loss in the occipitoatlantal and atlantoaxial joints (see the following images).
Rheumatoid spondylitis. Depiction of superior migration of the odontoid into the foramen magnum with compression of the spinal cord.
Rheumatoid spondylitis. Pertinent measurements of superior migration of the odontoid; cranial migration distance (CMD).
Subaxial subluxation results from destruction of the facets, intervertebral discs, and interspinous ligaments. Unlike degenerative disease, involvement of C2-C3 and C3-C4 is common, and osteophytes are seldom seen.
Evaluation of Rheumatoid Spondylitis
Rheumatoid involvement of the cervical spine (rheumatoid spondylitis, ankylosing spondylitis) is just one element in a systemic disease process. Cervical involvement often correlates with the degree of hand and wrist erosion. Cervical involvement also has been associated with the presence of rheumatoid nodules and the use of corticosteroids. Classically, craniocervical neck pain often is associated with occipital headaches.
Symptoms
Compression of the C2 sensory fibers supplying the nucleus of the spinal trigeminal tract can cause facial pain. Compression of the C2 sensory fibers supplying the greater auricular nerve may result in ear pain. Occipital neuralgia results from compression of the C2 sensory fibers supplying the greater occipital nerve. A history of myelopathic symptoms should be sought carefully. Patients may experience weakness, decreased endurance, gait difficulty, paresthesias of the hands, and loss of fine dexterity. Patients with involvement may experience and, eventually, incontinence.
Vertebrobasilar insufficiency may be found, particularly in patients with atlantoaxial instability (AAI). Complaints may include vertigo, loss of equilibrium, visual disturbances, tinnitus, and dysphagia. Similar symptomatology can also be caused by mechanical compression of the brainstem. In some patients, neck motion can elicit shocklike sensations through the torso or into the extremities (ie, Lhermitte sign).
Physical findings
The physical inventory of these patients frequently is confounded by the severity of their peripheral rheumatoid involvement. Weakness in these patients can also be due to tenosynovitis, tendon rupture, muscular atrophy, peripheral nerve entrapment, or articular involvement, making neurologic impairment less obvious. Signs of myelopathy should raise suspicion of cervical involvement. Rarely, cranial nerve dysfunction can occur secondary to compression of the medullary nuclei by the odontoid. Other rare findings in patients with advanced brainstem compression include vertical nystagmus and Cheyne-Stokes respirations.
Classification of Neurologic Deficits
The Ranawat classification can be used to categorize patients with rheumatoid myelopathy based on their clinical history and physical findings (see below).[17] This classification has some utility in determining the potential for neurologic recovery following surgery and is categorized as follows[17] :
Class I — No neural deficit
Class II — Subjective weakness, dysesthesias, and hyperreflexia
Class IIIA — Objective weakness and long-tract signs; patient remains ambulatory
Class IIIB — Objective weakness and long-tract signs; patient no longer ambulatory
Diagnostic Studies
Rheumatoid factor seropositivity has been correlated with more extensive cervical involvement (rheumatoid spondylitis, ankylosing spondylitis). The use of the rheumatoid factor as a predictor of neurologic involvement has not been established; therefore, it does not have a role in the surveillance of patients with rheumatoid arthritis with cervical involvement.
All patients with rheumatoid arthritis should have radiographic examination of the cervical spine because cervical involvement (rheumatoid spondylitis, ankylosing spondylitis) can remain asymptomatic. Imaging modalities include plain radiography, magnetic resonance imaging (MRI), polytomography, and computed tomography (CT) scanning. Although prediction of the onset of myelopathy in any particular patient is difficult, studies of large populations of patients have sought to establish parameters for predicting neurologic involvement via imaging studies.[11, 18, 19]
Plain Radiography
The initial imaging assessment in suspected rheumatoid spondylitis should consist of plain radiographs of the cervical spine, including lateral flexion and extension views. Several measurements that can help direct management can be made on plain radiographs.
AADI measurement
Traditionally, the anterior atlantodental interval (AADI) has been used to monitor patients with rheumatoid arthritis over time. This measures the interval from the posterior margin of the anterior ring of C1 to the anterior surface of the odontoid. An interval of more than 3 mm in an adult or 4 mm in a child is considered abnormal. Various authors have recommended surgery for values of more than 8 mm, 9 mm, or 10 mm (see Surgical Management).
Although the AADI was used commonly to monitor patients with cervical involvement, a number of investigations have shown that the AADI does not reliably discriminate between patients who are neurologically intact from those with neural deficit.[20] This is due in part to the 3-dimensional changes that take place with progressive subluxation. As the deformity progresses, the anterior arch of the atlas displaces in an anteroinferior direction as superior migration of the odontoid (SMO) combines with atlantoaxial instability (AAI). With continued SMO, the AADI decreases, although this vertical translocation is associated with a more unfavorable prognosis.
Boden and associates demonstrated this pitfall by examining the sensitivity, specificity, accuracy, and positive and negative predictive values of the AADI in predicting paralysis based on varying critical intervals (see the table below).[21] For example, raising the cut-off value for the AADI from 8 mm to 10 mm increases the specificity from 58% to 90%. However, the sensitivity with such a change in threshold value decreases from 59% to 35%. More recently, the posterior atlantodental interval (PADI) has been recommended as a more reliable predictor of whether neurologic compromise will develop.
Table. Reliability of the Anterior (AADI) and Posterior (PADI) Atlantodental Intervals in Predicting Paralysis in Patients with Rheumatoid Arthritis (Open Table in a new window)
| Test | SENS, % | SPEC, % | ACC, % | PPV, % | NPV, % |
| AADI | |||||
| 8 mm or greater | 59 | 58 | 58 | 61 | 56 |
| 9 mm or greater | 41 | 77 | 58 | 67 | 55 |
| 10 mm or greater | 35 | 90 | 62 | 80 | 56 |
| 11 mm or greater | 18 | 97 | 55 | 86 | 52 |
| PADI | |||||
| 12 mm or less | 76 | 90 | 83 | 90 | 78 |
| 13 mm or less | 91 | 71 | 82 | 78 | 88 |
| 14 mm or less | 97 | 52 | 75 | 69 | 94 |
| Note that all values are expressed as percentages. These numbers were calculated from a series of 73 patients. ACC = accuracy; NPV = negative predictive value; PPV = positive predictive value; SENS = sensitivity; SPEC = specificity. (Reprinted with permission from Boden SD, Dodge LD, Bohlman HH, Rechtine GR. J Bone Joint Surg Am. Sep 1993;75(9):1282-97.[21] ) | |||||
PADI measurement
Anterior atlantoaxial subluxation may also be assessed by the PADI measurement, as measured from the posterior aspect of the odontoid to the anterior margin of the lamina of C1. Because the synovial pannus may occupy 1-3 mm of the retro-odontoid space, this interval does not represent the true space available for the cord.
The PADI was compared with the traditional anterior interval in a long-term series involving 73 patients.[21] Using a critical PADI of 14 mm or less resulted in a sensitivity (ability to detect those with paralysis) of 97%, a level superior to that using the AADI (see the table above). More importantly, the negative predictive value, using a critical PADI of 14 mm, rises to 94%. Therefore, if the PADI is greater than 14 mm, there is a 94% chance that the patient will not have paralysis. Such a high negative predictive value makes the PADI extremely reliable as a screening test.
SMO assessment
A variety of measurements have been used to assess SMO. All of these measurements attempt to identify and grade the degree of odontoid encroachment on space normally occupied by the spinal cord and brainstem. Unfortunately, many of these are difficult to reproduce. The image below depicts a few pertinent measurements.
Rheumatoid spondylitis. Pertinent measurements of superior migration of the odontoid; cranial migration distance (CMD).
The McGregor line has become the most consistent reference, because it connects the posterior margin of the hard palate to the most caudal point of the occiput. Vertical settling is defined here by migration of the odontoid by more than 4.5 mm above this line.
The Redlund-Johnell line assesses the occiput-to-C2 complex. The value measures the distance between the midpoint of the inferior margin of the body of the axis to the McGregor line. Values less than 34 mm in males and 29 mm in females are considered abnormal and correlate with increased risk of neurologic injury.[22]
The Ranawat index targets disease in the C1-C2 segment by utilizing a lateral radiograph. A line is drawn from the pedicles of C2 superiorly along the vertical axis of the odontoid until it intersects a line connecting the anterior and posterior arches of C1. A value less than 13 mm is diagnostic of vertical settling.
The McRae line connects the front of the foramen magnum to the back. The upper tip of the odontoid process should not project above this line and should normally be 1 cm below the anterior margin of the foramen magnum.
The Chamberlain line is drawn from the posterior margin of the hard palate to the posterior margin of the foramen magnum. Projection of the tip of the odontoid 6 mm above this line is considered pathologic. However, the margins of the foramen magnum are frequently difficult to delineate without a tomogram.
Subaxial vertebral subluxations
Plain radiographs are also useful in detecting subaxial vertebral subluxations. These subluxations may be quantitated on lateral cervical radiographs as translation forward in millimeters or as a percentage slip of the total anteroposterior diameter of the inferior vertebral body. Historically, focus was directed on the number of millimeters of listhesis or the percentage of vertebral slip. However, recent demonstrations show that the sagittal diameter of the subaxial canal correlates with the presence and degree of paralysis more often than does the percentage of vertebral slip. Patients with canal diameters of 13 mm or less are at higher risk for neurologic involvement.
The following image depicts a cervical radiograph from a patient with combined SMO and subaxial subluxation who underwent Occipitocervical fusion and lateral mass plating.
Rheumatoid spondylitis. Occipitocervical fusion combined with lateral mass plating for a patient with combined superior migration of the odontoid and subaxial subluxation. Courtesy of Steven R. Garfin.
Magnetic Resonance Imaging
Magnetic resonance imaging (MRI) has provided an increased ability to visualize the extent of spinal cord compression, particularly when due to pannus.[23] Dvorak and colleagues showed that two thirds of patients with atlantoaxial subluxation (AAS) have a pannus of greater than 3 mm in diameter.[24] Therefore, the bony canal diameter measured on plain radiographs may not represent the true space available for the cord. Kawaida et al demonstrated spinal cord compression in all patients with rheumatoid arthritis when the space available for the cord (as measured on MRI) was 13 mm or less.[25]
Using MRI, the cervicomedullary angle is an effective indicator of cord distortion from superior migration of the odontoid (SMO). This angle incorporates lines drawn along the anterior aspects of the cervical cord and along the medulla. The normal range is 135-175°. Angles less than 135° indicate basilar invagination and have been associated with myelopathy (see the image below for a patient example).
Rheumatoid spondylitis. MRI of a patient with superior migration of the odontoid and subaxial subluxation. Courtesy of Steven R. Garfin.
Polytomography and CT Scanning
Historically, tomograms were useful for quantitating the degree of basilar invagination and to measure the anterior (AADI) and posterior (PADI) atlantodental intervals more accurately in patients with abnormal radiographs. However, computed tomography (CT) scanning with sagittal and coronal reformatting has largely supplanted biplanar tomography. A CT scan combined with intrathecal contrast provides excellent bony detail and the ability to detect spinal cord compression from synovial pannus.
Although the noninvasive nature of magnetic resonance imaging (MRI) has made it the preferred modality for this type of evaluation, CT myelography is useful for patients with contraindications to MRI.
Источник

