Узи сердца ревматоидный артрит
Поражение сердца при ревматоидном артрите в последние годы привлекает к себе внимание исследователей. Долгое время считалось, что отсутствие поражения сердца при инфектартрите является дифференциально-диагностическим признаком по отношению к ревматизму.
Engleman (1955) обнаружил значительное поражение сердца (очаговый миокардит, перикардит, изменения клапанов и коронариит, наличие ревматоидных узелков в миокарде и сосудах) в 38 из 43 аутопсий. Vignon, Perkin, Duran (1962) из 12 случаев аутопсий в шести нашли поражение клапанов сердца, аорты, коронарных сосудов и перикарда. Cruickshank при аутопсиях 100 больных инфектартритом обнаружил васкулит сосудов сердца в 20 случаях. В обстоятельной работе Cathcart и Spodik исследование 15 секционных случаев инфектартрита показало наличие утолщений митрального и аортального клапанов с субэндокардиально расположенными ревматоидными узелками, наличие подострого и слипчивого перикардита с лимфоцитарной инфильтрацией и узелками в миокарде в 7 случаях. У остальных 8 умерших были найдены более или менее выраженные явления атерокардиосклероза.
По данным различных авторов, органическое изменение клапанов сердца при инфектартрите встречается в 15-35% всех секционных случаев. В связи с этим некоторые авторы считают, что при инфектартрите имеет место прежде всего поражение эндокарда – вальвулит, главным образом аортальных клапанов (Ravault и Vignon). Другие указывают на преимущественное поражение миокарда, чаще всего типа очагового миокардита.
Во многих случаях инфектартрита при аутопсиях обнаруживается поражение аорты с образованием аортального порока. При этом, согласно данным Clark, Kulka, Bauer (1957), происходят следующие изменения: очаговое разрушение эластической ткани в аортальном кольце и его расширение, рубцовое стягивание створок аортальных клапанов и их краевая кальцинация и изредка сужение устий коронарных артерий. По данным этих авторов, картина ревматоидного аортита имеет место в 2% всех случаев инфектартрита, главным образом у мужчин, страдающих спондилитом.
Однако следует подчеркнуть, что столь частое поражение сердца при ревматоидном артрите обнаруживается только на аутопсиях, клинически же оно диагностируется значительно реже, в среднем, по обобщенным данным различных авторов, у 5% больных инфектартритом.
Еще в 1956 г. А. И. Нестеров и М. Г. Астапенко отмечали, что у большинства больных инфектартритом клинически можно констатировать явления миокардиодистрофии, а в некоторых случаях признаки медленно развивающегося порока – недостаточности митрального клапана. Эти данные, были впоследствии подтверждены в работе И. Е. Сперанской (1959), которая, обследовав 326 больных, диагностировала миокардиодистрофию у 50%, недостаточность митрального клапана – у 40 больных и сочетанный митральный порок у восьми; при этом все больные были моложе 50 лет и лишь трое из них ранее перенесли ревматизм.
По данным Kottgen и Calleusse у 1/3 детей, страдающих ревматоидным артритом, клинически можно обнаружить поражение сердца.
В исследованиях Berger и Schenck (1961) у 45% детей были отмечены патологические изменения на электро- и фонокардиограмме. При этом у 56% детей были обнаружены и мезодиастолические шумы. У части детей было отмечено уменьшение систолического и минутного объема сердца и удлинение времени напряжения. Все эти данные, по мнению авторов, свидетельствуют о поражении миокарда и указывают на то, что поражение сердца при ревматоидном артрите у детей встречается значительно чаще, чем это предполагают.
М. Г. Астапенко, В. М. Чепой, В. А. Шанина и Г. П. Котельникова, исследовав 100 больных достоверным инфектартритом в возрасте от 10 до 46 лет, предъявляющих кардиальные жалобы, обнаружили у 14 из них симптомы текущего воспалительного процесса в сердце (миокардит и перикардит). Однако в последующие 3 года у этих больных сформировался порок сердца (недостаточность митрального клапана), что свидетельствует также и о поражении эндокарда у этих больных.
Портативный аппарат для неотложной помощи, интенсивной терапии и спортивной медицины.
Исследования опорно-двигательного аппарата, мониторинг проведения анестезии и др.
Ювенильный ревматоидный артрит (ЮРА) — одно из наиболее частых и инвалидизирующих ревматических заболеваний у детей [1, 2]. Заболеваемость ювенильным ревматоидным артритом составляет 2-16 случаев на 100 000 детского населения в возрасте до 16 лет. Распространенность ювенильного ревматоидного артрита в разных странах составляет 0,05-0,6%. Распространенность ювенильного ревматоидного артрита у детей до 18 лет на территории Российской Федерации — 62,3 на 100 000, первичная заболеваемость — 16,2 на 100 000. У подростков распространенность ювенильного ревматоидного артрита составляет 116,4 на 100 000 (у детей до 14 лет — 45,8 на 100 000), первичная заболеваемость — 28,3 на 100 000 (у детей до 14 лет — 12,6 на 100 000). Чаще ревматоидным артритом болеют девочки. Смертность составляет 0,5-1%.
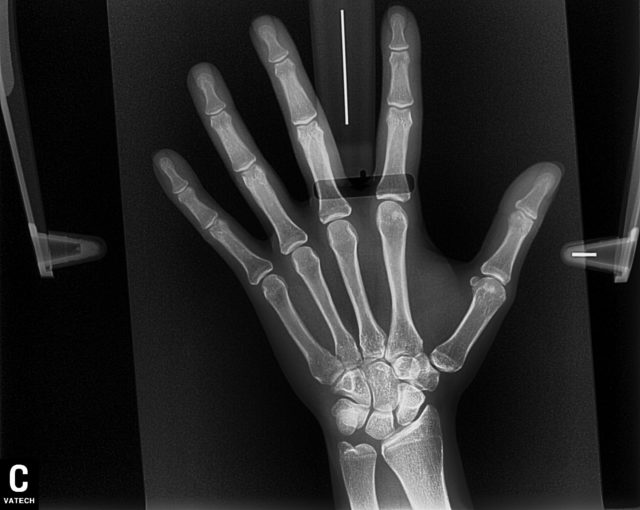
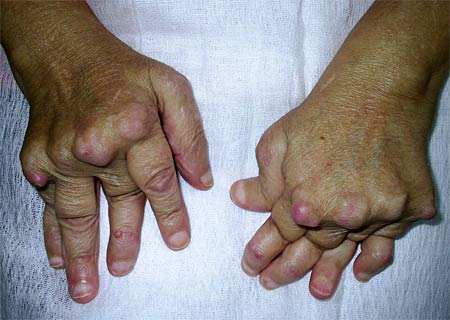
Ювенильного ревматоидный артрит — хроническое воспалительное заболевание суставов неизвестной этиологии и сложного патогенеза [3, 4]. Оно характеризуется неуклонно прогрессирующим течением, что приводит к инвалидизации. Среди множества проявлений ювенильного ревматоидного артрита одним из ведущих является суставной синдром, характеризующийся припухлостью, повышением местной кожной температуры над суставом, скованностью и болью в суставе. Патогенез связан с аутоиммунными нарушениями в первую очередь с ревматоидными факторами (антителами к иммуноглобулинам) и иммунокомплексными процессами, которые приводят к развитию синовита, а в ряде случаев и генерализованного васкулита. Деформацию суставов при ревматоидном артрите связывают с образованием и разрастанием в синовиальной оболочке грануляционной ткани, которая постепенно разрушает хрящ и субхондральные отделы костей с возникновением узур (эрозий), развитием склеротических изменений, фиброзного, а затем и костного анкилоза. Характерные подвывихи и контрактуры обусловлены отчасти и изменениями сухожилий, серозных сумок и капсулы сустава (рис.1). Как известно, лучевые методы диагностики представлены рентгенографическим исследованием, магнитно-резонансной томографией (МРТ), компьютерной томографией (КТ) и ультразвуковым исследованием (УЗИ). Рентгенография в большинстве случаев позволяет определить поражение суставов при вовлечении в патологический процесс только костных элементов, и зачастую эти изменения уже необратимы и трудны для лечения. Но, обладая рядом несомненных достоинств, традиционная рентгенография уже не может полностью удовлетворять потребности современной медицины в ранней диагностике заболеваний суставов в первую очередь в оценке воспалительных и дегенеративно-дистрофических изменений сухожильно- связочного аппарата и окружающих мягких тканей. Без всякого сомнения, МРТ является одним из самых эффективных методов исследования мягких тканей, костей и суставов, особенно их внутренних структур. Но высокая стоимость МРТ, трудность ее проведения у детей младшего возраста (в большинстве случаев детям до 3-х лет МР-исследования проводятся под наркозом) и относительно малое число МР-томографов не позволяют считать это обследование методом выбора при диагностике ревматоидного артрита. УЗИ позволяет оценить мягкие ткани сустава, хрящевую ткань и кортикальный слой костной ткани, а также связки, сухожилия, соединительнотканные элементы, жировую клетчатку, сосудисто-нервные пучки. Легкодоступность, быстрота и экономичность исследования позволяют данный метод использовать в диагностике ювенильного ревматоидного артрита на начальном этапе обследования пациента [5].
Рис. 1. Схематическое изображение сустава при ювенильном ревматоидном артрите.
Среди поражений суставов в 80% случаев коленный сустав поражается в первую очередь, в 40% — голеностопный сустав, в 20 % — плечевой сустав. На примере коленного сустава, как наиболее часто вовлекающегося в патологический процесс, мы выявили УЗ критерии поражения костной и хрящевой ткани, а также сухожильно-связочного аппарата.
Нами обследовано 25 детей с суставным синдромом в возрасте от 1 года до 16 лет, из них 20 девочек и 5 мальчиков. Всем пациентам проводили рентгенографическое исследование, МРТ и УЗИ суставов. Диагноз был поставлен по клиническим и лабораторным данным.
Ультразвуковое исследование коленных суставов проводилось по разработанной ранее методике, при этом оценивали структуру гиалинового хряща, наличие свободной жидкости в полости сустава, состояние кортикального слоя мыщелков большеберцовой и бедренной костей, а также сосудистую реакцию мягких тканей сустава с помощью методики УЗ-ангиографии.
В ходе проведенных исследований было установлено, что у 30% (8 детей исследуемой группы) рентгенографические исследования коленного сустава (КС) изменения не показали. Однако эхографическая картина того же сустава показала начальные изменения в виде умеренного неравномерного истончения гиалинового хряща и незначительного количества жидкости в области сустава. Кортикальный слой был представлен в виде неровных и размытых контуров, отмечалось утолщение кортикального слоя надколенника, что позволило сделать предположение о начальных проявлениях артрита, которые были позже подтверждены лабораторными исследованиями (рис. 2).
Друзья, ну оооочень много вопросов поступает о различных методах диагностики ревматических болезней. И правда, что выбрать из такого многообразия. УЗИ, рентген, МРТ, КТ… Постараюсь побольше уделять времени методам диагностики. А сегодня про УЗИ. Метод относительно (!) новый в практической ревматологии и вызывающий массу вопросов и споров относительно его целесообразности и ситуациях применения на практике.
Существуют рекомендации и алгоритмы практического применения ультразвука для диагностики и контроля за эффективностью терапии ревматоидного артрита (РА). Вот сегодня о них и поговорим, хочется чтобы вы сами разобрались в этом вопросе.
До 2016-2017 гг Европейская антиревматическая Лига (EULAR) хоть и поддерживала использование ультразвука, но не давала конкретных указаний относительно того, как и, главное, когда использовать ультразвук.
Экспертная комиссия EULAR предлагает 3 возможных области применения ультразвука.
- Уточнить, присутствует ли синовит у пациентов без клинических признаков воспаления.
- Контроль пациентов, которые вроде бы соответствуют критериям EULAR, но смущают врача.
- Контроль пациентов, которые не соответствуют критериям диагноза, но являются подозрительными в отношении РА.
А теперь комментарии…
Пациент А. имеет симптомы РА и/или положительные РФ/АЦЦП.
Шаг 1: определяем имеет ли он синовит (воспаление синовиальной оболочки и выпот в сустав) клинически (то есть определяемый при осмотре). Если ДА, выясняем соответствует ли он критериям диагноза РА. Если ДА, тогда выставляется диагноз РА, рекомендуется терапия.
❌Если НЕТ, то есть пациент НЕ соответствует критериям диагноза или мы клинически не видим у него синовита, тогда переходим к шагу 2.
✅Это УЗИ. Если на УЗИ выявлен синовит, то тогда все равно стоит рассмотреть вопрос о терапии с учётом факторов риска.
❌Если НЕТ — стоит искать другую болезнь.
Пациент Б, удовлетворяет критериям постановки диагноза РА.
Что же мы можем обнаружить на УЗИ и какой сделать вывод?
Ситуация 1: синовит обнаружен во многих суставах. Мы делаем вывод о наличии подтверждённого УЗИ РА.
❌Ситуация 2: синовит НЕ выявлен вообще. Исследование стоит повторить через 2-4 недели.
✅Ситуация 3: синовит выявлен, но незначительный и в единичных суставах. Эта находка диагноз РА не снимает, но тактику ведения стоит пересмотреть с учётом факторов риска.
Кроме того, эксперты делают вывод о том, что пациенты с РА, получающие стандартные базисные или биологические препараты должны пройти УЗИ на старте терапии и через 3-6 месяцев лечения для оценки ответа на лечение.
Источник
Одни и те же симптомы могут быть признаками разных заболеваний, а болезнь может протекать не по учебнику. Не пытайтесь лечиться сами — посоветуйтесь с врачом.
Лекарственная терапия включает применение трех групп препаратов:
Нестероидные противовоспалительные препараты
Представителями нестероидных противовоспалительных препаратов являются
Эти препараты имеют минимальный побочный эффект и сохраняют высокую противовоспалительную и обезболивающую активность.
Мелоксикам (мовалис) в начале лечения при активности воспалительного процесса назначают по 15 мг/сут., а в дальнейшем переходят на 7,5 мг/сут. в качестве поддерживающей терапии.
Нимесулид назначается в дозе 100 мг два раза в сутки.
Целекоксиб (целебрекс) назначается по 100–200 мг два раза в сутки.
Для пожилых людей подбор дозировки препарата не требуется. Однако у пациентов с массой тела ниже средней (50 кг) желательно начинать лечение с самой низкой рекомендованной дозы.
Следует избегать комбинации двух или более нестероидных противовоспалительных препаратов, поскольку их эффективность остается неизменной, а риск развития побочных эффектов возрастает.
Базисные препараты
Базисные препараты рекомендуется применять сразу после установления диагноза.
Основными лекарственными средствами базисной терапии ревматоидного артрита являются:
- метотрексат,
- сульфазалазин,
- D-пеницилламин,
- аминохинолиновые препараты,
- циклофосфан,
- азатиоприн,
- циклоспорин А (сандиммун),
- ремикейд (инфликсимаб),
- энбрел (этанерцепт),
- лефлуномид (арава) и другие.
Неэффективные на протяжении 1,5–3 месяцев базисные препараты должны быть заменены или использованы их комбинации с гормонами в малых дозах, что позволяет снизить активность ревматоидного артрита.
Шесть месяцев – критический срок, не позднее которого должна быть подобрана действенная базисная терапия.
В процессе лечения базисными препаратами тщательно мониторируют активность болезни и побочные эффекты.
Использование высоких доз гормонов (пульс-терапия) в комбинации с медленно действующими средствами позволяет повысить эффективность последних.
Глюкокортикостероиды (гормоны)
При высокой степени активности воспаления используют гормоны, причем в случаях системных проявлений ревматоидного артрита – в виде пульс-терапии (только гормоны или в сочетании с цитостатиком – циклофосфамидом), без системных проявлений – в виде курсового лечения.
Гормоны также применяют как поддерживающую противовоспалительную терапию при неэффективности других лекарственных средств.
В ряде случаев гормоны используются в качестве местной терапии. Препаратом выбора является дипроспан, оказывающий продленное действие.
Мази, кремы, гели на основе нестероидных противовоспалительных препаратов (ибупрофен, пироксикам, кетопрофен, диклофенак) используют в виде аппликаций на воспаленные суставы.
Для усиления противовоспалительного эффекта аппликации вышеназванных мазевых форм препаратов сочетают с аппликациями раствора диметилсульфоксида в разведении 1:2–1:4.
Дополнительная терапия
При отсутствии ответа на стандартное лекарственное лечение у больных с высокой активностью ревматоидного артрита применяют плазмаферез, лимфоцитаферез.
Важным моментом в лечении ревматоидного артрита является профилактика остеопороза – восстановление нарушенного кальциевого баланса в направлении повышения всасывания его в кишечнике и уменьшения выведения из организма.
Для этого применяется диета с повышенным содержанием кальция.
Источниками кальция являются молочные продукты (особенно твердые сорта сыра, а также плавленый сыр; в меньшей степени творог, молоко, сметана), миндаль, лесные и грецкие орехи и пр., а также препараты кальция в сочетании с витамином D или его активными метаболитами.
Препаратом, который можно отнести к базисным антиостеопоретическим средствам, является миакальцик. Он выпускается для внутримышечного введения по 100 ME и в виде назального спрея; назначается по схеме совместно с препаратами кальция (кальцитонин) и производными витамина D.
При лечении ревматоидного артрита используется также лазерная терапия. Особенно при тяжелых обострениях ревматоидного артрита в последние годы широко используются внекорпоральные методы лечения (в первую очередь гемосорбция и плазмаферез).
Лазеротерапия особенно показана на ранней стадии процесса. Курс не более 15 процедур.
С целью уменьшения боли и устранения спазма околосуставных тканей применяется криотерапия (лечение холодом), на курс 10–20 процедур.
С целью воздействия на аллергические процессы, улучшения питания тканей и устранения воспаления применяют и другие физические методы лечения.
В ранней стадии ревматоидного артрита рекомендуется ультрафиолетовое облучение пораженных суставов, электрофорез диметилсульфоксида, кальция, салицилатов.
При появлении более стойких изменений в суставах и при отсутствии признаков высокой активности назначают фонофорез гидрокортизона, магнитотерапию, импульсные токи.
Лечебная физкультура и массаж назначаются всем больным с целью снятия мышечного спазма, быстрейшего восстановления функции суставов.
Все больные ревматоидным артритом должны систематически наблюдаться и обследоваться ревматологом.
Больные с медленно прогрессирующим течением без поражения внутренних органов должны появляться у ревматолога 1 раз в 3 месяца. При наличии поражения внутренних органов больные осматриваются ревматологом 1 раз в 2–4 недели.
Курортное лечение больных ревматоидным артритом рекомендуется осуществлять ежегодно вне фазы обострения.
При доброкачественном течении процесса без выраженных изменений суставов показано применение радиоактивных ванн в Цхалтубо и Белокурихе; при типичном прогрессирующем процессе – лечение сероводородными ваннами в Сочи, Серноводске, Пятигорске, Кемери; при выраженных деформациях и контрактурах – лечение грязевыми аппликациями в Евпатории, Саках, Пятигорске, Одессе.
Источник
УЗИ сканер HS70
Точная и уверенная диагностика. Многофункциональная ультразвуковая система для проведения исследований с экспертной диагностической точностью.
Ювенильный ревматоидный артрит (ЮРА) — одно из наиболее частых и инвалидизирующих ревматических заболеваний у детей [1, 2]. Заболеваемость ювенильным ревматоидным артритом составляет 2-16 случаев на 100 000 детского населения в возрасте до 16 лет. Распространенность ювенильного ревматоидного артрита в разных странах составляет 0,05-0,6%. Распространенность ювенильного ревматоидного артрита у детей до 18 лет на территории Российской Федерации — 62,3 на 100 000, первичная заболеваемость — 16,2 на 100 000. У подростков распространенность ювенильного ревматоидного артрита составляет 116,4 на 100 000 (у детей до 14 лет — 45,8 на 100 000), первичная заболеваемость — 28,3 на 100 000 (у детей до 14 лет — 12,6 на 100 000). Чаще ревматоидным артритом болеют девочки. Смертность составляет 0,5-1%.
Ювенильного ревматоидный артрит — хроническое воспалительное заболевание суставов неизвестной этиологии и сложного патогенеза [3, 4]. Оно характеризуется неуклонно прогрессирующим течением, что приводит к инвалидизации. Среди множества проявлений ювенильного ревматоидного артрита одним из ведущих является суставной синдром, характеризующийся припухлостью, повышением местной кожной температуры над суставом, скованностью и болью в суставе. Патогенез связан с аутоиммунными нарушениями в первую очередь с ревматоидными факторами (антителами к иммуноглобулинам) и иммунокомплексными процессами, которые приводят к развитию синовита, а в ряде случаев и генерализованного васкулита. Деформацию суставов при ревматоидном артрите связывают с образованием и разрастанием в синовиальной оболочке грануляционной ткани, которая постепенно разрушает хрящ и субхондральные отделы костей с возникновением узур (эрозий), развитием склеротических изменений, фиброзного, а затем и костного анкилоза. Характерные подвывихи и контрактуры обусловлены отчасти и изменениями сухожилий, серозных сумок и капсулы сустава (рис.1). Как известно, лучевые методы диагностики представлены рентгенографическим исследованием, магнитно-резонансной томографией (МРТ), компьютерной томографией (КТ) и ультразвуковым исследованием (УЗИ). Рентгенография в большинстве случаев позволяет определить поражение суставов при вовлечении в патологический процесс только костных элементов, и зачастую эти изменения уже необратимы и трудны для лечения. Но, обладая рядом несомненных достоинств, традиционная рентгенография уже не может полностью удовлетворять потребности современной медицины в ранней диагностике заболеваний суставов в первую очередь в оценке воспалительных и дегенеративно-дистрофических изменений сухожильно- связочного аппарата и окружающих мягких тканей. Без всякого сомнения, МРТ является одним из самых эффективных методов исследования мягких тканей, костей и суставов, особенно их внутренних структур. Но высокая стоимость МРТ, трудность ее проведения у детей младшего возраста (в большинстве случаев детям до 3-х лет МР-исследования проводятся под наркозом) и относительно малое число МР-томографов не позволяют считать это обследование методом выбора при диагностике ревматоидного артрита. УЗИ позволяет оценить мягкие ткани сустава, хрящевую ткань и кортикальный слой костной ткани, а также связки, сухожилия, соединительнотканные элементы, жировую клетчатку, сосудисто-нервные пучки. Легкодоступность, быстрота и экономичность исследования позволяют данный метод использовать в диагностике ювенильного ревматоидного артрита на начальном этапе обследования пациента [5].
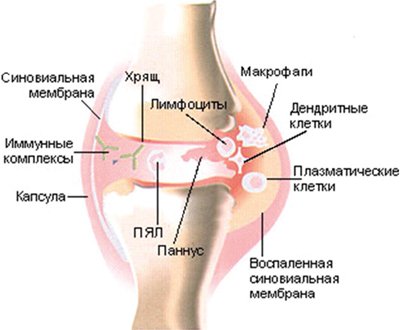
Рис. 1. Схематическое изображение сустава при ювенильном ревматоидном артрите.
Среди поражений суставов в 80% случаев коленный сустав поражается в первую очередь, в 40% — голеностопный сустав, в 20 % — плечевой сустав. На примере коленного сустава, как наиболее часто вовлекающегося в патологический процесс, мы выявили УЗ критерии поражения костной и хрящевой ткани, а также сухожильно-связочного аппарата.
Нами обследовано 25 детей с суставным синдромом в возрасте от 1 года до 16 лет, из них 20 девочек и 5 мальчиков. Всем пациентам проводили рентгенографическое исследование, МРТ и УЗИ суставов. Диагноз был поставлен по клиническим и лабораторным данным.
Ультразвуковое исследование коленных суставов проводилось по разработанной ранее методике, при этом оценивали структуру гиалинового хряща, наличие свободной жидкости в полости сустава, состояние кортикального слоя мыщелков большеберцовой и бедренной костей, а также сосудистую реакцию мягких тканей сустава с помощью методики УЗ-ангиографии.
В ходе проведенных исследований было установлено, что у 30% (8 детей исследуемой группы) рентгенографические исследования коленного сустава (КС) изменения не показали. Однако эхографическая картина того же сустава показала начальные изменения в виде умеренного неравномерного истончения гиалинового хряща и незначительного количества жидкости в области сустава. Кортикальный слой был представлен в виде неровных и размытых контуров, отмечалось утолщение кортикального слоя надколенника, что позволило сделать предположение о начальных проявлениях артрита, которые были позже подтверждены лабораторными исследованиями (рис. 2).
Рис. 2. Эхограммы коленного сустава.
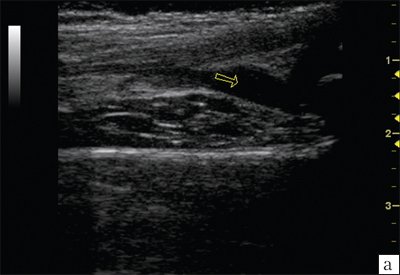
а) Синовит в полости сустава.
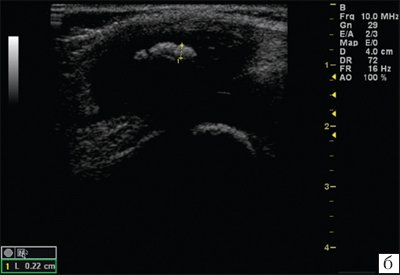
б) При начальных проявлениях ювенильного ревматоидного артрита.
У 70% (17 детей исследуемой группы) при эхографии визуализировалось наличие свободной жидкости в полости коленного сустава и изменения хрящевой и костной ткани. Кортикальный слой костей, образующих сустав, выглядел в виде прерывистой гиперэхогенной линейной структуры с формированием так называемых «эрозивных» участков. Хрящевая ткань имела вид «древообразных разрастаний» (рис. 3). При УЗ-ангиографии отмечалась гиперваскуляризация. Эти дегенеративные изменения хрящевой и костной ткани соответствовали наличию ювенильного ревматоидного артрита II-III стадии развития, что и подтверждалось данными рентгенологического исследования и МРТ.
Рис. 3. Эхограммы коленного сустава при ювенильном ревматоидном артрите II-III стадии.
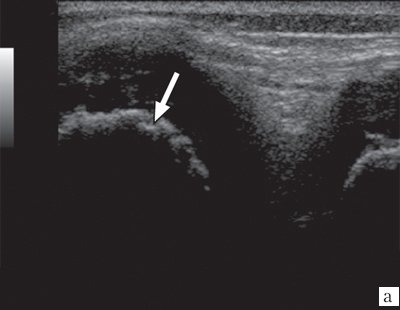
а) Кортикальный слой с формированием «псевдоэрозий».
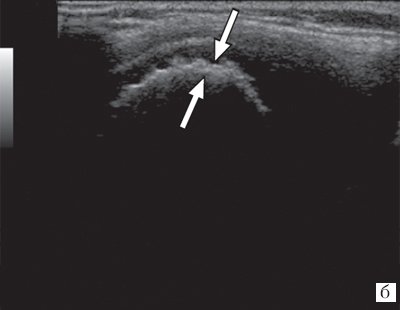
б) «Псевдоутолщение» кортикального слоя.
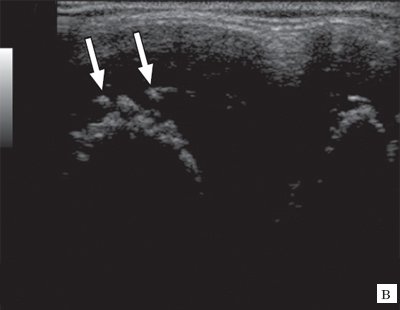
в) Хрящевая ткань в виде «древообразных разрастаний».
Таким образом, ультразвуковое исследование является высокоинформативным, легкодоступным и экономичным методом исследования, который можно использовать в ранней диагностике ювенильного ревматоидного артрита у детей.
Литература
- Алексеева Е.И. Ювенильный ревматоидный артрит // Педиатрия. М.: Издательская группа «ГЭОТАР-Медиа». 2005.
- Мерта Дж. Артралгия и артриты // Consiliummedicum. 1999. Т. 1 N5.
- Petty R.E., Southwood T.R., Baum J. et al. Revision of proposed classification criteria for juvenile idiopathic arthritis. J. Rheumatol 2001.
- Алексеева Е.И., Шахбазян И.Е. Принципы патогенетической терапии тяжелых системных вариантов венильного ревматоидного артрита. Аутоиммунные болезни. М.: 2002.
- Алешкевич А.И., Малевич Э.Е. Рентгенологическая и ультразвуковая диагностика дегенеративно-дистрофических поражений коленного сустава. Материалы научно-практической конференции «Новые технологии в медицине: диагностика, лечение, реабилитация». Минск, 21-22 ноября 2002 г.

УЗИ сканер HS70
Точная и уверенная диагностика. Многофункциональная ультразвуковая система для проведения исследований с экспертной диагностической точностью.
Источник