Визуальная ревматология ревматоидный артрит
Содержание:
«В движении жизнь» – это выражение, вероятно, слышали все. Действительно, для осуществления нормальной жизнедеятельности человеку приходится постоянно перемещать свое тело в пространстве. В ходе эволюции организм обзавелся прекрасными элементами, которые обеспечивают данную функцию на высшем уровне. Эти удивительные части тела – суставы. Все кости человека удивительно прочны и упруги по отдельности, что позволяет им выдерживать колоссальные нагрузки. Соединяясь же воедино, они формируют удивительно подвижный скелет, который позволяет выполнять невероятные движения. Все это достигается благодаря слаженной работе массы суставов.
К сожалению, есть заболевания, в результате прогрессирования которых суставы организма поражаются и теряют свою подвижность. В результате у пациента значительно снижается качество жизни. Ревматоидный артрит – очень актуальная проблема современной ревматологии. Это системное заболевание, поражающее соединительную ткань. В результате его развития у пациента поражаются мелкие суставы по эрозивно-деструктивному типу. Во всем мире от данного заболевания страдает около 60 миллионов пациентов, что составляет до 1% от всей популяции.
Еще более усугубляет всю ситуацию то, что врачи не смогли до настоящего времени определить точную причину развития заболевания. Есть отдельные теории и предположения, но ни одна из них не нашла действительно весомого подтверждения. С течением времени же все симптомы болезни неуклонно усугубляются, постепенно приводя к стойкой утрате нетрудоспособности человеком. Примерно в три раза чаще заболевают женщины. Средний возраст пациента при выявлении заболевания – 30-35 лет.
Причины ревматоидного артрита
В настоящее время есть несколько наиболее вероятных этиологических факторов болезни. Каждая версия имеет свои преимущества и недостатки. В целом же все больше медиков склоняются к тому, что ревматоидный артрит – полифакторное заболевание, которое развивается при комбинировании сразу нескольких причин.
— Генетическая предрасположенность – у пациентов с данным диагнозом установлена предрасположенность к нарушениям активности иммунной системы на генетическом уровне. Уже обнаружены некоторые антигены, наличие которых может приводить к изменению гуморального и клеточного иммунитета вследствие воздействия некоторых инфекций. Также можно проследить повышенную вероятность развития ревматоидного артрита у людей, ближайшие родственники которых также болели ним.
— Инфекционные агенты, способные в результате своих специфических свойств вызывать изменения в иммунитете человека, в результате чего собственные защитные факторы атакуют свою соединительную ткань. На роль этих возбудителей выдвигаются: вирус Эбштейн-Бара, ретровирусы, возбудители краснухи, герпеса, цитомегаловирус, микоплазмы. У врачей есть некоторые доказательства в пользу этой гипотезы:
- У 80% пациентов выявляются повышенные титры антител к вирусу Эбштейн-Бара.
- В лимфоцитах больных ревматоидным артритом Эбштейн-Бара выявляется намного чаще, чем у здоровых людей.
Выше были указаны факторы, которые создают предпосылки для развития заболевания. Выделяют также пусковые факторы, которые провоцируют его проявление у конкретного пациента в определенное время.
- Переохлаждение.
- Повышенное воздействие солнечного света (гиперинсоляция).
- Интоксикация, в том числе и токсинами микроорганизмов.
- Бактериальная инфекция.
- Прием некоторых лекарственных препаратов.
- Нарушение функции эндокринных желез.
- Эмоциональное перенапряжение и стрессы.
Что интересно, кормление грудью на протяжении двух лет и более снижает вероятность развития ревматоидного артрита в два раза.
Механизм развития ревматоидного артрита
Установлено, что при воздействии одного или комбинации провоцирующих факторов в организме пациента запускает неверная иммунная реакция. Собственные клетки вырабатывают вещества, которые вызывают повреждение синовиальной оболочки суставов. Сначала развивается синовиит, который впоследствии переходит в пролиферативную стадию и вызывает повреждение самого хряща и костей.
Также иммунитет вырабатывает патологические цитокины, которые обладают рядом отрицательных свойств:
- провоцируют выработку в повышенном количестве провоспалительных факторов, способствующих дальнейшему прогрессированию заболевания;
- активирую некоторые ферменты, которые способны разрушать хрящ, покрывающий сустав и обеспечивающий эластичное скольжение поверхностей;
- поставляют на мембраны тучных слеток специальные молекулы, которые заставляют эти лейкоциты проявлять аутоиммунное действие;
- привлекают в став дополнительные иммунокомпетентные клетки, которые также отрицательно сказываются на течении заболевания в данном случае;
- усиление ангиогенеза, что позволяет сосудам прорастать в хрящ и облегчает для агрессивных факторов попадание вглубь хрящевой ткани.
Классификация ревматоидного артрита
Есть несколько критериев, по которым классифицируется данное заболевание.
Клинико-анатомические формы
- Ревматоидный артрит (олигоартрит, моноартрит, полиартрит) – форма заболевания, при котором происходит поражение исключительно суставов, а другие органы нормально функционируют без нарушения функции.
- Ревматоидный артрит с системными проявлениями – дополнительно аутоиммунные процессы затрагивают серозные оболочки организма (перикард сердца, плевру), легкие, кровеносные сосуды, почки, нервную систему, вызывает отложение во внутренних органах патологического белка – амилоида.
- Ревматоидный артрит, сочетающийся с деформирующим остеоартрозом, ревматизмом.
- Ювенильный ревматоидный артрит.
Характеристика с точки зрения иммунологии
В зависимости от того, выявляется ли ревматоидный фактор в крови пациента, все случаи заболевания делят на серопозитивные и серонегативные. Это имеет большое значение для врачей во время диагностики и планирования предстоящего лечения.
Течение заболевани
- Медленно прогрессирующее – заболевание на протяжении многих лет медленно переходит на другие суставы, больные сочленения не сильно повреждаются.
- Быстро прогрессирующее – болезнь очень часто обостряется, постепенно вовлекая все больше суставов. Суставные поверхности претерпевают значительные изменения в худшую сторону. Лечение не дает большого эффекта.
- Без заметного прогрессирования – наиболее благоприятная форма. С которой пациент может прожить всю жизнь, сохранив достаточно высокое качество жизни.
Рентгенологическая стадия заболевания
- Околосуставной остеопороз – уменьшение плотности костной ткани за счет снижения содержания в ней кальциевых солей.
- Остеопороз, дополняющийся незначительным снижением суставной щели.
- Сужение суставной щели и остеопороз дополняются множественными узурами.
- Ко всему указанному выше присоединяются костные анкилозы – главная и самая стойкая причина снижения подвижности вплоть до полного ее отсутствия.
Узуры – это глубокие эрозии на суставной поверхности хрящей.
Степень функциональной недостаточности опорно-двигательного аппарата
- 0 – пациент может совершать все движения в полном объеме.
- 1 – человек не может в полной мере выполнять все движения, которые обеспечивают ему возможность выполнять свои профессиональные обязанности.
- 2 – пациент не может трудиться за счет утраты профессиональной трудоспособности.
- 3 – человек не может самостоятельно себя обслуживать в полной мере.
Симптомы ревматоидного артрита
На начальных этапах заболевание протекает без яркой клинической картины. Пациент может годами и не подозревать о том, что у него ревматоидный артрит. Ведущим клиническим проявлением болезни является суставной синдром.
- Утренняя скованность – специфическое проявление заболевания, на котором пациент не заостряет внимания. Во время сна синовиальные оболочки суставов несколько воспаляются за счет снижения секреции глюкокортикоидов в ночное время. Иногда пациенты просто не могут, нормально снять с себя одеяло. Спустя примерно час все симптомы проходят, и человек может активно двигаться.
- Периодические боли в суставах, снижение аппетита, усталость, похудание – все это можно отметить в продромальном периоде.
- Острые боли в суставах, лихорадка – вот так у пациента начинается болезнь. Чаще всего поражаются суставы кистей и стоп, запястья, коленные и локтевые. Другие сочленения поражаются реже. Около сустава отмечается отек, а поверхность кожных покровов имеет более высокую температуру, чем на остальном теле. Также область сустава гиперемирована за счет протекания воспалительных процессов.
- При пальпации суставы болезненны, движение в них ограничено. По мере прогрессирования болезни пролиферативные процессы начинают преобладать, и может происходить значительное ограничение подвижности, деформация и подвывих суставов.
- Ревматоидные узелки – специфическое проявление заболевания, при котором на разгибательной поверхности сустава можно пальпировать плотные подкожные образования. Этот признак является одним из важных диагностических критериев ревматоидного артрита.
Также у пациента могут поражаться практически все органы в теле, в зависимости от степени активности процесса, но это отмечается относительно редко.
Диагностика ревматоидного артрита
Лабораторные исследования
- Общий анализ крови – выявляют анемию, увеличение скорости оседания эритроцитов, увеличение количества лейкоцитов.
- Биохимическое исследование крови – позволяет определить степень активности воспалительного процесса.
- Иммунологическое исследование крови – может определяться ревматоидный фактор, иногда обнаруживаются иммунные комплексы.
Инструментальная диагностика
- Рентгенологическое исследование суставов – в классификации описаны все критерии, которыми руководствуются врачи при выставлении рентгенологической стадии заболевания.
- Радиоизотопное исследование – вводимый элемент активно накапливается в пораженных суставах, а нормальная синовиальная ткань привлекает не так много атомов.
- Пункция сустава и исследование синовиальной жидкости.
- В самых тяжелых случаях – биопсия участка синовиальной оболочки.
Ревматоидный артрит: лечение
Системное лечение данного заболевания предусматривает использование следующих основных групп препаратов:
- нестероидные противовоспалительные вещества;
- базисные препараты;
- гормональные вещества (глюкокортикоиды);
- биологические агенты.
Нестероидные противовоспалительные вещества
Эти лекарства уже относительно давно хорошо себя зарекомендовали в лечении ревматоидного артрита и до сих пор являются лечебными средствами первой линии. Они позволяют относительно быстро купировать острые проявления заболевания и иногда добиться наступления стойкой ремиссии – состояния, при котором симптомы болезни отсутствуют, и пациент может жить полноценной жизнью.
Если пациент попадает к ревматологу в острый период заболевания, то одними только нестероидными противовоспалительными препаратами не обходятся – дополняют их высокими дозами глюкокортикоидов. Этот способ лечения называется пульс-терапией.
Эффект достигается за счет блокирования циклооксигеназы – фермента, благодаря которому в норме арахидоновая кислота распадается с образованием простагландинов и прочих биологически активных веществ, играющих важное значение в развитии воспалительной реакции.
Более старые препараты инактивируют циклооксигеназу-1, за счет чего при передозировке может происходить нарушение функции почек, печени, развиваться энцефалопатия. Современные препараты, используемые для лечения ревматоидного артрита, имеют большую селективность и не так опасны, поэтому пациентам нечего опасаться.
Врачи избегают комбинирования нестероидных противовоспалительных препаратов друг с другом, поскольку в таком случае значительно повышается вероятность развития у пациента побочных реакций, а вот лечебный эффект остается практически неизменным.
Базисные препараты для лечения ревматоидного артрита
Наиболее популярными и эффективными лекарствами для лечения ревматоидного артрита в настоящее время являются: препараты золота, метотрексат, лефлуномид, пеницилламин, сульфасалазин.
Есть также средства резерва: циклофосфан, азатиоприн, циклоспорин – они используются тогда, когда основные препараты не дали желаемого эффекта.
Еще относительно недавно врачи предпочитали постепенно наращивать дозу препарата, получаемую пациентом (принцип пирамиды). В настоящее время доказано, что при начале лечения с использованием высоких доз можно добиться более впечатляющих результатов за счет изменения характера течения заболевания. Только что обнаруженный ревматоидный артрит характеризуется практически полным отсутствием изменений в суставах пациента и высокой вероятностью наступления длительной ремиссии.
Если на протяжении первых месяцев заболевания лечение базисными препаратами не приносит желаемого эффекта, то врачи комбинируют их с глюкокортикоидами. Гормональные препараты снижают активность воспалительного процесса и позволяют подобрать эффективную базисную терапию. Считается, что врачи должны подобрать эффективное лечение ревматоидного артрита препаратами данной группы за полгода.
В процессе лечения пациент должен периодически проходить медицинский осмотр на предмет наличия побочных эффектов от приема препаратов и оценки степени активность самого заболевания.
Глюкокортикоиды
Данная группа препаратов может использоваться по-разному.
- В виде пульс-терапии – прием пациентом высоких доз препарата в сочетании с веществами базисной терапии заболевания. Это позволяет очень быстро снизить активность процесса и убрать воспалительные явления. При этом курс приема препарата не может быть длительным ввиду высокой вероятности развития побочных эффектов.
- В виде курсового лечения с целью угнетения воспалительной реакции при неэффективности других веществ. В данном случае доза значительно отличается в меньшую сторону, а медики стараются подобрать ее таким образом, чтобы пациент принимал минимум гормона, который при этом окажет необходимое действие.
- Локальная терапия – в составе мазей, которыми смазывают пораженные суставы. Показанием в большинстве случаев является олигоартрит или моноартрит крупных суставов. Также использоваться они могут при наличии противопоказаний к системному лечению гормонами и значительным преобладанием местных симптомов над общими.
- Внутрисуставное введение геля, содержащего в своем составе гормональные препараты. Это позволяет на относительно длительное (до месяца) время обеспечить непрерывное воздействие препарата на поврежденную суставную поверхность.
Биологические средства
Моноклональные антитела к некоторым цитокинам обеспечивают нейтрализацию фактора некроза опухолей, который в случае ревматоидного артрита провоцирует поражение собственных тканей.
Также есть исследования, предлагающие использовать в качестве лечения ревматоидного артрита регуляторы дифференцировки лимфоцитов. Это позволит избежать повреждения синовиальных оболочек Т-лимфоцитами, которые неверно «направляются» в суставы иммунитетом.
Другие лечебные мероприятия
- Физиотерапевтические процедуры.
- Профилактика остеопороза.
- Лечебная гимнастика в период ремиссии.
- Хирургическая коррекция патологии суставов.
Источник
Статья посвящена ревматоидный артриту — клиническим ситуацииям и алгоритмам лечения

Ревматоидный артрит (РА) – хроническое системное иммуновоспалительное заболевание неизвестной этиологии, сопровождающееся развитием симметричного прогрессирующего эрозивно-деструктивного полиартрита и внесуставными проявлениями [1]. РА ассоциирован с высоким риском кардиоваскулярных событий, остеопоротических переломов, ранней инвалидизацией и преждевременной смертностью пациентов. Улучшить прогноз и исходы болезни способны только своевременная диагностика и раннее активное лечение больных РА.
Течение болезни складывается из нескольких последовательных стадий: ранней, развернутой и поздней, каждая из них имеет свои клинические особенности и подходы к терапии.
Базовые принципы терапии РА («Treat to target» или «Лечение до достижения цели») [2, 3]:
1. Достижение ремиссии (DAS28 (суммарный индекс (включает упрощенный счет из 28 суставов), позволяет многократно оценивать активность РА и может быть использован для контроля его активности в повседневной практике) <2,6) или как минимум низкой активности заболевания (DAS28 <3,2).
2. Ранняя активная терапия базисными противовоспалительными препаратами (БПВП), в первую очередь метотрексатом (МТ), не позднее первых 3 мес. от начала болезни.
3. Лечение должно быть максимально активным, с быстрой эскалацией дозы МТ и последующим изменением (при необходимости) схемы лечения в течение 3 мес. до достижения ремиссии (или низкой активности) болезни.
4. Тщательный контроль изменений активности заболевания и коррекция терапии не реже 1 раза в 3 мес. или ежемесячно у больных с высокой и умеренной активностью РА.
5. В случае недостаточной эффективности стандартной терапии БПВП показано назначение генно-инженерных биологических препаратов (ГИБП).
6. Определение тактики терапии должно быть согласовано с пациентом.
К факторам неблагоприятного прогноза (ФНП) у больных РА относятся [4]:
– молодой возраст;
– женский пол;
– высокие титры ревматоидного фактора (РФ) и/или антитела к циклическому цитруллиновому пептиду (АЦЦП);
– эрозивный процесс в суставах по данным рентгенографического исследования или магнитно-резонансной томографии (МРТ);
– повышение уровней острофазовых показателей: скорости оседания эритроцитов (СОЭ) или С-реактивного белка (СРБ);
– высокая активность заболевания согласно индексам DAS28, SDAI (Simplified Disease Activity Index) или CDAI (Clinical Disease Activity Index);
– внесуставные проявления (синдром Шегрена, поражение легких и т. д.).
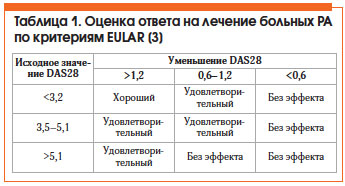
Оценка эффективности лечения РА по критериям Европейской антиревматической лиги (EULAR) представлена в таблице 1. Общепризнанным методом оценки активности РА является расчет индекса DAS28, который можно автоматически произвести на сайте www.das-score.nl.
Критерии эффективности терапии РА [5]:
• хороший клинический ответ (≈ ACR 70) (критерии Американской коллегии ревматологов);
• низкая активность болезни (DAS28 ≤ 3,2) или ремиссия (DAS28 ≤ 2,6);
• улучшение функции (HAQ (Health Assessment Questionare, опросник состояния здоровья, позволяющий оценить функциональные способности больных РА) <1,5) и качества жизни;
• предотвращение прогрессирования деструкции:
– замедление нарастания рентгенологических индексов (Sharp, Larsen);
– отсутствие появления новых эрозий;
– стабилизация или улучшение состояния по данным МРТ.
У пациентов, находящихся в состоянии ремиссии более 1 года после отмены глюкокортикостероидов (ГКС), следует рассмотреть вопрос о возможности прекращения лечения ГИБП, особенно если они применялись в комбинации с БПВП. Важное значение при определении тактики лечения имеет выбор пациентов.
Рассмотрим отдельные клинические ситуации и подходы к терапии при РА.
I. Пациент с впервые установленным ранним РА
Ранняя стадия РА – условно выделенная, клинико-патогенетическая стадия заболевания с длительностью активного синовита до 1 года, характеризуется преобладанием экссудативных изменений в пораженных суставах, частым атипичным течением и хорошим ответом на лечение. Выделение понятия «ранний РА» связано со сложившимися представлениями о патогенезе болезни и необходимости проведения ранней активной терапии РА. Ранний РА может дебютировать как недифференцированный артрит, что требует динамического наблюдения за больными и проведения тщательного дифференциально-диагностического поиска. На ранней стадии РА наиболее информативными являются диагностические критерии Американского и Европейского ревматологических сообществ, предложенные в 2010 г. (табл. 2).

Диагноз РА может быть установлен при общем счете не менее 6 баллов.
Доказано, что адекватная базисная терапия на ранней стадии РА позволяет предотвратить структурные повреждения, что способствует сохранению функциональной активности пациентов и улучшает отдаленный прогноз. БПВП необходимо назначать не позднее 3 мес. от начала РА с быстрой эскалацией дозы для достижения оптимального эффекта (DAS <2,4) и последующей заменой препарата в течение 3–6 мес. при его неэффективности [1]. Терапию БПВП следует продолжать даже при снижении активности заболевания и достижении ремиссии.
К БПВП первого ряда отнесены МТ, лефлуномид (ЛФ) и сульфасалазин (СС) (табл. 3), т. к. доказана их эффективность в отношении предотвращения деструктивных изменений суставов (уровень доказательности А). Препараты «второй линии» (гидроксихлорохин, препараты золота и др.) применяются при неэффективности препаратов первого ряда либо в комбинации с ними.
МТ – «золотой стандарт» терапии активного РА. При необходимости назначения МТ в дозе > 15 мг/нед. рекомендуется использовать парентеральный путь введения (в/м или п/к). Также с целью минимизации побочных явлений необходимо назначение фолиевой кислоты 1 мг/cут (5 мг/нед.), исключая дни приема МТ.

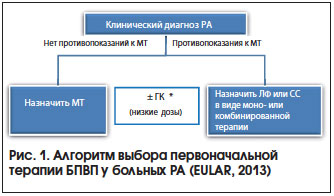
Основные стратегии лечения раннего РА (рис. 1) [7]:
1. Монотерапия МТ c последующей заменой на другие БПВП (ЛФ, СС) через 3–6 мес. в случае неэффективности или плохой переносимости).
2. Комбинированная базисная терапия, в т. ч. в сочетании с высокой дозой ГК. Используются комбинации БПВП как первого ряда (МТ + СС или МТ + ЛФ), так и второго ряда (МТ + Плаквенил) и т. д.
3. Комбинированная терапия синтетическими БПВП + ГИБП (в первую очередь ингибиторы фактора некроза опухоли (ФНО) при сохраняющейся > 3–6 мес. высокой активности РА, а также при наличии ФНП. Например, МТ 25 мг/нед. + Инфликсимаб 3 мг/кг массы тела.
II. Пациент с развернутым РА, не отвечающий на традиционные БПВП
Развернутая стадия РА – заболевание с отчетливо выраженной симптоматикой и длительностью болезни более 1 года. Суставной синдром имеет стойкий, симметричный и полиартикулярный характер с преимущественным поражением суставов кистей и стоп, выявляются признаки высокой или умеренной лабораторной активности, серопозитивность по РФ, эрозивный процесс в суставах по данным рентгенографии. Если диагноз устанавливается впервые, то стратегия ведения больного та же, что и при раннем РА. В случае уже проводившегося лечения с недостаточным эффектом или непереносимостью синтетических БПВП (как в виде монотерапии, так и при комбинированном их использовании), а также наличием ФНП прибегают к назначению ГИБП (рис. 2). Использование ГИБП позволяет максимально избирательно воздействовать на отдельные звенья иммунопатогенеза РА и существенно улучшить состояние больных РА, резистентных к стандартным БПВП и ГК [8]. Установлено, что комбинация традиционных БПВП с ГИБП более эффективна, чем монотерапия.
Назначение ГИБП показано:
– при длительно сохраняющейся (> 3–6 мес.) высокой активности РА;
– при высокой активности заболевания < 3 мес., только при наличии у больных ФНП.
Препаратами первого ряда среди ГИБП являются ингибиторы ФНО-α. Другие ГИБП назначаются больным РА с неадекватным ответом на блокаторы ФНО-α или при невозможности их применения (табл. 4).

Противопоказания к назначению ГИБП: отсутствие лечения одним или более БПВП (в первую очередь МТ) в полной терапевтической дозе; купирование обострений; тяжелые инфекционные заболевания (сепсис, септический артрит, пиелонефрит, остеомиелит, туберкулезная и грибковая инфекции, вирус иммунодефицита человека), злокачественные новообразования; беременность и лактация.
III. Пациент с поздним РА и остеопоротическими переломами
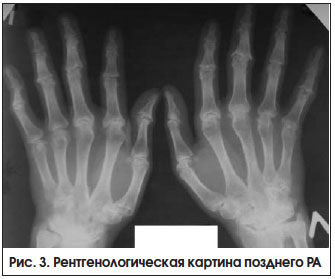
Поздняя стадия РА определяется как стадия необратимых структурных изменений (деформаций, подвывихов) суставов при длительности болезни > 2-х лет, с выраженными признаками активного воспаления или без них (рис. 3). Неуклонное прогрессирование болезни приводит к формированию различных видов подвывихов и контрактур суставов, в связи с чем возрастает роль реабилитационных и ортопедических мероприятий.
Развитие остеопороза (ОП) и ассоциированных с ним переломов является одним из наиболее тяжелых осложнений РА, определяющим неблагоприятное течение и прогноз болезни. Частота остеопоротических переломов среди больных РА в 1,5–2,5 раза выше, чем в общей популяции [9]. Предполагается, что развитие ОП и суставной деструкции при РА имеет единые патогенетические механизмы, в основе которых лежит цитокин-зависимая активация остеокластогенеза, приводящая к повышению костной резорбции [10]. Развитие ОП при РА определяется множеством общих и специфических, ассоциированных с заболеванием и лечением, факторов риска.
РА-ассоциированные факторы риска ОП и переломов [11]:
– активность воспалительного процесса,
– рентгенологическая стадия,
– тяжесть функциональных нарушений (HAQ > 1,25),
– длительность болезни,
– прием ГК,
– высокий риск падений.
У больных РА прием ГК в 4–5 раз повышает риск вертебральных переломов и удваивает риск переломов бедра. При этом доказано, что не существует безопасной дозы ГК. Также следует помнить, что развитие переломов у больных, получающих ГК, происходит при более высоких значениях минеральной плотности ткани (МПК), чем при первичном ОП, поэтому антиостеопоротическую терапию следует начинать при значениях Т-критерия < -1,5 стандартного отклонения от референсных значений.
Программа ведения больных РА и с остеопоротическими переломами включает контроль активности РА, коррекцию модифицируемых факторов риска ОП и переломов, предупреждение падений, антиостеопоротическую терапию, диету и физические упражнения. Всем больным РА необходимы проведение расчета абсолютного риска переломов (FRAX-алгоритм) (fracture risk assessment tool, 10-летний абсолютный риск перелома – инструмент оценки риска перелома ВОЗ) и профилактическое назначение препаратов кальция и витамина D. Назначение антиостеопоротической терапии без учета данных МПК проводится у пациентов в возрасте 65 лет и старше при наличии в анамнезе переломов при минимальной травме. Препаратами первой линии в лечении ОП у больных РА являются бисфосфонаты (БФ) и антитела к RANKL (лиганду рецептора активатора ядерного фактора каппа бета), обладающие антирезорбтивным действием (табл. 5). Привлекательность БФ при РА заключается еще и в том, что, по данным экспериментальных исследований, они могут оказывать благоприятное влияние на течение болезни. Установлено, что БФ способны ингибировать cинтез провоспалительных цитокинов и развитие костных эрозий при РА [12]. У пациентов с ранним артритом БФ в комбинации с МТ эффективно предотвращают развитие костной деструкции [13].

IV. Пожилой пациент с РА и НПВП-гастропатией
РА у лиц пожилого возраста характеризуется активным быстропрогрессирующим течением, высоким уровнем коморбидности и неблагоприятными исходами. Особое значение в структуре коморбидных состояний при РА имеют кардиоваскулярная и гастроинтестинальная патологии. По данным многочисленных исследований, сердечно-сосудистая заболеваемость и смертность у больных РА в 2–4 раза выше, чем в общей популяции, что диктует необходимость своевременного выявления и коррекции факторов кардиоваскулярного риска.
Рекомендации по снижению кардиоваскулярного риска у больных РА [14]:
• АСК следует принимать за ≥2 ч до приема нестероидных противовоcпалительных препаратов (НПВП).
• Не использовать НПВП в течение 3–6 мес. после острого сердечно-сосудистого события или процедуры.
• Регулярно контролировать артериальное давление.
• Использовать НПВП в низких дозах с коротким периодом полураспада (избегать назначения НПВП с пролонгированным высвобождением).
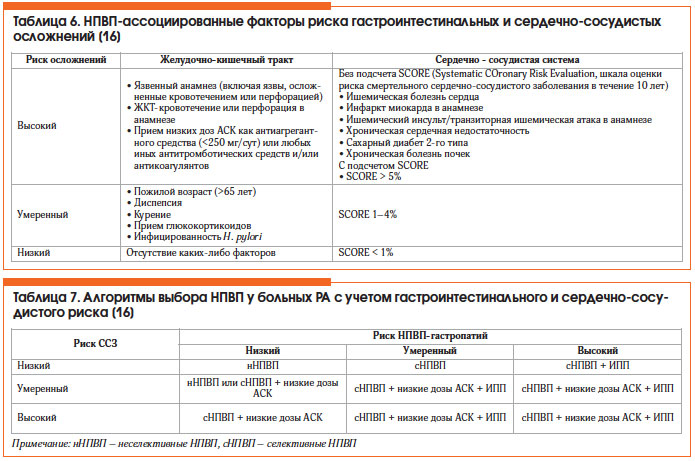
НПВП-гастропатия – одно из наиболее частых осложнений длительного приема НПВП, проявляющееся в виде эрозивного или язвенного поражения верхних отделов желудочно-кишечного тракта (ЖКТ) (преимущественно антральный и препилорический отделы желудка). Прием НПВП не влияет на прогрессирование РА, однако позволяет лучше контролировать симптомы заболевания на фоне терапии БПВП и ГИБП. НПВП-ассоциированные факторы риска гастроинтестинальных и сердечно-сосудистых осложнений представлены в таблице 6.
Экспертами EULAR разработан «калькулятор» для индивидуального подбора НПВП в зависимости от наличия факторов риска в отношении ЖКТ и сердечно-сосудистой системы [15]. К НПВП с наименьшим кардиоваскулярным риском отнесены напроксен, целекоксиб, кетопрофен, низкие дозы ибупрофена (<1200 мг/сут). Основные лекарственные средства, которые используют для лечения НПВП-индуцированных гастропатий, — ингибиторы протонной помпы (ИПП), Н2-блокаторы и мизопростол (синтетический аналог ПГ Е2). Алгоритмы выбора НПВП у больных РА с учетом гастроинтестинального и сердечно-сосудистого риска представлены в таблице 7 [16].
Не так давно появилась новая генерация НПВП, которые повышают активность оксида азота (NO) в слизистой желудка (NO-НПВП). Как известно, NO обладает гастропротективными свойствами: стимулирует секрецию слизи, бикарбоната, улучшает микроциркуляцию, ингибирует адгезию лейкоцитов к эндотелию, что и определяет фармакологические преимущества данной группы НПВП. Одним из представителей NO-НПВП является препарат Найзилат (амтолметин гуацил), который наряду с высокой анальгетической и противовоспалительной активностью обладает гастропротективными свойствами. В рандомизированных клинических исследованиях были продемонстрированы более низкие частота и тяжесть повреждений слизистой оболочки желудка после применения амтолметин гуацила по сравнению с таковыми других неселективных НПВП (диклофенак, индометацин, пироксикам), при сопоставимой противовоспалительной и анальгетической их эффективности [17]. Сравнительное исследование амтолметин гуацила 1200 мг/сут и целекоксиба 400 мг/сут у больных РА показало равнозначные эффективность и безопасность препаратов [18]. Терапевтическая доза амтолметин гуацила (Найзилат) составляет 600 мг 2 р./сут натощак, поддерживающая – 600 мг/сут.
Заключение
РА является гетерогенным заболеванием, исходы которого во многом определяются своевременной диагностикой болезни и правильно выбранной тактикой лечения. Ранняя стадия РА, особенно первые 3 мес. от начала заболевания, наиболее благоприятны для проведения эффективной базисной терапии. Основой ведения больных РА является тщательное мониторирование активности заболевания (не реже 1 р./3 мес.) с последующей коррекцией терапии при необходимости. Выбор терапии определяется стадией РА, активностью болезни, наличием ФНП, сосуществующими коморбидными состояниями, а также эффективностью предшествующего лечения.
Источник


