Алгоритм лечения ревматоидного артрита
Статья посвящена ревматоидный артриту — клиническим ситуацииям и алгоритмам лечения
Ревматоидный артрит (РА) – хроническое системное иммуновоспалительное заболевание неизвестной этиологии, сопровождающееся развитием симметричного прогрессирующего эрозивно-деструктивного полиартрита и внесуставными проявлениями [1]. РА ассоциирован с высоким риском кардиоваскулярных событий, остеопоротических переломов, ранней инвалидизацией и преждевременной смертностью пациентов. Улучшить прогноз и исходы болезни способны только своевременная диагностика и раннее активное лечение больных РА.
Течение болезни складывается из нескольких последовательных стадий: ранней, развернутой и поздней, каждая из них имеет свои клинические особенности и подходы к терапии.
Базовые принципы терапии РА («Treat to target» или «Лечение до достижения цели») [2, 3]:
1. Достижение ремиссии (DAS28 (суммарный индекс (включает упрощенный счет из 28 суставов), позволяет многократно оценивать активность РА и может быть использован для контроля его активности в повседневной практике) <2,6) или как минимум низкой активности заболевания (DAS28 <3,2).
2. Ранняя активная терапия базисными противовоспалительными препаратами (БПВП), в первую очередь метотрексатом (МТ), не позднее первых 3 мес. от начала болезни.
3. Лечение должно быть максимально активным, с быстрой эскалацией дозы МТ и последующим изменением (при необходимости) схемы лечения в течение 3 мес. до достижения ремиссии (или низкой активности) болезни.
4. Тщательный контроль изменений активности заболевания и коррекция терапии не реже 1 раза в 3 мес. или ежемесячно у больных с высокой и умеренной активностью РА.
5. В случае недостаточной эффективности стандартной терапии БПВП показано назначение генно-инженерных биологических препаратов (ГИБП).
6. Определение тактики терапии должно быть согласовано с пациентом.
К факторам неблагоприятного прогноза (ФНП) у больных РА относятся [4]:
– молодой возраст;
– женский пол;
– высокие титры ревматоидного фактора (РФ) и/или антитела к циклическому цитруллиновому пептиду (АЦЦП);
– эрозивный процесс в суставах по данным рентгенографического исследования или магнитно-резонансной томографии (МРТ);
– повышение уровней острофазовых показателей: скорости оседания эритроцитов (СОЭ) или С-реактивного белка (СРБ);
– высокая активность заболевания согласно индексам DAS28, SDAI (Simplified Disease Activity Index) или CDAI (Clinical Disease Activity Index);
– внесуставные проявления (синдром Шегрена, поражение легких и т. д.).
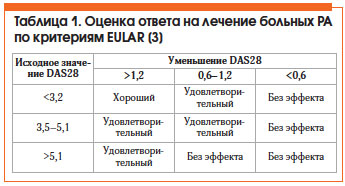
Оценка эффективности лечения РА по критериям Европейской антиревматической лиги (EULAR) представлена в таблице 1. Общепризнанным методом оценки активности РА является расчет индекса DAS28, который можно автоматически произвести на сайте www.das-score.nl.
Критерии эффективности терапии РА [5]:
• хороший клинический ответ (≈ ACR 70) (критерии Американской коллегии ревматологов);
• низкая активность болезни (DAS28 ≤ 3,2) или ремиссия (DAS28 ≤ 2,6);
• улучшение функции (HAQ (Health Assessment Questionare, опросник состояния здоровья, позволяющий оценить функциональные способности больных РА) <1,5) и качества жизни;
• предотвращение прогрессирования деструкции:
– замедление нарастания рентгенологических индексов (Sharp, Larsen);
– отсутствие появления новых эрозий;
– стабилизация или улучшение состояния по данным МРТ.
У пациентов, находящихся в состоянии ремиссии более 1 года после отмены глюкокортикостероидов (ГКС), следует рассмотреть вопрос о возможности прекращения лечения ГИБП, особенно если они применялись в комбинации с БПВП. Важное значение при определении тактики лечения имеет выбор пациентов.
Рассмотрим отдельные клинические ситуации и подходы к терапии при РА.
I. Пациент с впервые установленным ранним РА
Ранняя стадия РА – условно выделенная, клинико-патогенетическая стадия заболевания с длительностью активного синовита до 1 года, характеризуется преобладанием экссудативных изменений в пораженных суставах, частым атипичным течением и хорошим ответом на лечение. Выделение понятия «ранний РА» связано со сложившимися представлениями о патогенезе болезни и необходимости проведения ранней активной терапии РА. Ранний РА может дебютировать как недифференцированный артрит, что требует динамического наблюдения за больными и проведения тщательного дифференциально-диагностического поиска. На ранней стадии РА наиболее информативными являются диагностические критерии Американского и Европейского ревматологических сообществ, предложенные в 2010 г. (табл. 2).

Диагноз РА может быть установлен при общем счете не менее 6 баллов.
Доказано, что адекватная базисная терапия на ранней стадии РА позволяет предотвратить структурные повреждения, что способствует сохранению функциональной активности пациентов и улучшает отдаленный прогноз. БПВП необходимо назначать не позднее 3 мес. от начала РА с быстрой эскалацией дозы для достижения оптимального эффекта (DAS <2,4) и последующей заменой препарата в течение 3–6 мес. при его неэффективности [1]. Терапию БПВП следует продолжать даже при снижении активности заболевания и достижении ремиссии.
К БПВП первого ряда отнесены МТ, лефлуномид (ЛФ) и сульфасалазин (СС) (табл. 3), т. к. доказана их эффективность в отношении предотвращения деструктивных изменений суставов (уровень доказательности А). Препараты «второй линии» (гидроксихлорохин, препараты золота и др.) применяются при неэффективности препаратов первого ряда либо в комбинации с ними.
МТ – «золотой стандарт» терапии активного РА. При необходимости назначения МТ в дозе > 15 мг/нед. рекомендуется использовать парентеральный путь введения (в/м или п/к). Также с целью минимизации побочных явлений необходимо назначение фолиевой кислоты 1 мг/cут (5 мг/нед.), исключая дни приема МТ.

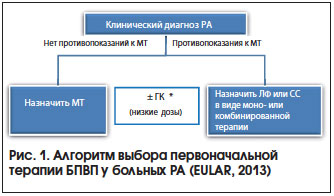
Основные стратегии лечения раннего РА (рис. 1) [7]:
1. Монотерапия МТ c последующей заменой на другие БПВП (ЛФ, СС) через 3–6 мес. в случае неэффективности или плохой переносимости).
2. Комбинированная базисная терапия, в т. ч. в сочетании с высокой дозой ГК. Используются комбинации БПВП как первого ряда (МТ + СС или МТ + ЛФ), так и второго ряда (МТ + Плаквенил) и т. д.
3. Комбинированная терапия синтетическими БПВП + ГИБП (в первую очередь ингибиторы фактора некроза опухоли (ФНО) при сохраняющейся > 3–6 мес. высокой активности РА, а также при наличии ФНП. Например, МТ 25 мг/нед. + Инфликсимаб 3 мг/кг массы тела.
II. Пациент с развернутым РА, не отвечающий на традиционные БПВП
Развернутая стадия РА – заболевание с отчетливо выраженной симптоматикой и длительностью болезни более 1 года. Суставной синдром имеет стойкий, симметричный и полиартикулярный характер с преимущественным поражением суставов кистей и стоп, выявляются признаки высокой или умеренной лабораторной активности, серопозитивность по РФ, эрозивный процесс в суставах по данным рентгенографии. Если диагноз устанавливается впервые, то стратегия ведения больного та же, что и при раннем РА. В случае уже проводившегося лечения с недостаточным эффектом или непереносимостью синтетических БПВП (как в виде монотерапии, так и при комбинированном их использовании), а также наличием ФНП прибегают к назначению ГИБП (рис. 2). Использование ГИБП позволяет максимально избирательно воздействовать на отдельные звенья иммунопатогенеза РА и существенно улучшить состояние больных РА, резистентных к стандартным БПВП и ГК [8]. Установлено, что комбинация традиционных БПВП с ГИБП более эффективна, чем монотерапия.
Назначение ГИБП показано:
– при длительно сохраняющейся (> 3–6 мес.) высокой активности РА;
– при высокой активности заболевания < 3 мес., только при наличии у больных ФНП.
Препаратами первого ряда среди ГИБП являются ингибиторы ФНО-α. Другие ГИБП назначаются больным РА с неадекватным ответом на блокаторы ФНО-α или при невозможности их применения (табл. 4).

Противопоказания к назначению ГИБП: отсутствие лечения одним или более БПВП (в первую очередь МТ) в полной терапевтической дозе; купирование обострений; тяжелые инфекционные заболевания (сепсис, септический артрит, пиелонефрит, остеомиелит, туберкулезная и грибковая инфекции, вирус иммунодефицита человека), злокачественные новообразования; беременность и лактация.
III. Пациент с поздним РА и остеопоротическими переломами
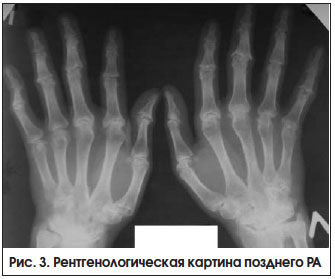
Поздняя стадия РА определяется как стадия необратимых структурных изменений (деформаций, подвывихов) суставов при длительности болезни > 2-х лет, с выраженными признаками активного воспаления или без них (рис. 3). Неуклонное прогрессирование болезни приводит к формированию различных видов подвывихов и контрактур суставов, в связи с чем возрастает роль реабилитационных и ортопедических мероприятий.
Развитие остеопороза (ОП) и ассоциированных с ним переломов является одним из наиболее тяжелых осложнений РА, определяющим неблагоприятное течение и прогноз болезни. Частота остеопоротических переломов среди больных РА в 1,5–2,5 раза выше, чем в общей популяции [9]. Предполагается, что развитие ОП и суставной деструкции при РА имеет единые патогенетические механизмы, в основе которых лежит цитокин-зависимая активация остеокластогенеза, приводящая к повышению костной резорбции [10]. Развитие ОП при РА определяется множеством общих и специфических, ассоциированных с заболеванием и лечением, факторов риска.
РА-ассоциированные факторы риска ОП и переломов [11]:
– активность воспалительного процесса,
– рентгенологическая стадия,
– тяжесть функциональных нарушений (HAQ > 1,25),
– длительность болезни,
– прием ГК,
– высокий риск падений.
У больных РА прием ГК в 4–5 раз повышает риск вертебральных переломов и удваивает риск переломов бедра. При этом доказано, что не существует безопасной дозы ГК. Также следует помнить, что развитие переломов у больных, получающих ГК, происходит при более высоких значениях минеральной плотности ткани (МПК), чем при первичном ОП, поэтому антиостеопоротическую терапию следует начинать при значениях Т-критерия < -1,5 стандартного отклонения от референсных значений.
Программа ведения больных РА и с остеопоротическими переломами включает контроль активности РА, коррекцию модифицируемых факторов риска ОП и переломов, предупреждение падений, антиостеопоротическую терапию, диету и физические упражнения. Всем больным РА необходимы проведение расчета абсолютного риска переломов (FRAX-алгоритм) (fracture risk assessment tool, 10-летний абсолютный риск перелома – инструмент оценки риска перелома ВОЗ) и профилактическое назначение препаратов кальция и витамина D. Назначение антиостеопоротической терапии без учета данных МПК проводится у пациентов в возрасте 65 лет и старше при наличии в анамнезе переломов при минимальной травме. Препаратами первой линии в лечении ОП у больных РА являются бисфосфонаты (БФ) и антитела к RANKL (лиганду рецептора активатора ядерного фактора каппа бета), обладающие антирезорбтивным действием (табл. 5). Привлекательность БФ при РА заключается еще и в том, что, по данным экспериментальных исследований, они могут оказывать благоприятное влияние на течение болезни. Установлено, что БФ способны ингибировать cинтез провоспалительных цитокинов и развитие костных эрозий при РА [12]. У пациентов с ранним артритом БФ в комбинации с МТ эффективно предотвращают развитие костной деструкции [13].

IV. Пожилой пациент с РА и НПВП-гастропатией
РА у лиц пожилого возраста характеризуется активным быстропрогрессирующим течением, высоким уровнем коморбидности и неблагоприятными исходами. Особое значение в структуре коморбидных состояний при РА имеют кардиоваскулярная и гастроинтестинальная патологии. По данным многочисленных исследований, сердечно-сосудистая заболеваемость и смертность у больных РА в 2–4 раза выше, чем в общей популяции, что диктует необходимость своевременного выявления и коррекции факторов кардиоваскулярного риска.
Рекомендации по снижению кардиоваскулярного риска у больных РА [14]:
• АСК следует принимать за ≥2 ч до приема нестероидных противовоcпалительных препаратов (НПВП).
• Не использовать НПВП в течение 3–6 мес. после острого сердечно-сосудистого события или процедуры.
• Регулярно контролировать артериальное давление.
• Использовать НПВП в низких дозах с коротким периодом полураспада (избегать назначения НПВП с пролонгированным высвобождением).
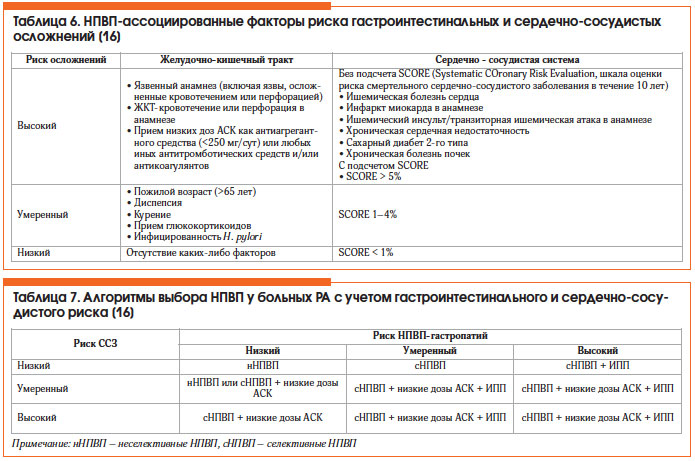
НПВП-гастропатия – одно из наиболее частых осложнений длительного приема НПВП, проявляющееся в виде эрозивного или язвенного поражения верхних отделов желудочно-кишечного тракта (ЖКТ) (преимущественно антральный и препилорический отделы желудка). Прием НПВП не влияет на прогрессирование РА, однако позволяет лучше контролировать симптомы заболевания на фоне терапии БПВП и ГИБП. НПВП-ассоциированные факторы риска гастроинтестинальных и сердечно-сосудистых осложнений представлены в таблице 6.
Экспертами EULAR разработан «калькулятор» для индивидуального подбора НПВП в зависимости от наличия факторов риска в отношении ЖКТ и сердечно-сосудистой системы [15]. К НПВП с наименьшим кардиоваскулярным риском отнесены напроксен, целекоксиб, кетопрофен, низкие дозы ибупрофена (<1200 мг/сут). Основные лекарственные средства, которые используют для лечения НПВП-индуцированных гастропатий, — ингибиторы протонной помпы (ИПП), Н2-блокаторы и мизопростол (синтетический аналог ПГ Е2). Алгоритмы выбора НПВП у больных РА с учетом гастроинтестинального и сердечно-сосудистого риска представлены в таблице 7 [16].
Не так давно появилась новая генерация НПВП, которые повышают активность оксида азота (NO) в слизистой желудка (NO-НПВП). Как известно, NO обладает гастропротективными свойствами: стимулирует секрецию слизи, бикарбоната, улучшает микроциркуляцию, ингибирует адгезию лейкоцитов к эндотелию, что и определяет фармакологические преимущества данной группы НПВП. Одним из представителей NO-НПВП является препарат Найзилат (амтолметин гуацил), который наряду с высокой анальгетической и противовоспалительной активностью обладает гастропротективными свойствами. В рандомизированных клинических исследованиях были продемонстрированы более низкие частота и тяжесть повреждений слизистой оболочки желудка после применения амтолметин гуацила по сравнению с таковыми других неселективных НПВП (диклофенак, индометацин, пироксикам), при сопоставимой противовоспалительной и анальгетической их эффективности [17]. Сравнительное исследование амтолметин гуацила 1200 мг/сут и целекоксиба 400 мг/сут у больных РА показало равнозначные эффективность и безопасность препаратов [18]. Терапевтическая доза амтолметин гуацила (Найзилат) составляет 600 мг 2 р./сут натощак, поддерживающая – 600 мг/сут.
Заключение
РА является гетерогенным заболеванием, исходы которого во многом определяются своевременной диагностикой болезни и правильно выбранной тактикой лечения. Ранняя стадия РА, особенно первые 3 мес. от начала заболевания, наиболее благоприятны для проведения эффективной базисной терапии. Основой ведения больных РА является тщательное мониторирование активности заболевания (не реже 1 р./3 мес.) с последующей коррекцией терапии при необходимости. Выбор терапии определяется стадией РА, активностью болезни, наличием ФНП, сосуществующими коморбидными состояниями, а также эффективностью предшествующего лечения.
Источник

В современной медицине, несмотря на все прогрессивные достижения, остается большое количество заболеваний, имеющих недостаточно изученные причины и сложные многоступенчатые механизмы развития, формирующие разнообразную клиническую картину с поражением тканей и органов, что обуславливает сложности в лечении. Например, системные заболевания соединительной ткани. К этой группе заболеваний относится ревматоидный артрит, отличительной чертой которого является эрозионно-деструктивное поражение суставов, преимущественно мелких. Причина его до сих пор не установлена, в механизме развития основная роль принадлежит атаке иммунитета на собственные ткани организма.
Продолжаются исследования причин и механизмов развития указанной патологии, поиск новых, более эффективных и безопасных методик лечения, особенно комплексного.
Ревматоидный артрит суставов: симптомы и лечение
Ревматоидный артрит характеризуется прогрессирующим разрушением суставов, которые на поздних стадиях заболевания приобретают необратимый характер. Типичные признаки патологии:
- наличие эрозивно-деструктивных элементов в области суставных поверхностей;
- разрушение мелких суставов;
- симметричное поражение;
- развитие воспаления в области стоп и кистей;
- деформации, препятствующие нормальному функционированию суставов.
Помимо типичных суставных поражений характерны также и нарушения со стороны других тканей и систем, включающие наличие серозитов (воспалительный процесс в области оболочек сердца, брюшины, плевральной оболочки), формирование воспалительных узелков под кожей, поражение сосудов в виде васкулитов, увеличение лимфоузлов (лимфаденопатии) и периферические поражения нервных окончаний (нейропатии).
Методы лечения ревматоидного артрита определяет врач-ревматолог, специализирующийся на аутоиммунных, воспалительных заболеваний. Он проводит полноценную диагностику: внешний осмотр с анализом всех жалоб и их подробной фиксацией в карте, проведение целого ряда лабораторных анализов и инструментальных исследований (включая данные УЗИ, рентгенографии и иных дополнительных процедур).
Медицинская коррекция базируется на длительных курсах лекарственных препаратов в сочетании с физиотерапией и немедикаментозными методиками, диетической коррекцией и, в некоторых случаях, с оперативным вмешательством. Проводятся курсы противорецидивной терапии и реабилитации, при этом чем раньше будут назначены препараты и рекомендованы методы лекарственного воздействия, тем более благоприятным будет прогноз. В запущенных случаях заболевание грозит стойкой инвалидностью.
Чаще подобная проблема возникает у взрослых, для детей типична своеобразная форма отклонения в виде ЮРА (ювенильной), с особенностями клинической симптоматики, диагностики и терапевтических подходов.

Причины и диагностика патологии
Точные причины заболевания на сегодняшний день не установлены, хотя имеются теории о природе его развития. По мнению большинства исследователей, имеют место наследственная предрасположенность, перенесенные инфекции и действие провоцирующих факторов. Отмечено, что некоторые микроорганизмы (ретровирусы, вирусы герпеса, цитомегаловирус, Эпштейн-Барр, краснухи, а также микоплазмы) способствуют развитию воспалительных процессов в суставах. В результате перенесённой инфекции и неправильной работы иммунитета происходит запуск аутоиммунных реакций — агрессии собственного иммунитета против соединительной ткани суставов и других частей тела, что приводит к разрастанию соединительной ткани и разрушению хрящевых структур и их необратимой деформацией. Процесс приводит к контрактурам — ограничениям в движениях и необратимым деформациям суставов, подвывихам и нарушению их функциональной активности.
При обращении к специалисту с жалобами «у меня ревматоидный артрит, как и чем лечить», выявляются следующие симптомы:
- скованность в суставах по утрам, проходящая через некоторое время;
- деформация мелких суставов пальцев кистей и стоп (специфический симптом – деформация пальцев кисти по типу «пуговичной петли» или «ласт моржа»;
- симметричные изменения суставов конечностей;
- отёк области суставов.
В результатах лабораторных исследований обнаруживается увеличение СОЭ, щелочной фосфатазы и специфических показателей системных заболеваний – ревматоидного фактора, сиаловых кислот и серомукоида. При рентгенологическом исследовании появляются специфические симптомы поражения суставов.
Ревматоидный артрит: лечение в домашних условиях или стационарно?
Помещение пациента в стационар, когда возникают подозрения на развитие болезни или при уже установленном диагнозе, показано в следующих случаях:
- при необходимости подтверждения или опровержения диагноза, для уточнения особенностей течения, оценки прогноза в отношении дальнейшей жизни и трудоспособности, решения вопроса с инвалидностью;
- подбор базисной противовоспалительной терапии (БПВТ) препаратами на начальном этапе и затем на протяжении болезни;
- при резком обострении и развитии осложнений;
- когда имеют место тяжелые и системные проявления с вовлечением нервной системы и серозных оболочек;
- при формировании сопутствующих осложнений, признаков септического артрита или других, в том числе связанных с приемом лекарств.
Во всех остальных случаях допускается лечение в домашних условиях при строгом условии постоянного контроля врача с регулярным прохождением обследований.

Как избавиться от ревматоидного артрита: принципы терапии
Основу составляет комплексный подход и сочетание приема лекарств с немедикаментозными методиками, диетой, физионагрузками и реабилитационными мероприятиями. При необходимости к консультированию и разработке схемы терапии привлекается врач-ортопед, невролог, кардиолог, психотерапевт. При незначительной деформации суставов пациентам можно продолжать привычную деятельность с ограничением физических нагрузок и стрессов, при условии профилактики инфекционных заболеваний и отказа от вредных привычек.
Не менее важное условие для уменьшении симптомов, особенно в области нижних конечностей – это контроль за массой тела, что уменьшает нагрузки на пораженные суставные поверхности и кости, снижает риск остеопороза, переломов и деформаций. Правильно подобранная диета с высоким содержанием полиненасыщенных жирных кислот, качественных животных и растительных белков помогает в уменьшении интенсивности воспаления и стимулирует восстановление хрящевых тканей.
Врач подробно рассказывает пациенту как уменьшить проявление болезни за счет изменений физической активности, посредством занятий лечебной физкультурой и применения физиотерапевтических методик. В стадии минимальных проявлений или в период ремиссии показано санаторно-курортное оздоровление.
Стандарт лечения ревматоидного артрита
В последние время наблюдается ощутимый прогресс в понимании основных механизмов формирования, патологию рассматривают как хроническое воспалительное заболевание иммунной природы, при котором наиболее эффективна терапия в начальный период. Сегодня разработан новый стандарт, включающий применение целого ряда препаратов различного действия:
- нестероидные противовоспалительные средства (НПВС);
- гормональные (глюкокортикостероиды, или ГКС);
- биологические;
- синтетические средства для купирования иммунных и воспалительных реакций.
Основа улучшения самочувствия – это базисная противовоспалительная терапия (БПВТ), которую важно начать в первые месяцы развития, причем прием лекарственных средств должен быть регулярным (перорально, инъекционно), с постоянным изменением схемы при малой эффективности. Исчезновение или уменьшение клинических симптомов и признаков воспаления по лабораторным данным свидетельствует о результативности проводимых мер. Применение БПВТ должно осуществляться с учетом возможных побочных эффектов.
Как вылечить ревматоидный артрит
В острой стадии или при обострении хронической патологии необходима медикаментозная коррекция, но как проходит лечение, определяет исключительно лечащий врач. Применяются стероидные средства, препараты фактора некроза опухоли (ФНО), нестероидные противовоспалительные средства (НПВС).
На первом этапе проводят подавление острых процессов, с последующим переходом на поддерживающую терапию в период затухания симптомов и ремиссии. Нестероидные лекарства применяются наиболее активно, обычно это группа неселективных ингибиторов ЦОГ (циклооксигеназа — фермент, ответственный за синтез веществ, способствующих развитию воспаления). Эффект при их приеме развивается быстро, после 3-5 суток приема, но сами лекарства обладают целым рядом побочных эффектов, ограничивающих их длительное применение и выбор для некоторых категорий пациентов. Активно применяют селективные ингибиторы ЦОГ, обладающие меньшим списком побочных эффектов, они относятся к средствам нового поколения, лучше переносятся и более эффективны.
Лечение ревматоидного артрита подразумевает также лекарства группы глюкокортикоидов. Они быстро и сильно подавляют иммунные и воспалительные реакции, влияют на обменные процессы и применимы при неэффективности нестероидных противовоспалительных лекарств. ГКС уменьшают воспаление в области суставов и снижают вероятность поражения внутренних органов, но также имеют внушительный список побочных эффектов и противопоказаний, в связи с чем их употребление строго контролируется и подбирается очень тщательно и индивидуально. При пульс-терапии, в комбинации с цитостатическими средствами применяются только на базе стационара. Домашний неконтролируемый прием этих препаратов запрещен, они могут быть опасными в плане серьезных осложнений.

Препараты нового поколения для лечения ревматоидного артрита
На сегодняшний день для борьбы с данной патологией широко применяются препараты нового ряда – биологическая терапия. Специфические соединения, относящиеся к группе ингибиторов ФНО (факторы некроза опухоли), не позволяют разворачиваться клинической картине иммунного воспаления. Средства относительно недавно применяются, показали хорошие результаты, но значительно влияют на иммунитет, подавляя его на фоне длительного приема. Их назначают в сложных случаях, когда заболевание устойчиво к привычным средствам. Биопрепараты обладают одним существенным недостатком — высокой стоимостью, что ограничивает их широкое применение.
Местная терапия
Практикуется и наружный способ применения медикаментов, с этими целями назначаются лекарства для местного нанесения – гели, мази, кремы, пластыри с противовоспалительными компонентами. Основной эффект заключается в локальном воздействии на ткани сустава и околосуставные поверхности, лекарства используются с целью уменьшения боли и отека. Однако они обладают низкой эффективностью по сравнению с лекарствами, которые принимаются внутрь (таблетки), и рекомендуются только в комплексной терапии.
Часто наружные средства имеют многокомпонентный состав, могут содержать НПВС, гепарин (для улучшения микроциркуляции и проницаемости сосудов), местные анестетики (для уменьшения болезненности сустава).
Как лечиться от ревматоидного артрита при помощи физиотерапии
По мере стихания острого процесса всегда встает вопрос о том, что делать далее, в стадию затухания воспаления и при выходе в ремиссии. На этапе дополнительной коррекции, в том числе и в домашних условиях, показаны физионагрузки. Процедуры способствуют снижению болевых ощущений, устранению скованности по утрам, расширяют физическую активность пациента.
Применяются методики воздействия гальваническими токами и магнитными полями на область пораженных поверхностей, аппликации парафина или озокерита. Не менее эффективны и методики дозированного облучения инфракрасными лучами или ультразвуком определенной частоты.
Магнитотерапия при заболеваниях суставов оказывает наиболее выраженное положительное действие:
- уменьшает боли и отеки в области суставов;
- повышает объем движений;
- устраняет утреннюю скованность;
- позволяет уменьшить лекарственную нагрузку на организм, так как снижает необходимость приема препаратов с обезболивающим эффектом.
Хотя данные методики обладают достаточной активностью, они не могут применяться как единственное средство при решении вопроса как вылечить ревматоидный артрит и без назначения врача. Физиотерапия показана как дополнительная методика на фоне базисного лечения.
Задать вопрос врачу
Остались вопросы по теме «Как вылечить ревматоидный артрит»?
Задайте их врачу и получите бесплатную консультацию.
Источник

