Доказательная медицина ревматоидный артрит
Этиология РА неизвестна, что делает невозможным проведение эффективной этиотропной терапии. Поэтому лечение РА остается одной из наиболее сложных проблем современной клинической медицины и фармакологии. Однако расшифровка патогенетических механизмов, лежащих в основе ревматоидного воспаления, послужила основой для разработки концепции патогенетической (базисной) терапии, которая сформировалась более 10 лет назад. К числу базисных относят большое число разнообразных по химической структуре и фармакологическим свойствам лекарственных средств.
Их объединяет способность в большей или меньшей степени и за счет различных механизмов подавлять воспаление и/или патологическую активацию системы иммунитета. Прогресс, достигнутый в лечении РА в последние годы, очень хорошо виден при сопоставлении Международных рекомендаций (Американская коллегия ревматологов) по фармакотерапии РА, опубликованных в 1996 и 2002 годах. За это время разработаны новые симптоматические (ЦОГ2 ингибиторы) и базисные (лефлюномид, антицитокины) препараты, что самое главное более четко сформулирована концепция ранней агрессивной терапии РА.
Лечение ревматоидного артрита
Основные задачи фармакотерапии РА представлены на рисунке 4. В последние годы стало особенно очевидным, что наиболее высокая скорость нарастания рентгенологических изменений в суставах наблюдается именно на ранних стадиях РА, что коррелирует с неблагоприятным прогнозом. Поскольку применение базисных препаратов при раннем РА позволяет модифицировать течение болезни, лечение РА (как и многих других хронических заболеваний человека, таких как сахарный диабет, артериальная гипертензия, ИБС и др.) должно начинаться как можно раньше, желательно в течение первых 3х месяцев после постановки достоверного диагноза РА.
Это особенно важно у пациентов, имеющих факторы риска неблагоприятного прогноза, к которым относятся высокие титры ревматоидного фактора, выраженное увеличение СОЭ, поражение более 20 суставов, наличие внесуставных проявлений (ревматоидные узелки, синдром Шегрена, эписклерит и склерит, интерстициальное поражение легких, перикардит, системный васкулит, синдром Фелти). Например, у серопозитивных пациентов с полиартритом в дебюте болезни вероятность тяжелого эрозивного поражения суставов в течение первых двух лет болезни чрезвычайно высока (70%).
В то же время следует обратить внимание на трудности дифференциальной диагностики раннего РА (< 6-12 мес от начала симптомов) от ряда других ревматических и неревматических заболеваний (грипп, краснуха, парвовирус В19, корь, гепатит, лаймборрелиоз, серонегативные спондилоартропатии, микрокристаллические артриты, ревматическая лихорадка, СЗСТ, остеоартроз, ревматическая полимиалгия, системные васкулиты, опухолевый артрит и др.), которые могут начинаться с ревматоидоподобного поражения суставов.
Ниже суммированы клинические и лабораторные признаки, позволяющие заподозрить дебют РА, при наличии которых пациент должен быть незамедлительно направлен на консультацию к врачуревматологу. После постановки достоверного диагноза РА всем больным необходимо провести базовое клиническое, лабораторное и инструментальное обследование.
При каждом визите пациента врачревматолог должен оценить активность болезни. Разработаны международные критерии эффективности терапии и клинической ремиссии. По критериям Американской коллегии ревматологов (ACR), свидетельством эффективности терапии может быть 20% улучшение (ACR20) счета припухших и болезненных суставов, наряду с 20% улучшением 3 из 5 следующих параметров: общая оценка эффективности лечения по мнению врача и пациента, оценка интенсивности боли по мнению пациента, оценка степени потери трудоспособности и острофазовых показателей.
Нестероидные противовоспалительные препараты
Основной метод симптоматического лечения РА назначение нестероидных противовоспалительных препаратов (НПВП) с целью уменьшения боли и воспаления в суставах. Условно НПВП подразделяются на короткоживущие (диклофенак, кетопрофен, лорноксикам (Ксефокам) и др.) (< 6 часов) и длительноживущие (пироксикам, напроксен и др.) (> 6 часов). Однако четкая связь между периодом полужизни НПВП в плазме и его клинической эффективностью не прослеживается. Короткоживущие препараты могут длительно и в высокой концентрации накапливаться в зоне воспаления, например, в полости сустава.
Поэтому однодвукратный прием короткоживу щих препаратов нередко столь же эффективен, как и многократный. При выборе НПВП необходимо учитывать ряд факторов: эффективность, переносимость, безопасность и стоимость препаратов. У пациентов, имеющих факторы риска осложнений со стороны желудочнокишечного тракта, препаратами выбора являются так называемые селективные ингибиторы циклооксигеназы (ЦОГ)2. Ограничением монотерапии НПВП является то, что эти препараты редко полностью подавляют клинические проявления артрита, не влияют на прогрессирование повреждения суставов и вызывают побочные эффекты, особенно у лиц пожилого возраста.
К факторам риска желудочнокишечных побочных эффектов относятся пожилой возраст (старше 75 лет), ?язвенный? анамнез, сочетанное применение глюкокортикостероидов, тяжелые сопутствующие заболевания, прием высоких доз НПВП или одномоментное применение нескольких препаратов. Для профилактики и лечения НПВПиндуцировнных поражений ЖКТ можно использовать блокаторы H2гистаминовых рецепторов (только высокие дозы), ингибиторы протонной помпы и мизопростол.
Следует подчеркнуть: хотя симптомы диспепсии, очень часто возникающие на фоне приема НПВП, нередко купируются низкими дозами блокаторов Н2гистаминовых рецепторов, их прием не только не уменьшает, но может даже увеличивать риск тяжелых осложнений со стороны ЖКТ (прободений, перфоративных язв и желудочных кровотечений). Хотя селективные ингибиторы ЦОГ2 существенно реже вызывают поражение ЖКТ, чем стандартные НПВП, на фоне их приема также могут возникать нежелательные эффекты, включая симптомы диспепсии, замедление заживления язв желудка и 12перстной кишки, задержка жидкости, повышение артериального давления.
Кроме того, в одном исследовании было показано, что у пациентов РА, принимавших селективный ингибитор ЦОГ2 (рофекоксиб), отмечается более высокая частота тромботических осложнений (инфаркт миокарда), чем у пациентов, принимающих напроксен. Однако данные других исследований свидетельствуют о том, что применение других селективных ингибиторов ЦОГ2 мелоксикама и целекоксиба не приводит к нарастанию частоты кардиоваскулярных тромбозов, по сравнению с пациентами, принимавшими ?стандартные? НПВП.
Применение как ?стандартных? НПВП, так и селективных ингибиторов ЦОГ2 должно проводиться с особой осторожностью у пациентов со сниженным внутрисосудистым объемом или отеками, связанными с застойной сердечной недостаточностью, нефротическим синдромом, циррозом печени и при повышении креатинина более 2,5 мг%.
Глюкокортикоиды
Лечение низкими (< 10 мг/сут) дозами глюкокортикоидов (ГКС) нередко позволяет адекватно контролировать ревматоидные воспаления, не уступая в этом отношении базисным противоревматическим препаратам приемлемым профилем токсичности, снижением скорости рентгенологического прогрессирования у больных с ранним активным РА (особенно при сочетанном применении с метотрексатом).
Особенно показано назначение ГКС у пациентов, не отвечающих на НПВП или имеющих противопоказания для их назначения в адекватной дозе. К сожалению, у многих пациентов попытка отмены ГКС приводит к обострению синовита, даже несмотря на использование базисных препаратов, то есть развивается функциональная глюкокортикоидная зависимость.
Пульстерапия ГКС (метилпреднизолон, дексаметазон) позволяет достигнуть быстрого (в течение 24 часов), но кратковременного (3-12 нед) подавления активности воспалительного процесса, даже у больных, резистентных к предшествующей терапии. Однако влияние пульстерапии на рентгенологическое прогрессирование поражения суставов не доказано.
Локальная терапия ГКС имеет вспомогательное значение. Ее целью является подавление активного синовита в начале болезни и его обострений в 1 или нескольких суставах, улучшение функции суставов. Однако глюкокортикоиды оказывают влияние только на локальный процесс (а РА системное заболевание) и вызывают только временное улучшение.
Наиболее эффективны пролонгированные глюкокортикоиды (триамцинолон, метилпреднизолон) и особенно бетаметазон. Следует иметь в виду, что не каждое обострение моноартрита при РА связано с активностью самого заболевания, это может быть проявление инфекционного или микрокристаллического артрита. Не рекомендуется проведение повторных инъекций ГКС в один и тот же сустав чаще, чем один раз в три месяца. Потребность в более частых инъекциях может отражать неадекватность ?базисной? терапии.
Хотя у пациентов РА наблюдается склонность к развитию остеопороза независимо от глюкокортикоидной терапии, у пациентов, получающих даже низкие дозы ГКС перорально, отмечается увеличение риска остеопоретических переломов. Это диктует необходимость периодического определения минеральной плотности костной ткани (МПКТ) с помощью методов костной денситометрии (примерно раз в 12 мес) и обязательного назначения препаратов кальция (1500 мг) и колекальциферола (400-800 МЕ в сутки) с момента назначения ГКС. При недостаточной эффективности целесообразно применение других антиостеопоретических препаратов, таких как бисфосфонаты и кальцитонин.
Базисная терапия
Эффективность базисных препаратов в виде моно или комбинированной терапии в отношении контролирования симптомов поражения суставов, положительное влияние на рентгенологическое прогрессирование, функциональный статус и качество жизни, строго доказана в процессе плацебоконтролируемых исследованиях. Полагают, что их применение позволяет снизить общую стоимость медицинского обслуживания пациентов, а рано начатая адекватная базисная терапия может способствовать увеличению продолжительности жизни пациентов РА.
Показанием для незамедлительного (в течение 3х месяцев) назначения базисных препаратов является достоверный РА, при котором, несмотря на применение НПВП в адекватных дозах, сохраняются боли в суставах, утренняя скованность (или общее недомогание), активный синовит, стойкое увеличение СОЭ или СРБ, и/или признаки эрозивного поражения суставов.
«Базисная» терапия снижает потребность в НПВП и глюкокортикоидах (а следовательно, вероятность развития побочных эффектов, возникающих на фоне лечения этими препаратами), позволяет улучшить качество жизни и отдаленный прогноз. К «недостаткам» базисной терапии следует отнести необходимость тщательного мониторинга за развитием побочных эффектов.
Выбор того или иного «базисного» препарата зависит от ряда субъективных и объективных факторов и должен быть по возможности индивидуализирован. К сожалению, сравнению эффективности и безопасности различных «базисных» препаратов и комбинированной терапии несколькими «базисными» препаратами посвящено относительно мало исследований. У женщин детородного возраста на фоне приема большинства «базисных» препаратов необходима эффективная контрацепция, а случае наступления беременности или при кормлении грудью режим приема «базисных» препаратов должен быть модифицирован.
Учитывая высокую безопасность, многие ревматологи предпочитают начинать базисную терапию с назначения гидроксихлорохина или сульфасалазина, эффективность которых (особенно у пациентов с ранним РА) с умеренной активностью доказана во многих исследованиях. Хотя монотерапия гидроксихлорохином не замедляет рентгенологическое прогрессирование поражения суставов, в целом она достаточно эффективна в отношении улучшения отдаленного прогноза болезни.
Сульфасалазин подавляет воспаление быстрее, чем гидроксихлорохин в течение первого месяца от начала терапии. Кроме того, на фоне лечения отмечается замедление рентгенологического прогрессирования болезни. Побочные эффекты в виде тошноты и болей в животе выражены умеренно и обычно развиваются в течение первых нескольких месяцев терапии. Частота побочных эффектов уменьшается при медленном увеличении дозы препарата.
Однако лейкопения и другие более тяжелые побочные эффекты могут развиться в любой период лечения, что диктует необходимость периодического лабораторного обследования. При отсутствии клинического эффекта в течение 4 месяцев необходимо назначение другого базисного препарата.
У пациентов с активным РА или имеющих факторы риска неблагоприятного прогноза препаратом выбора является метотрексат, который обладает наиболее благоприятным соотношением эффективность/токсичность. Это позволяет рассматривать его в качестве ?олотого стандарта фармакотерапии РА при проведении испытаний эффективности и безопасных новых базисных препаратов.
Имеются данные о том, что более 50% пациентов РА могут принимать метотрексат более 3х лет, что существенно больше, чем других базисных препаратов. В целом, прекращение лечения метотрексатом чаще связано с развитием побочных эффектов, чем с неэффективностью лечения. Частоту многих побочных эффектов (стоматит, тошнота, диарея, алопеция) можно снизить при назначении фолиевой кислоты, без потери эффективности.
Относительными противопоказаниями для назначения метотрексата являются заболевания печени, существенное нарушение функции почек, болезни легких и злоупотребление алкоголем. Несмотря на то, что наиболее частым побочным эффектом является увеличение печеночных ферментов, риск тяжелого поражения печени низок. Проведение биопсии печени показано только пациентам со стойким увеличением уровня печеночных ферментов после прекращения приема препарата.
Пациентам, которым противопоказано лечение метотрексатом, у которых на фоне лечения метотрексатом (до 25 мг/нед) не удается достигнуть стойкого клинического улучшения или развиваются побочные эффекты, показано назначение нового базисного препарата лефлюномида, биологических агентов, или других базисных препаратов в виде моно или комбинированной терапии.
Снижение активности РА и замедление рентгенологического прогрессирования на фоне лечения лефлюномида выражено в той же степени, что и при использовании метотрексата. Кроме того, лефлюномид может быть с успехом использован в комбинации с метотрексатом у пациентов, у которых монотерапия метотрексатом недостаточно эффективна. Однако у пациентов, получающих комбинированную терапию метотрексатом и лефлюномидом, увеличение концентрации печеночных ферментов наблюдается значительно чаше, чем на фоне монотерапии лефлюномидом.
Необходимо иметь в виду, что поскольку метаболизм лефлюномида зависит от печеночной энтероциркуляции, этот препарат имеет очень длительный период полувыведения и может задерживаться в организме более 2х лет. Для его элиминации рекомендуется использовать холестирамин. Противопоказаниями для использования лефлюномида являются заболевания печени, имунодефициты, применение римфапицина, вызывающего увеличение концентрации лефлюномида.
К числу эффективных препаратов для лечения РА относятся соли золота. D–пеницилламин и циклоспорин А в настоящее время применяются реже, в первую очередь из–за побочных эффектов. Например, на фоне D–пеницилламина описано развитие аутоимммунных синдромов (миастения гравис, синдром Гудпасчера, полимиозит).
Длительное применение циклоспорина А лимитируется развитием артериальной гипертензии и дозозависимого нарушения функции почек, которое иногда сохраняется после отмены препарата. Кроме того, многие препараты могут вызывать увеличение уровня циклоспорина А в сыворотке крови и таким образом способствовать нефротоксичности последнего. Поэтому циклосопорин А рекомендуется применять преимущественно у пациентов РА, которые «рефрактерны» к другим «базисным» препаратам.
Антицитокиновая терапия
Одно из наиболее ярких достижений фармакотерапии РА связано с разработкой принципиально новой группы лекарственных средств, которые получили название биологические агенты (biologic agents), механизм действия которых связан с подавлением синтеза провоспалительных цитокинов ФНОa и ИЛ1, играющих, как уже отмечалось, фундаментальную роль в иммунопатогенезе РА.
В настоящее время при лечении РА используют 3 группы препаратов, 2 из которых моноклональные антитела (мАТ) к ФНОa инфликсимаб (Ремикейд) и рекомбинантный растворимый ФНОa рецептор, соединенный с Fc фрагментом IgG (Etanercept) ингибируют синтез и биологические эффекты ФНОa и рекомбинантный растворимый антагонист ИЛ1 (Anakinra), подавляющий функциональную активность ИЛ1.
Источник
Статья посвящена ревматоидный артриту — клиническим ситуацииям и алгоритмам лечения

Ревматоидный артрит (РА) – хроническое системное иммуновоспалительное заболевание неизвестной этиологии, сопровождающееся развитием симметричного прогрессирующего эрозивно-деструктивного полиартрита и внесуставными проявлениями [1]. РА ассоциирован с высоким риском кардиоваскулярных событий, остеопоротических переломов, ранней инвалидизацией и преждевременной смертностью пациентов. Улучшить прогноз и исходы болезни способны только своевременная диагностика и раннее активное лечение больных РА.
Течение болезни складывается из нескольких последовательных стадий: ранней, развернутой и поздней, каждая из них имеет свои клинические особенности и подходы к терапии.
Базовые принципы терапии РА («Treat to target» или «Лечение до достижения цели») [2, 3]:
1. Достижение ремиссии (DAS28 (суммарный индекс (включает упрощенный счет из 28 суставов), позволяет многократно оценивать активность РА и может быть использован для контроля его активности в повседневной практике) <2,6) или как минимум низкой активности заболевания (DAS28 <3,2).
2. Ранняя активная терапия базисными противовоспалительными препаратами (БПВП), в первую очередь метотрексатом (МТ), не позднее первых 3 мес. от начала болезни.
3. Лечение должно быть максимально активным, с быстрой эскалацией дозы МТ и последующим изменением (при необходимости) схемы лечения в течение 3 мес. до достижения ремиссии (или низкой активности) болезни.
4. Тщательный контроль изменений активности заболевания и коррекция терапии не реже 1 раза в 3 мес. или ежемесячно у больных с высокой и умеренной активностью РА.
5. В случае недостаточной эффективности стандартной терапии БПВП показано назначение генно-инженерных биологических препаратов (ГИБП).
6. Определение тактики терапии должно быть согласовано с пациентом.
К факторам неблагоприятного прогноза (ФНП) у больных РА относятся [4]:
– молодой возраст;
– женский пол;
– высокие титры ревматоидного фактора (РФ) и/или антитела к циклическому цитруллиновому пептиду (АЦЦП);
– эрозивный процесс в суставах по данным рентгенографического исследования или магнитно-резонансной томографии (МРТ);
– повышение уровней острофазовых показателей: скорости оседания эритроцитов (СОЭ) или С-реактивного белка (СРБ);
– высокая активность заболевания согласно индексам DAS28, SDAI (Simplified Disease Activity Index) или CDAI (Clinical Disease Activity Index);
– внесуставные проявления (синдром Шегрена, поражение легких и т. д.).
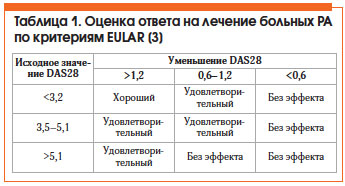
Оценка эффективности лечения РА по критериям Европейской антиревматической лиги (EULAR) представлена в таблице 1. Общепризнанным методом оценки активности РА является расчет индекса DAS28, который можно автоматически произвести на сайте www.das-score.nl.
Критерии эффективности терапии РА [5]:
• хороший клинический ответ (≈ ACR 70) (критерии Американской коллегии ревматологов);
• низкая активность болезни (DAS28 ≤ 3,2) или ремиссия (DAS28 ≤ 2,6);
• улучшение функции (HAQ (Health Assessment Questionare, опросник состояния здоровья, позволяющий оценить функциональные способности больных РА) <1,5) и качества жизни;
• предотвращение прогрессирования деструкции:
– замедление нарастания рентгенологических индексов (Sharp, Larsen);
– отсутствие появления новых эрозий;
– стабилизация или улучшение состояния по данным МРТ.
У пациентов, находящихся в состоянии ремиссии более 1 года после отмены глюкокортикостероидов (ГКС), следует рассмотреть вопрос о возможности прекращения лечения ГИБП, особенно если они применялись в комбинации с БПВП. Важное значение при определении тактики лечения имеет выбор пациентов.
Рассмотрим отдельные клинические ситуации и подходы к терапии при РА.
I. Пациент с впервые установленным ранним РА
Ранняя стадия РА – условно выделенная, клинико-патогенетическая стадия заболевания с длительностью активного синовита до 1 года, характеризуется преобладанием экссудативных изменений в пораженных суставах, частым атипичным течением и хорошим ответом на лечение. Выделение понятия «ранний РА» связано со сложившимися представлениями о патогенезе болезни и необходимости проведения ранней активной терапии РА. Ранний РА может дебютировать как недифференцированный артрит, что требует динамического наблюдения за больными и проведения тщательного дифференциально-диагностического поиска. На ранней стадии РА наиболее информативными являются диагностические критерии Американского и Европейского ревматологических сообществ, предложенные в 2010 г. (табл. 2).

Диагноз РА может быть установлен при общем счете не менее 6 баллов.
Доказано, что адекватная базисная терапия на ранней стадии РА позволяет предотвратить структурные повреждения, что способствует сохранению функциональной активности пациентов и улучшает отдаленный прогноз. БПВП необходимо назначать не позднее 3 мес. от начала РА с быстрой эскалацией дозы для достижения оптимального эффекта (DAS <2,4) и последующей заменой препарата в течение 3–6 мес. при его неэффективности [1]. Терапию БПВП следует продолжать даже при снижении активности заболевания и достижении ремиссии.
К БПВП первого ряда отнесены МТ, лефлуномид (ЛФ) и сульфасалазин (СС) (табл. 3), т. к. доказана их эффективность в отношении предотвращения деструктивных изменений суставов (уровень доказательности А). Препараты «второй линии» (гидроксихлорохин, препараты золота и др.) применяются при неэффективности препаратов первого ряда либо в комбинации с ними.
МТ – «золотой стандарт» терапии активного РА. При необходимости назначения МТ в дозе > 15 мг/нед. рекомендуется использовать парентеральный путь введения (в/м или п/к). Также с целью минимизации побочных явлений необходимо назначение фолиевой кислоты 1 мг/cут (5 мг/нед.), исключая дни приема МТ.

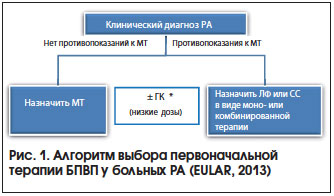
Основные стратегии лечения раннего РА (рис. 1) [7]:
1. Монотерапия МТ c последующей заменой на другие БПВП (ЛФ, СС) через 3–6 мес. в случае неэффективности или плохой переносимости).
2. Комбинированная базисная терапия, в т. ч. в сочетании с высокой дозой ГК. Используются комбинации БПВП как первого ряда (МТ + СС или МТ + ЛФ), так и второго ряда (МТ + Плаквенил) и т. д.
3. Комбинированная терапия синтетическими БПВП + ГИБП (в первую очередь ингибиторы фактора некроза опухоли (ФНО) при сохраняющейся > 3–6 мес. высокой активности РА, а также при наличии ФНП. Например, МТ 25 мг/нед. + Инфликсимаб 3 мг/кг массы тела.
II. Пациент с развернутым РА, не отвечающий на традиционные БПВП
Развернутая стадия РА – заболевание с отчетливо выраженной симптоматикой и длительностью болезни более 1 года. Суставной синдром имеет стойкий, симметричный и полиартикулярный характер с преимущественным поражением суставов кистей и стоп, выявляются признаки высокой или умеренной лабораторной активности, серопозитивность по РФ, эрозивный процесс в суставах по данным рентгенографии. Если диагноз устанавливается впервые, то стратегия ведения больного та же, что и при раннем РА. В случае уже проводившегося лечения с недостаточным эффектом или непереносимостью синтетических БПВП (как в виде монотерапии, так и при комбинированном их использовании), а также наличием ФНП прибегают к назначению ГИБП (рис. 2). Использование ГИБП позволяет максимально избирательно воздействовать на отдельные звенья иммунопатогенеза РА и существенно улучшить состояние больных РА, резистентных к стандартным БПВП и ГК [8]. Установлено, что комбинация традиционных БПВП с ГИБП более эффективна, чем монотерапия.
Назначение ГИБП показано:
– при длительно сохраняющейся (> 3–6 мес.) высокой активности РА;
– при высокой активности заболевания < 3 мес., только при наличии у больных ФНП.
Препаратами первого ряда среди ГИБП являются ингибиторы ФНО-α. Другие ГИБП назначаются больным РА с неадекватным ответом на блокаторы ФНО-α или при невозможности их применения (табл. 4).

Противопоказания к назначению ГИБП: отсутствие лечения одним или более БПВП (в первую очередь МТ) в полной терапевтической дозе; купирование обострений; тяжелые инфекционные заболевания (сепсис, септический артрит, пиелонефрит, остеомиелит, туберкулезная и грибковая инфекции, вирус иммунодефицита человека), злокачественные новообразования; беременность и лактация.
III. Пациент с поздним РА и остеопоротическими переломами
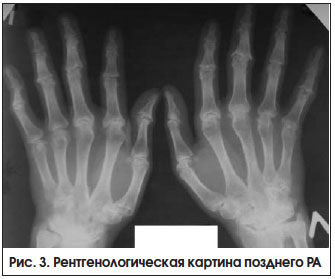
Поздняя стадия РА определяется как стадия необратимых структурных изменений (деформаций, подвывихов) суставов при длительности болезни > 2-х лет, с выраженными признаками активного воспаления или без них (рис. 3). Неуклонное прогрессирование болезни приводит к формированию различных видов подвывихов и контрактур суставов, в связи с чем возрастает роль реабилитационных и ортопедических мероприятий.
Развитие остеопороза (ОП) и ассоциированных с ним переломов является одним из наиболее тяжелых осложнений РА, определяющим неблагоприятное течение и прогноз болезни. Частота остеопоротических переломов среди больных РА в 1,5–2,5 раза выше, чем в общей популяции [9]. Предполагается, что развитие ОП и суставной деструкции при РА имеет единые патогенетические механизмы, в основе которых лежит цитокин-зависимая активация остеокластогенеза, приводящая к повышению костной резорбции [10]. Развитие ОП при РА определяется множеством общих и специфических, ассоциированных с заболеванием и лечением, факторов риска.
РА-ассоциированные факторы риска ОП и переломов [11]:
– активность воспалительного процесса,
– рентгенологическая стадия,
– тяжесть функциональных нарушений (HAQ > 1,25),
– длительность болезни,
– прием ГК,
– высокий риск падений.
У больных РА прием ГК в 4–5 раз повышает риск вертебральных переломов и удваивает риск переломов бедра. При этом доказано, что не существует безопасной дозы ГК. Также следует помнить, что развитие переломов у больных, получающих ГК, происходит при более высоких значениях минеральной плотности ткани (МПК), чем при первичном ОП, поэтому антиостеопоротическую терапию следует начинать при значениях Т-критерия < -1,5 стандартного отклонения от референсных значений.
Программа ведения больных РА и с остеопоротическими переломами включает контроль активности РА, коррекцию модифицируемых факторов риска ОП и переломов, предупреждение падений, антиостеопоротическую терапию, диету и физические упражнения. Всем больным РА необходимы проведение расчета абсолютного риска переломов (FRAX-алгоритм) (fracture risk assessment tool, 10-летний абсолютный риск перелома – инструмент оценки риска перелома ВОЗ) и профилактическое назначение препаратов кальция и витамина D. Назначение антиостеопоротической терапии без учета данных МПК проводится у пациентов в возрасте 65 лет и старше при наличии в анамнезе переломов при минимальной травме. Препаратами первой линии в лечении ОП у больных РА являются бисфосфонаты (БФ) и антитела к RANKL (лиганду рецептора активатора ядерного фактора каппа бета), обладающие антирезорбтивным действием (табл. 5). Привлекательность БФ при РА заключается еще и в том, что, по данным экспериментальных исследований, они могут оказывать благоприятное влияние на течение болезни. Установлено, что БФ способны ингибировать cинтез провоспалительных цитокинов и развитие костных эрозий при РА [12]. У пациентов с ранним артритом БФ в комбинации с МТ эффективно предотвращают развитие костной деструкции [13].

IV. Пожилой пациент с РА и НПВП-гастропатией
РА у лиц пожилого возраста характеризуется активным быстропрогрессирующим течением, высоким уровнем коморбидности и неблагоприятными исходами. Особое значение в структуре коморбидных состояний при РА имеют кардиоваскулярная и гастроинтестинальная патологии. По данным многочисленных исследований, сердечно-сосудистая заболеваемость и смертность у больных РА в 2–4 раза выше, чем в общей популяции, что диктует необходимость своевременного выявления и коррекции факторов кардиоваскулярного риска.
Рекомендации по снижению кардиоваскулярного риска у больных РА [14]:
• АСК следует принимать за ≥2 ч до приема нестероидных противовоcпалительных препаратов (НПВП).
• Не использовать НПВП в течение 3–6 мес. после острого сердечно-сосудистого события или процедуры.
• Регулярно контролировать артериальное давление.
• Использовать НПВП в низких дозах с коротким периодом полураспада (избегать назначения НПВП с пролонгированным высвобождением).
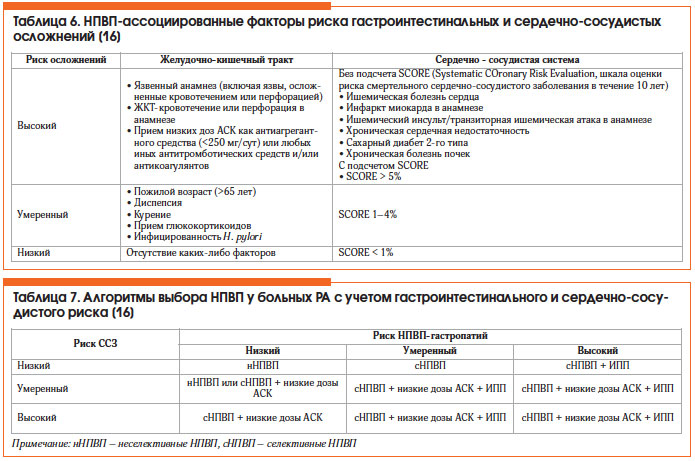
НПВП-гастропатия – одно из наиболее частых осложнений длительного приема НПВП, проявляющееся в виде эрозивного или язвенного поражения верхних отделов желудочно-кишечного тракта (ЖКТ) (преимущественно антральный и препилорический отделы желудка). Прием НПВП не влияет на прогрессирование РА, однако позволяет лучше контролировать симптомы заболевания на фоне терапии БПВП и ГИБП. НПВП-ассоциированные факторы риска гастроинтестинальных и сердечно-сосудистых осложнений представлены в таблице 6.
Экспертами EULAR разработан «калькулятор» для индивидуального подбора НПВП в зависимости от наличия факторов риска в отношении ЖКТ и сердечно-сосудистой системы [15]. К НПВП с наименьшим кардиоваскулярным риском отнесены напроксен, целекоксиб, кетопрофен, низкие дозы ибупрофена (<1200 мг/сут). Основные лекарственные средства, которые используют для лечения НПВП-индуцированных гастропатий, — ингибиторы протонной помпы (ИПП), Н2-блокаторы и мизопростол (синтетический аналог ПГ Е2). Алгоритмы выбора НПВП у больных РА с учетом гастроинтестинального и сердечно-сосудистого риска представлены в таблице 7 [16].
Не так давно появилась новая генерация НПВП, которые повышают активность оксида азота (NO) в слизистой желудка (NO-НПВП). Как известно, NO обладает гастропротективными свойствами: стимулирует секрецию слизи, бикарбоната, улучшает микроциркуляцию, ингибирует адгезию лейкоцитов к эндотелию, что и определяет фармакологические преимущества данной группы НПВП. Одним из представителей NO-НПВП является препарат Найзилат (амтолметин гуацил), который наряду с высокой анальгетической и противовоспалительной активностью обладает гастропротективными свойствами. В рандомизированных клинических исследованиях были продемонстрированы более низкие частота и тяжесть повреждений слизистой оболочки желудка после применения амтолметин гуацила по сравнению с таковыми других неселективных НПВП (диклофенак, индометацин, пироксикам), при сопоставимой противовоспалительной и анальгетической их эффективности [17]. Сравнительное исследование амтолметин гуацила 1200 мг/сут и целекоксиба 400 мг/сут у больных РА показало равнозначные эффективность и безопасность препаратов [18]. Терапевтическая доза амтолметин гуацила (Найзилат) составляет 600 мг 2 р./сут натощак, поддерживающая – 600 мг/сут.
Заключение
РА является гетерогенным заболеванием, исходы которого во многом определяются своевременной диагностикой болезни и правильно выбранной тактикой лечения. Ранняя стадия РА, особенно первые 3 мес. от начала заболевания, наиболее благоприятны для проведения эффективной базисной терапии. Основой ведения больных РА является тщательное мониторирование активности заболевания (не реже 1 р./3 мес.) с последующей коррекцией терапии при необходимости. Выбор терапии определяется стадией РА, активностью болезни, наличием ФНП, сосуществующими коморбидными состояниями, а также эффективностью предшествующего лечения.
Источник

