Ревматоидный артрит клинические рекомендации 2013
Ревматоидный артрит — серьезная болезнь, привлекающая внимание докторов разных стран. Отсутствие ясности причин возникновения, тяжесть протекания, сложность исцеления обуславливают важность кооперации докторов в изучении заболевания. Клинические рекомендации разрабатываются ассоциацией ревматологов с целью выработки единой схемы выявления недуга, разработки путей лечения, использования современных лекарств.
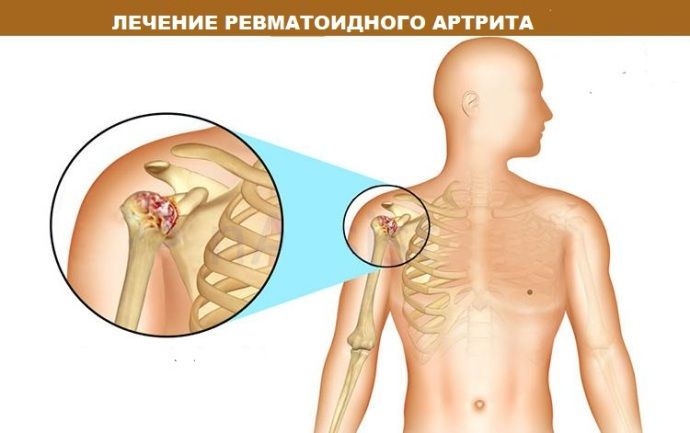
Классификация заболевания согласно клиническим рекомендациям
Ревматоидный артрит в условиях клинических рекомендаций описывается как хроническая болезнь. Недуг вызывает аутоиммунный ответ организма — яркое изменение защитной реакции, вызванное неясной причиной. Согласно МКБ 10 проявления ревматоидного артрита закодированы М05-М06 (относятся к классу воспалительных патологий).
Пациентов характеризует тяжелое патологическое состояние, которое протекает по-разному в разных стадиях. Клинические рекомендации рассматривают несколько периодов недуга:
- Сверхранний период (до полугода развития болезни).
- Ранний период (от полугода до года).
- Развернутый период (от года до двух).
- Поздний период (от двух лет существования болезни).
Раннее обнаружение заболевания повышает шансы на купирование патологического процесса. Медицинские сотрудники рекомендуют обращаться за помощью сразу после нахождения подозрительных негативных симптомов.
Клиника ревматоидного артрита отмечается следующими проявлениями:
- воспаление суставов (часто встречается поражение суставов кистей);
- ощущения скованности движений, особенно после пробуждения;
- повышенная температура;
- перманентная слабость;
- высокое потоотделение;
- снижение аппетита;
- появление подкожных узелков.
Отличительная черта заболевания — проявление симметричности воспаленных суставов. Например, воспаление на правой ноге сопровождается аналогичным поражением левой конечности. Обратитесь к доктору при симметричных поражениях немедленно!
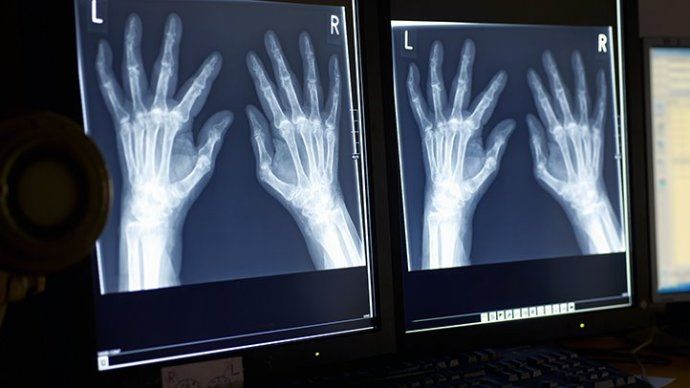
Обследования больных при помощи рентгена показывают наличие нескольких стадий:
- стадия № 1 проявляет небольшое понижение плотности костей в околосуставной сфере;
- стадия № 2 отмечает расширение поражения кости, возникновение просветов, начальные признаки деформации кости;
- стадия № 3 выявляет выраженный остеопороз, сопровождаемый яркими деформациями костной ткани, суставными вывихами;
- стадия № 4 высвечивает яркие поражения костей, нарушения соединения суставов, наросты на суставах.
Важное условие правильной классификации — профессионализм медицинских сотрудников. Опытный доктор верно классифицирует болезнь, выделит степень развития недуга, уточнит симптоматику.
Помните — недоверие к доктору затрудняет результативность излечения. При отсутствии контакта с медицинским работником стоит обратиться за исцелением к другому специалисту.
Основные принципы диагностики болезни
Поставить верное медицинское заключение достаточно сложно. Доктора руководствуются следующими принципами диагностики недуга:
- Уникальных характеристик болезни не существует. Не стоит ожидать специфических проявлений ревматоидного артрита. Важно осознавать — подозрения доктора обязательно стоит подтвердить достоверными исследованиями (например, рентгенографией, лабораторными методами).
- Окончательное медицинское заключение выносится доктором-ревматологом. Терапевт обязательно направляет пациента на ревматологическую консультацию при подозрительных симптомах (длительное ощущение скованности, наличие опухлости сферы сустава).
- При сомнениях стоит проводить консилиум специалистов, помогающий поставить верное медицинское заключение.
- Важно помнить о необходимости анализа возможности проявления иных болезней. Доктору необходимо изучить все вероятные недуги, обладающие сходным проявлением симптоматики.
Важно! При воспалении сустава не ждите изменений в других суставах! Не затягивайте с обращением к доктору, теряя время. Раннее обращение (желательно до полугода болезни) предоставит шанс на полное сохранение качества жизни больных.
Дифференциальная диагностика патологии, основанная на клинических рекомендациях
Диагностирование доктором ревматоидного артрита по клиническим рекомендациям проводится комплексно по нескольким направлениям. Базой постановки медицинского заключения служат классификационные критерии, описанные в клинических рекомендациях. При осмотре доктора настораживают следующие симптомы:
- больной жалуется на разнообразные боли в суставной области;
- больным свойственна утренняя скованность (около получаса пациентам сложно двигать суставами);
- пораженные области отличаются припухлостью;
- воспалительный процесс беспокоит пациента не менее двух недель.
Поражения суставов сотрудники оценивают по пятибалльной системе. Единица выставляется в ситуации воспаления от 2 до 10 крупных суставов, максимальные 5 баллов получает пациент с множеством воспаленных суставов (не менее 10 крупных суставов, как минимум один мелкий).
Помните — заболевание поражает неспешно. Развитие недуга характеризуется замедленным нарастанием боли в течение нескольких месяцев. Больных радует отсутствие ярких симптомов, но данный симптом — тревожный сигнал для доктора. Обязательно отслеживайте интенсивность негативных симптомов, частоту проявления болей, силу болезненных ощущений.
Инструментальная диагностика позволяет уточнить медицинское заключение, проводя следующие процедуры:
- Рентгенография позволяет увидеть изменения в сфере суставов. Доктор рассматривает состояние суставных щелей, анализирует наличие суставных вывихов (подвывихов), изучает плотность костей, видит кисты, диагностирует наличие эрозийного поражения. Исследования применяют для первичного анализа недуга. Далее больным рекомендуется ежегодно повторять данную процедуру обследования.
- Магнитно-резонансная томография более чувствительна в сравнении с проведением рентгена. Посредством МРТ выявляются воспалительные процессы в сфере синовиальных оболочек, эрозийные поражения костей, поражения соединительных тканей (окружающих суставы).
- Ультразвуковая диагностика позволяет разглядеть патологические изменения в сфере суставов. Медицинский сотрудник способен увидеть эрозии, пораженные участки соединительных тканей, разрастание синовиальной оболочки, наличие патологических выпотов (места скопления жидкости). Результаты ультразвуковой диагностики демонстрируют границы пораженной области, позволяют отследить интенсивность воспаления.
Инструментальные обследования дополняют диагноз. Однако по результатам данной диагностики неправомерно выставлять медицинское заключение. Наличие болезни обязательно должно подтвердиться лабораторными исследованиями!
Большое значение для верного медицинского заключение имеют лабораторные методы:
- Анализ крови на антитела в отношении цитруллинированного циклического пептида (АЦЦП). Данный метод позволяет продиагностировать заболевания на начальной ступени. Анализ АЦЦП позволяет подтвердить медицинское заключение, выделить форму заболевания, проанализировать течение. Посредством анализа медицинские сотрудники предсказывают скорость прогресса болезни. В норме содержание специфичных антител не превышает 20 МЕ/мл. Повышенные показатели — повод для беспокойства. Зачастую положительные результаты анализа опережают проявление негативных симптомов.
- Тест на обладание ревматоидным фактором помогает диагностировать недуг. При отсутствии болезни показатели нулевые либо не выше 14 МЕ/мл (показатели едины для несовершеннолетних, взрослых, пожилых).
- Исследования на наличие вирусов в организме (тесты на ВИЧ-инфекцию, на различные виды гепатитов).
Анализы АЦЦП и тест на наличие ревматоидного фактора берутся из вены пациента. Рекомендуется обращаться в лабораторию утром, не есть перед сдачей анализов. За сутки до посещения лаборантов недопустимо есть жирную пищу, копченую продукцию. Сыворотка крови способна свернуться, лишив пациента правильных результатов.
Современные тенденции лечения заболевания
Услышав о неизлечимости заболевания, больные чувствуют опустошенность, тревогу, безнадежность. Поддаваться депрессии не стоит — медицинские сотрудники помогут одолеть недуг. Традиционно хронический ревматоидный артрит усмиряют посредством комплексного лечения:
- Базисные противовоспалительные препараты помогают купировать воспалительные процессы у больных. Среди лекарств данной категории популярны таблетки Метотрексата. При недостаточной переносимости доктора назначают Лефлуномид. Также допустимо лечение Сульфасалазином. Пациенты оставляют о результативности препаратов золота положительные отзывы.
- Нестероидные противовоспалительные препараты существенно облегчают самочувствие больных за счет снижения болевых ощущений. Активно помогают больным Ибупрофен, Кетонал, Диклоберл. Тяжелые ситуации заболевания требуют выписки Кеторолака. Доктор рассматривает каждую ситуацию индивидуально, выбирая оптимальное сочетание лекарственных средств, подходящее определенному больному.
- Глюкокортикоиды способствуют подавлению атипичных реакций организма, позволяя погасить симптомы болезни. Активно используются Дексаметазон, Преднизон. Гормональную терапию с особой осторожностью используют при излечении несовершеннолетних, опасаясь нарушить развитие детских организмов. Взрослым пациентам препараты данного ряда выписываются в ситуациях подтверждения отсутствия результатов от предыдущего лечения.
Самое сложное в лечении недуга — подбор эффективных лекарственных средств. Предсказать воздействие препарата на конкретного пациента нельзя. Доктора вынуждены наблюдать за действием лекарства около трех месяцев (минимальное время составляет около месяца). Отсутствие ожидаемого результата вынуждает изменить дозу лекарственных средств либо полностью сменить препарат.
Новым методом в ревматологии признается использование генной инженерии. Данная группа препаратов представляет генно-инженерные разработки, подавляющие атипичные реакции организма.
Надежду на выздоровление больных придают инъекции инфликсимаба. Ремикейд — единственный препарат, содержащий данное вещество. Инфликсимад — синтез человеческого и мышиного ДНК, позволяющий связаться с негативными факторами, нейтрализовать иммунные ответы, погасить атипичные реакции. Конечный результат — устранение ревматоидного артрита. Явные преимущества препарата Ремикейд:
- быстрый эффект (наступают явные улучшения через пару дней);
- высокая результативность (погашение механизма развития недуга);
- длительность позитивных результатов (на несколько лет пациенты забывают о неприятном диагнозе);
- эффективность даже при запущенных ситуациях.
Недостатки применения инфликсимаба в комплексном лечении ревматоидного артрита:
- Необходимость нахождения под капельницами (лекарство вводится курсом).
- Разнообразие побочных действий (вероятность возникновения тошноты, болей головы, нарушений деятельности сердца, аллергических проявлений, иных негативных реакций).
- Крайне высокая цена (за 100 миллиграмм препарата пациентам придется заплатить около 400 долларов).
Отсутствие денежных средств для излечения — не повод грустить. Проводя эксперименты, медицинские сотрудники предлагают пациентам бесплатно излечиться. Существуют возможности попадания в экспериментальные группы, принятия участия в тестировании новых лекарств. Важно следить за новостями, активно изучать современные форумы, подавать заявки для пробных исследований.
Биологические лекарственные средства — еще одна новинка в сфере борьбы с недугом. Основное действие лекарства обусловлено установлением специфических связей с молекулами белка, подавляющих атипичные реакции организма. Клинические рекомендации по ревматоидному артриту выдвигают предложение использовать новые биологические препараты для излечения болезни. Среди данной группы лекарственных средств выделяются:
- Хумира включает активный ингредиент адалимумаб, останавливающий фактор некроза опухоли. Взрослым пациентам препарат вкалывают в сферу живота, бедра;
- Кинерет (анакинра) используется подкожно, осуществляя блокировку интерлейкин-1 –белка;
- Этанерцепт стимулирует воспроизведение лейкоцитов. Лекарство колют подкожно взрослым, несовершеннолетним, пожилым пациентам.
Использование сразу нескольких биологических лекарств — большая ошибка. Недопустимо считать препараты безвредными, смешивать разные виды, назначать самостоятельное лечение. Лечитесь только под контролем медицинских сотрудников!
Ревматоидный артрит — крайне сложный недуг, требующий тщательного лечения. Окончательное исцеление невозможно, но современные клинические рекомендации позволяют потушить проявления заболевания, минимизировать негативные последствия, позволить пациентам радоваться жизни.
Источник
Статья посвящена ревматоидный артриту — клиническим ситуацииям и алгоритмам лечения

Ревматоидный артрит (РА) – хроническое системное иммуновоспалительное заболевание неизвестной этиологии, сопровождающееся развитием симметричного прогрессирующего эрозивно-деструктивного полиартрита и внесуставными проявлениями [1]. РА ассоциирован с высоким риском кардиоваскулярных событий, остеопоротических переломов, ранней инвалидизацией и преждевременной смертностью пациентов. Улучшить прогноз и исходы болезни способны только своевременная диагностика и раннее активное лечение больных РА.
Течение болезни складывается из нескольких последовательных стадий: ранней, развернутой и поздней, каждая из них имеет свои клинические особенности и подходы к терапии.
Базовые принципы терапии РА («Treat to target» или «Лечение до достижения цели») [2, 3]:
1. Достижение ремиссии (DAS28 (суммарный индекс (включает упрощенный счет из 28 суставов), позволяет многократно оценивать активность РА и может быть использован для контроля его активности в повседневной практике) <2,6) или как минимум низкой активности заболевания (DAS28 <3,2).
2. Ранняя активная терапия базисными противовоспалительными препаратами (БПВП), в первую очередь метотрексатом (МТ), не позднее первых 3 мес. от начала болезни.
3. Лечение должно быть максимально активным, с быстрой эскалацией дозы МТ и последующим изменением (при необходимости) схемы лечения в течение 3 мес. до достижения ремиссии (или низкой активности) болезни.
4. Тщательный контроль изменений активности заболевания и коррекция терапии не реже 1 раза в 3 мес. или ежемесячно у больных с высокой и умеренной активностью РА.
5. В случае недостаточной эффективности стандартной терапии БПВП показано назначение генно-инженерных биологических препаратов (ГИБП).
6. Определение тактики терапии должно быть согласовано с пациентом.
К факторам неблагоприятного прогноза (ФНП) у больных РА относятся [4]:
– молодой возраст;
– женский пол;
– высокие титры ревматоидного фактора (РФ) и/или антитела к циклическому цитруллиновому пептиду (АЦЦП);
– эрозивный процесс в суставах по данным рентгенографического исследования или магнитно-резонансной томографии (МРТ);
– повышение уровней острофазовых показателей: скорости оседания эритроцитов (СОЭ) или С-реактивного белка (СРБ);
– высокая активность заболевания согласно индексам DAS28, SDAI (Simplified Disease Activity Index) или CDAI (Clinical Disease Activity Index);
– внесуставные проявления (синдром Шегрена, поражение легких и т. д.).
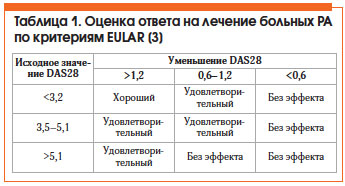
Оценка эффективности лечения РА по критериям Европейской антиревматической лиги (EULAR) представлена в таблице 1. Общепризнанным методом оценки активности РА является расчет индекса DAS28, который можно автоматически произвести на сайте www.das-score.nl.
Критерии эффективности терапии РА [5]:
• хороший клинический ответ (≈ ACR 70) (критерии Американской коллегии ревматологов);
• низкая активность болезни (DAS28 ≤ 3,2) или ремиссия (DAS28 ≤ 2,6);
• улучшение функции (HAQ (Health Assessment Questionare, опросник состояния здоровья, позволяющий оценить функциональные способности больных РА) <1,5) и качества жизни;
• предотвращение прогрессирования деструкции:
– замедление нарастания рентгенологических индексов (Sharp, Larsen);
– отсутствие появления новых эрозий;
– стабилизация или улучшение состояния по данным МРТ.
У пациентов, находящихся в состоянии ремиссии более 1 года после отмены глюкокортикостероидов (ГКС), следует рассмотреть вопрос о возможности прекращения лечения ГИБП, особенно если они применялись в комбинации с БПВП. Важное значение при определении тактики лечения имеет выбор пациентов.
Рассмотрим отдельные клинические ситуации и подходы к терапии при РА.
I. Пациент с впервые установленным ранним РА
Ранняя стадия РА – условно выделенная, клинико-патогенетическая стадия заболевания с длительностью активного синовита до 1 года, характеризуется преобладанием экссудативных изменений в пораженных суставах, частым атипичным течением и хорошим ответом на лечение. Выделение понятия «ранний РА» связано со сложившимися представлениями о патогенезе болезни и необходимости проведения ранней активной терапии РА. Ранний РА может дебютировать как недифференцированный артрит, что требует динамического наблюдения за больными и проведения тщательного дифференциально-диагностического поиска. На ранней стадии РА наиболее информативными являются диагностические критерии Американского и Европейского ревматологических сообществ, предложенные в 2010 г. (табл. 2).

Диагноз РА может быть установлен при общем счете не менее 6 баллов.
Доказано, что адекватная базисная терапия на ранней стадии РА позволяет предотвратить структурные повреждения, что способствует сохранению функциональной активности пациентов и улучшает отдаленный прогноз. БПВП необходимо назначать не позднее 3 мес. от начала РА с быстрой эскалацией дозы для достижения оптимального эффекта (DAS <2,4) и последующей заменой препарата в течение 3–6 мес. при его неэффективности [1]. Терапию БПВП следует продолжать даже при снижении активности заболевания и достижении ремиссии.
К БПВП первого ряда отнесены МТ, лефлуномид (ЛФ) и сульфасалазин (СС) (табл. 3), т. к. доказана их эффективность в отношении предотвращения деструктивных изменений суставов (уровень доказательности А). Препараты «второй линии» (гидроксихлорохин, препараты золота и др.) применяются при неэффективности препаратов первого ряда либо в комбинации с ними.
МТ – «золотой стандарт» терапии активного РА. При необходимости назначения МТ в дозе > 15 мг/нед. рекомендуется использовать парентеральный путь введения (в/м или п/к). Также с целью минимизации побочных явлений необходимо назначение фолиевой кислоты 1 мг/cут (5 мг/нед.), исключая дни приема МТ.

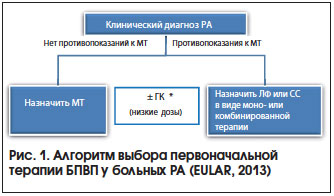
Основные стратегии лечения раннего РА (рис. 1) [7]:
1. Монотерапия МТ c последующей заменой на другие БПВП (ЛФ, СС) через 3–6 мес. в случае неэффективности или плохой переносимости).
2. Комбинированная базисная терапия, в т. ч. в сочетании с высокой дозой ГК. Используются комбинации БПВП как первого ряда (МТ + СС или МТ + ЛФ), так и второго ряда (МТ + Плаквенил) и т. д.
3. Комбинированная терапия синтетическими БПВП + ГИБП (в первую очередь ингибиторы фактора некроза опухоли (ФНО) при сохраняющейся > 3–6 мес. высокой активности РА, а также при наличии ФНП. Например, МТ 25 мг/нед. + Инфликсимаб 3 мг/кг массы тела.
II. Пациент с развернутым РА, не отвечающий на традиционные БПВП
Развернутая стадия РА – заболевание с отчетливо выраженной симптоматикой и длительностью болезни более 1 года. Суставной синдром имеет стойкий, симметричный и полиартикулярный характер с преимущественным поражением суставов кистей и стоп, выявляются признаки высокой или умеренной лабораторной активности, серопозитивность по РФ, эрозивный процесс в суставах по данным рентгенографии. Если диагноз устанавливается впервые, то стратегия ведения больного та же, что и при раннем РА. В случае уже проводившегося лечения с недостаточным эффектом или непереносимостью синтетических БПВП (как в виде монотерапии, так и при комбинированном их использовании), а также наличием ФНП прибегают к назначению ГИБП (рис. 2). Использование ГИБП позволяет максимально избирательно воздействовать на отдельные звенья иммунопатогенеза РА и существенно улучшить состояние больных РА, резистентных к стандартным БПВП и ГК [8]. Установлено, что комбинация традиционных БПВП с ГИБП более эффективна, чем монотерапия.
Назначение ГИБП показано:
– при длительно сохраняющейся (> 3–6 мес.) высокой активности РА;
– при высокой активности заболевания < 3 мес., только при наличии у больных ФНП.
Препаратами первого ряда среди ГИБП являются ингибиторы ФНО-α. Другие ГИБП назначаются больным РА с неадекватным ответом на блокаторы ФНО-α или при невозможности их применения (табл. 4).

Противопоказания к назначению ГИБП: отсутствие лечения одним или более БПВП (в первую очередь МТ) в полной терапевтической дозе; купирование обострений; тяжелые инфекционные заболевания (сепсис, септический артрит, пиелонефрит, остеомиелит, туберкулезная и грибковая инфекции, вирус иммунодефицита человека), злокачественные новообразования; беременность и лактация.
III. Пациент с поздним РА и остеопоротическими переломами
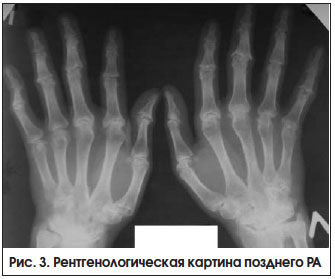
Поздняя стадия РА определяется как стадия необратимых структурных изменений (деформаций, подвывихов) суставов при длительности болезни > 2-х лет, с выраженными признаками активного воспаления или без них (рис. 3). Неуклонное прогрессирование болезни приводит к формированию различных видов подвывихов и контрактур суставов, в связи с чем возрастает роль реабилитационных и ортопедических мероприятий.
Развитие остеопороза (ОП) и ассоциированных с ним переломов является одним из наиболее тяжелых осложнений РА, определяющим неблагоприятное течение и прогноз болезни. Частота остеопоротических переломов среди больных РА в 1,5–2,5 раза выше, чем в общей популяции [9]. Предполагается, что развитие ОП и суставной деструкции при РА имеет единые патогенетические механизмы, в основе которых лежит цитокин-зависимая активация остеокластогенеза, приводящая к повышению костной резорбции [10]. Развитие ОП при РА определяется множеством общих и специфических, ассоциированных с заболеванием и лечением, факторов риска.
РА-ассоциированные факторы риска ОП и переломов [11]:
– активность воспалительного процесса,
– рентгенологическая стадия,
– тяжесть функциональных нарушений (HAQ > 1,25),
– длительность болезни,
– прием ГК,
– высокий риск падений.
У больных РА прием ГК в 4–5 раз повышает риск вертебральных переломов и удваивает риск переломов бедра. При этом доказано, что не существует безопасной дозы ГК. Также следует помнить, что развитие переломов у больных, получающих ГК, происходит при более высоких значениях минеральной плотности ткани (МПК), чем при первичном ОП, поэтому антиостеопоротическую терапию следует начинать при значениях Т-критерия < -1,5 стандартного отклонения от референсных значений.
Программа ведения больных РА и с остеопоротическими переломами включает контроль активности РА, коррекцию модифицируемых факторов риска ОП и переломов, предупреждение падений, антиостеопоротическую терапию, диету и физические упражнения. Всем больным РА необходимы проведение расчета абсолютного риска переломов (FRAX-алгоритм) (fracture risk assessment tool, 10-летний абсолютный риск перелома – инструмент оценки риска перелома ВОЗ) и профилактическое назначение препаратов кальция и витамина D. Назначение антиостеопоротической терапии без учета данных МПК проводится у пациентов в возрасте 65 лет и старше при наличии в анамнезе переломов при минимальной травме. Препаратами первой линии в лечении ОП у больных РА являются бисфосфонаты (БФ) и антитела к RANKL (лиганду рецептора активатора ядерного фактора каппа бета), обладающие антирезорбтивным действием (табл. 5). Привлекательность БФ при РА заключается еще и в том, что, по данным экспериментальных исследований, они могут оказывать благоприятное влияние на течение болезни. Установлено, что БФ способны ингибировать cинтез провоспалительных цитокинов и развитие костных эрозий при РА [12]. У пациентов с ранним артритом БФ в комбинации с МТ эффективно предотвращают развитие костной деструкции [13].

IV. Пожилой пациент с РА и НПВП-гастропатией
РА у лиц пожилого возраста характеризуется активным быстропрогрессирующим течением, высоким уровнем коморбидности и неблагоприятными исходами. Особое значение в структуре коморбидных состояний при РА имеют кардиоваскулярная и гастроинтестинальная патологии. По данным многочисленных исследований, сердечно-сосудистая заболеваемость и смертность у больных РА в 2–4 раза выше, чем в общей популяции, что диктует необходимость своевременного выявления и коррекции факторов кардиоваскулярного риска.
Рекомендации по снижению кардиоваскулярного риска у больных РА [14]:
• АСК следует принимать за ≥2 ч до приема нестероидных противовоcпалительных препаратов (НПВП).
• Не использовать НПВП в течение 3–6 мес. после острого сердечно-сосудистого события или процедуры.
• Регулярно контролировать артериальное давление.
• Использовать НПВП в низких дозах с коротким периодом полураспада (избегать назначения НПВП с пролонгированным высвобождением).
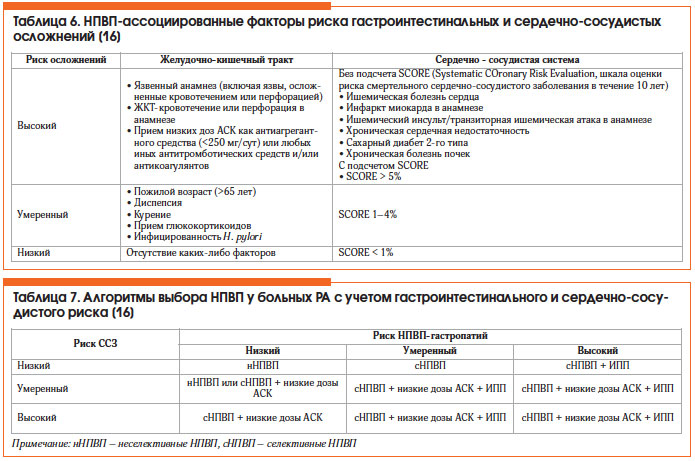
НПВП-гастропатия – одно из наиболее частых осложнений длительного приема НПВП, проявляющееся в виде эрозивного или язвенного поражения верхних отделов желудочно-кишечного тракта (ЖКТ) (преимущественно антральный и препилорический отделы желудка). Прием НПВП не влияет на прогрессирование РА, однако позволяет лучше контролировать симптомы заболевания на фоне терапии БПВП и ГИБП. НПВП-ассоциированные факторы риска гастроинтестинальных и сердечно-сосудистых осложнений представлены в таблице 6.
Экспертами EULAR разработан «калькулятор» для индивидуального подбора НПВП в зависимости от наличия факторов риска в отношении ЖКТ и сердечно-сосудистой системы [15]. К НПВП с наименьшим кардиоваскулярным риском отнесены напроксен, целекоксиб, кетопрофен, низкие дозы ибупрофена (<1200 мг/сут). Основные лекарственные средства, которые используют для лечения НПВП-индуцированных гастропатий, — ингибиторы протонной помпы (ИПП), Н2-блокаторы и мизопростол (синтетический аналог ПГ Е2). Алгоритмы выбора НПВП у больных РА с учетом гастроинтестинального и сердечно-сосудистого риска представлены в таблице 7 [16].
Не так давно появилась новая генерация НПВП, которые повышают активность оксида азота (NO) в слизистой желудка (NO-НПВП). Как известно, NO обладает гастропротективными свойствами: стимулирует секрецию слизи, бикарбоната, улучшает микроциркуляцию, ингибирует адгезию лейкоцитов к эндотелию, что и определяет фармакологические преимущества данной группы НПВП. Одним из представителей NO-НПВП является препарат Найзилат (амтолметин гуацил), который наряду с высокой анальгетической и противовоспалительной активностью обладает гастропротективными свойствами. В рандомизированных клинических исследованиях были продемонстрированы более низкие частота и тяжесть повреждений слизистой оболочки желудка после применения амтолметин гуацила по сравнению с таковыми других неселективных НПВП (диклофенак, индометацин, пироксикам), при сопоставимой противовоспалительной и анальгетической их эффективности [17]. Сравнительное исследование амтолметин гуацила 1200 мг/сут и целекоксиба 400 мг/сут у больных РА показало равнозначные эффективность и безопасность препаратов [18]. Терапевтическая доза амтолметин гуацила (Найзилат) составляет 600 мг 2 р./сут натощак, поддерживающая – 600 мг/сут.
Заключение
РА является гетерогенным заболеванием, исходы которого во многом определяются своевременной диагностикой болезни и правильно выбранной тактикой лечения. Ранняя стадия РА, особенно первые 3 мес. от начала заболевания, наиболее благоприятны для проведения эффективной базисной терапии. Основой ведения больных РА является тщательное мониторирование активности заболевания (не реже 1 р./3 мес.) с последующей коррекцией терапии при необходимости. Выбор терапии определяется стадией РА, активностью болезни, наличием ФНП, сосуществующими коморбидными состояниями, а также эффективностью предшествующего лечения.
Источник


