Вторичный остеоартроз при ревматоидном артрите
Роза Исмаиловна Ягудина, д. фарм. н., проф., зав. кафедрой организации лекарственного обеспечения и фармакоэкономики и зав. лабораторией фармакоэкономических исследований Первого МГМУ им. И. М. Сеченова.
Евгения Евгеньевна Аринина, к. м. н., ведущий научный сотрудник лаборатории фармакоэкономических исследований Первого МГМУ им. И. М. Сеченова.
Поражения суставов широко распространены во всех возрастных группах, особенно в старшей. Причиной артралгий могут быть разные заболевания, дифференцировать которые иногда бывает достаточно трудно. Сегодня мы поговорим о двух наиболее распространенных патологиях суставов, а именно об остеоартрозе суставов и ревматоидном артрите.
Этиология и течение остеоартроза
Остеоартроз (ОА) — хроническое дегенеративно-дистрофическое заболевание суставов, в основе которого лежит нарушение процессов синтеза и деградации матрикса суставного хряща, при этом в патологический процесс, как правило, вовлекаются все структуры сустава. Причин развития остеоартроза несколько. Наиболее частая — механическое повреждение суставных поверхностей, связанное с длительной статической нагрузкой на сустав, а также нарушение региональной гемодинамики. Наиболее значимые факторы риска для развития остеоартроза (ОА) — это женский пол и пожилой возраст больных. Также в группе риска оказываются спортсмены, люди с ожирением, и те, чья деятельность связана с длительным пребыванием на ногах.
Различают первичный (идиопатический) и вторичный ОА. Этиология первичного ОА до настоящего времени неизвестна. Причинами вторичного ОА являются дисплазия суставов и костей, травмы, метаболические заболевания (охроноз, гемохроматоз, подагра и др.), эндокринные (гипотиреоз, акромегалия и др.) и другие факторы.
Поражение суставов при ОА бывает локальным (менее трех различных суставных групп) и генерализованным (более трех суставных групп). Генерализованный ОА чаще встречается у женщин и передается по наследству.
Охроноз (алкаптонурия) — наследственное заболевание, обусловленное избыточным отложением в различных тканях гомогентизиновой кислоты в связи с отсутствием фермента гомогентизиназы.
Компенсированная стадия ОА может долго протекать без клинических проявлений и выявляться только при рентгенографическом исследовании суставов. Как правило, данная форма наблюдается более чем у 80 % людей в возрасте старше 60 лет. Однако в определенных стадиях ОА возникают клинические проявления.
Основные симптомы остеоартроза:
- боль в суставах (стартовая боль);
- ограничение движений;
- утренняя скованность (до 30 мин.);
- крепитация (хруст) в суставах при движении;
- болезненность при пальпации;
- дефигурация или деформация суставов;
- неустойчивость/нестабильность сустава;
- нарушение функции суставов.
Ведущий клинический симптом при ОА — боль в суставе, источником которой могут быть: синовиальная оболочка, капсула сустава, периартикулярные связки и мышцы, надкостница и субхондральная кость. При ОА боль носит неоднородный характер и является одним из ранних симптомов болезни. Заболевание может сопровождаться утренней скованностью, припухлостью сустава, локальным повышением температуры. Присоединяющийся синовит усугубляет течение болезни. Постепенно развиваются деформация и тугоподвижность суставов.
Наиболее инвалидизирующими формами заболевания являются гонартроз (поражение коленного сустава) и коксартроз (артроз тазобедренного сустава). Третья по значимости локализация — артроз дистальных и проксимальных межфаланговых суставов кисти (узелки Гебердена и Бушара).
Лечение остеоартроза
Лечение больных остеоартрозом включает различные комбинации медикаментозных и немедикаментозных методов. Терапевтическая тактика направлена на решение следующих задач:
- механическая разгрузка пораженных суставов;
- купирование синовита и болевого синдрома;
- профилактика прогрессирования заболевания.
К немедикаментозным методам лечения ОА относятся: ЛФК, плавание, коррекция массы тела, использование ортезов (наколенников, ортопедических стелек и др.), физиотерапия, иглорефлексотерапия, массаж, бальнеотерапия (сульфидные, радоновые ванны и т. д.). При недостаточной эффективности этих мероприятий назначается лекарственная терапия.
Препараты от остеоартроза, применяемые в лечении, можно разделить на 3 группы:
1. Симптоматические препараты для лечения суставов быстрого действия:
- анальгетики. Парацетамол — препарат первого выбора для купирования болевого синдрома при ОА.
- нестероидные противовоспалительные средства (НПВС) — кеторолак, нимесулид, напроксен и др. Показаны пациентам, не ответившим на терапию парацетамолом. Препараты назначают перорально, а также парентерально или местно в виде мазей, кремов, гелей (подробнее об этом можно прочитать в статье «Боли в спине»).
- опиоидные анальгетики (трамадол). Применяются в течение короткого периода при неэффективности и/или плохой переносимости НПВП.
2. Симптоматические препараты замедленного действия:
- диацереин, гиалуроновая кислота, неомыляемые соединения авокадо и сои. Эти препараты способствуют уменьшению болей в суставах, позволяют снизить дозу НПВС и хорошо переносятся. Обезболивающий эффект сохраняется в течение нескольких месяцев после завершения лечения.
3. ЛС, модифицирующие структуру хряща:
- хондроитин сульфат, глюкозамин сульфат. Глюкозамин сульфат принимает участие в синтезе мукополисахаридов, введение препарата стимулирует синтез в хряще гликозаминагликанов и протеогликанов. Хондроитин сульфат — компонент матрикса суставного хряща, который проникает в структуры матрикса и оказывает влияние на метаболические процессы.
- дериваты гиалуроновой кислоты для внутрисуставного введения. Оказывают пролонгированное симптомомодифицирующее (анальгетическое) действие, а также улучшают подвижность суставов благодаря эффекту смазки и стимуляции выработки собственной гиалуроновой кислоты синовиальными клетками.
Если при ОА развивается реактивный синовит, рекомендуется внутрисуставное введение пролонгированных глюкокортикостероидов (гидрокортизон, триамцинолон, метилпреднизолон и др.)
Также можно отметить еще не вошедшие в широкую клиническую практику структурно-модифицирующие препараты, содержащие глюкозамин сульфат, ингибиторы матриксных металлопротеиназ, ингибиторы фермента конвертазы интерлейкина 1b и катепсина К.
Этиология и течение ревматоидного артрита
Ревматоидный артрит (РА) — хроническое аутоиммунное заболевание с преимущественным поражением периферических суставов по типу эрозивно-деструктивного артрита.
В качестве этиологических факторов рассматривают стрептококки группы А и В, микоплазмы, вирусы (Эпштейна — Барр, цитомегаловирус, ретровирусы и др.), интоксикации и т. д. Заболевание развивается у людей, имеющих генетическую предрасположенность к РА, и чаще встречается у женщин среднего и пожилого возраста.
В основе развития РА лежит генерализованный дефект иммунных механизмов, которые регулируют клеточные и гуморальные реакции, что приводит к хроническому прогрессирующему воспалению, которое затрагивает не только суставы, но и внутренние органы.
Основным проявлением РА является стойкий артрит мелких суставов кистей и стоп. Для РА характерно ощущение утренней скованности, симметричность поражения, боль, припухлость суставов, повышение температуры кожи в области сустава. В большинстве случаев РА развивается постепенно, отличается волнообразным течением и медленным прогрессированием суставного синдрома. Клиническая картина при РА — деформация пястно-фаланговых (сгибательные контрактуры, подвывихи), проксимальных межфаланговых, лучезапястных суставов с отклонением кисти во внешнюю сторону, а также плюснефаланговых суставов. К внесуставным проявлениям ревматоидного артрита относятся: подкожные (ревматоидные) узелки в области локтевого сустава, серозиты (плеврит и перикардит), лимфаденопатия, периферическая нейропатия, кожный васкулит и др. У 70–80 % больных в сыворотке крови выявляют ревматоидный фактор (РФ), такой РА называют серопозитивным.
Выделяют несколько степеней активности ревматоидного артрита:
а)Степень 0 — неактивный ревматоидный артрит. Боли в суставах отсутствуют. Температура, СОЭ, содержание С-реактивного белка и другие показатели в норме.
б) Степень I — минимальная активность. Умеренные боли в суставах и небольшая скованность по утрам. СОЭ и показатели С-реактивного белка несколько повышены.
в) Степень II — средняя активность. Боли в суставах не только при движении, но и в покое. Экссудативные явления (припухлость, выпот, бурсит) и выраженное ограничение подвижности в суставах. Субфебрильная температура, СОЭ 30–40 мм/ч, значительное увеличение уровня С-реактивного белка.
г) Степень III — высокая активность. Выраженная утренняя скованность, сильные боли в покое, выраженные экссудативные явления в суставах (припухлость, гиперемия и повышение температуры кожи над суставами), выраженное ограничение подвижности. Признаки активного воспалительного процесса во внутренних органах (плеврит, перикардит, миокардит). Температура тела высокая. Значительное повышение СОЭ (40–60 мм/ч) и показателей С-реактивного белка.
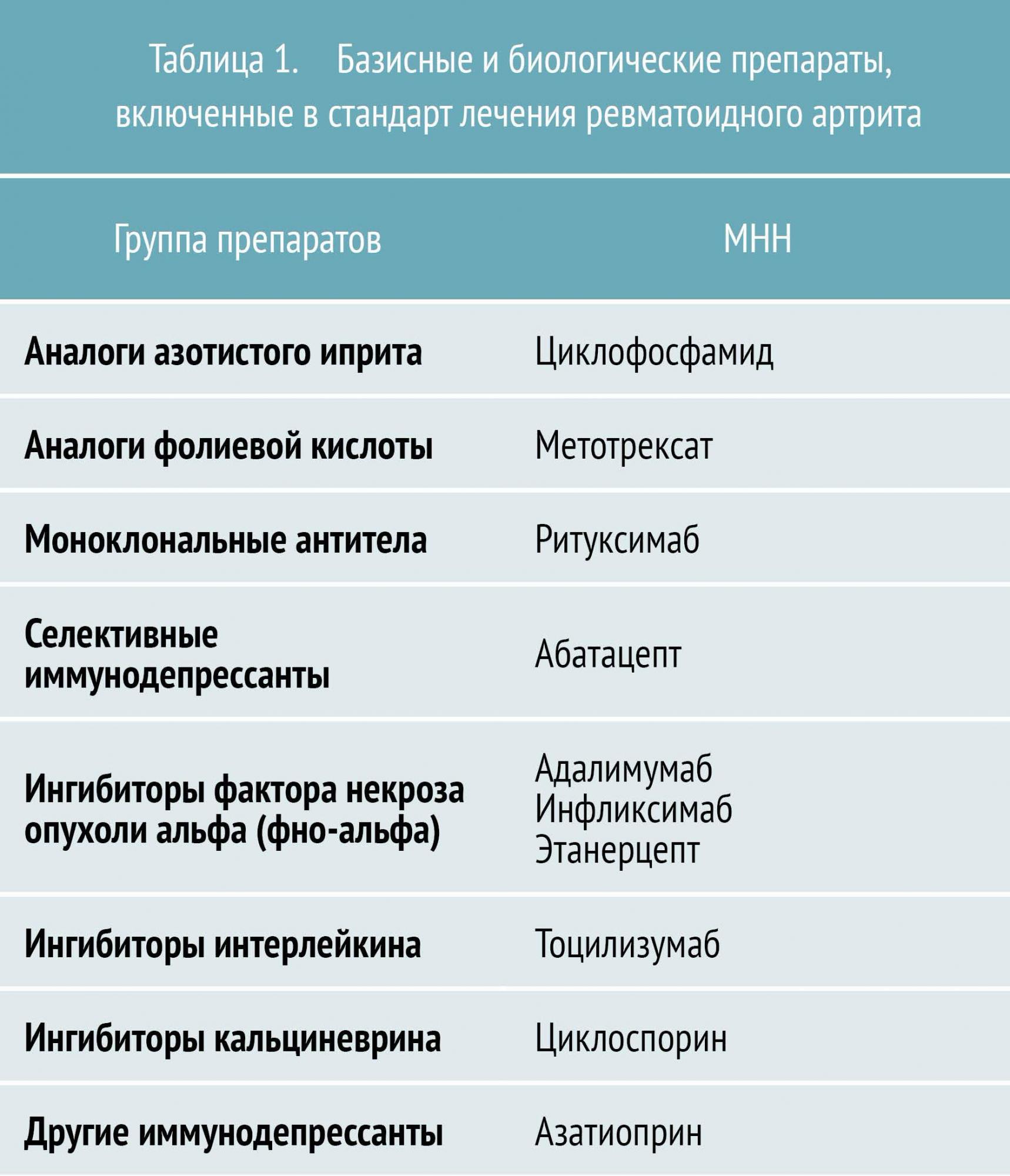
Таблица 1 — Лечение ревматоидного артрита: препараты
Лечение ревматоидного артрита лекарствами
Лечение РА направлено на подавление симптомов артрита и внесуставных проявлений, предотвращение костной деструкции и деформации суставов, сохранение качества жизни пациентов и достижение ремиссии заболевания.
Основу лечения ревматоидного артрита составляет медикаментозная иммуносупрессия. К группе иммуносупрессоров, применяемых для лечения, относятся базисные противовоспалительные препараты (БПВП), биологические препараты (см. таблицу 1) и глюкокортикостероиды (ГК).
Базисные противовоспалительные препараты (БПВП) в настоящее время являются основой лечения и назначаются после установления диагноза РА. БПВП подавляют активность и пролиферацию иммунокомпетентных клеток, замедляют прогрессирование эрозивного процесса в суставах, подавляют активность процесса (т. е. обладают иммуносупрессивным действием), а также пролиферацию синовиоцитов и фибробластов, что сопровождается выраженным снижением клинико-лабораторной активности РА и вызывает стойкую клиническую ремиссию.
БПВП различают по механизму действия и особенностям применения. Условно их разделяют на препараты первого и второго ряда. К БПВП первого ряда относятся метотрексат, лефлуномид и сульфасалазин. Препараты второго ряда (циклофосфан, азатиоприн, циклоспорин А) обладают большей токсичностью и менее эффективны, поэтому назначаются, как правило, при непереносимости БПВП первого ряда.
Глюкокортикостероиды при РА применяются системно и локально. Они обладают выраженным противовоспалительным действием, оказывают быстрый дозозависимый эффект, однако не влияют на основные патогенетические звенья РА и не обеспечивают полноценного контроля над течением заболевания. Как правило, их назначают вместе с БПВП. При высокой воспалительной активности, большом количестве пораженных суставов, недостаточной эффективности БПВП назначают системную терапию низкими дозами ГК (преднизолон, метилпреднизолон) на длительный период. Для лечения тяжелых системных проявлений ревматоидного артрита (выпотной серозит, гемолитическая анемия, кожный васкулит, лихорадка и др.) назначают средние и высокие дозы глюкокортикостероидов внутрь, а также пульс-терапию глюкокортикостероидами.
В качестве дополнительного метода купирования обострений РА применяют внутрисуставные и периартикулярные инъекции ГК (бетаметазон, триамцинолон, метилпреднизолон, гидрокортизон).
Биологические препараты для лечения ревматоидного артрита производятся с помощью биотехнологий и подавляют иммунное воспаление путем воздействия на определенные молекулы-мишени (фактор некроза опухолей, цитокины и др.).
Основными такими препаратами являются:
инфликсимаб, адалимумаб, этанерцепт (воздействуют на фактор некроза опухоли (ФНО-α));
ритуксимаб (воздействует на CD20 рецептор В-лимфоцитов);
абатацепт (воздействует на CD80, CD86, CD28).
Биологические препараты оказывают выраженный клинический эффект и тормозят деструкцию суставов, поэтому занимают второе по значимости место в лечении РА после БПВП.
Нестероидные противовоспалительные препараты — вспомогательные средства в терапии РА. Действие НПВП связано с подавлением активности циклоксигеназы (ЦОГ) и снижением синтеза простагландинов. НПВП оказывают выраженное противовоспалительное и обезболивающее действие, но не оказывают влияния на течение заболевания. Их применяют в качестве симптоматической терапии, как правило, в сочетании с БПВП.
Напомним, неселективные НПВП блокируют обе изоформы циклоксигеназы (ЦОГ-1 и ЦОГ-2), селективные — избирательно блокируют ЦОГ-2. Селективные НПВП (мелоксикам, нимесулид, целекоксиб и др.) реже вызывают НПВП-гастропатии и серьезные осложнения со стороны ЖКТ, но полностью не исключают возможность их развития. К наиболее часто применяемым при ревматоидном артрите НПВП относятся диклофенак, нимесулид, целекоксиб, мелоксикам, ибупрофен, лорноксикам (подробнее об этом также в статье «Боли в спине»)
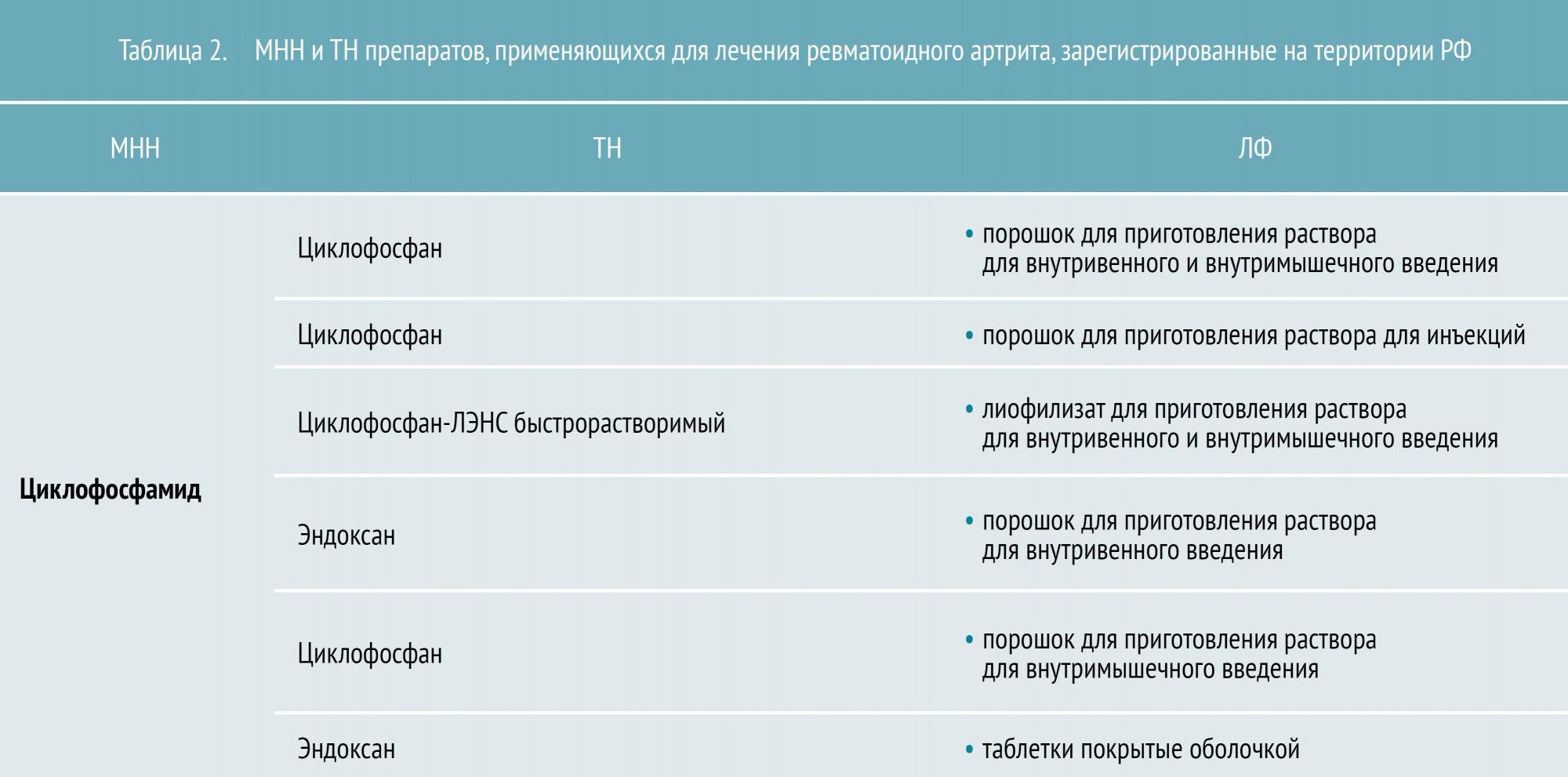
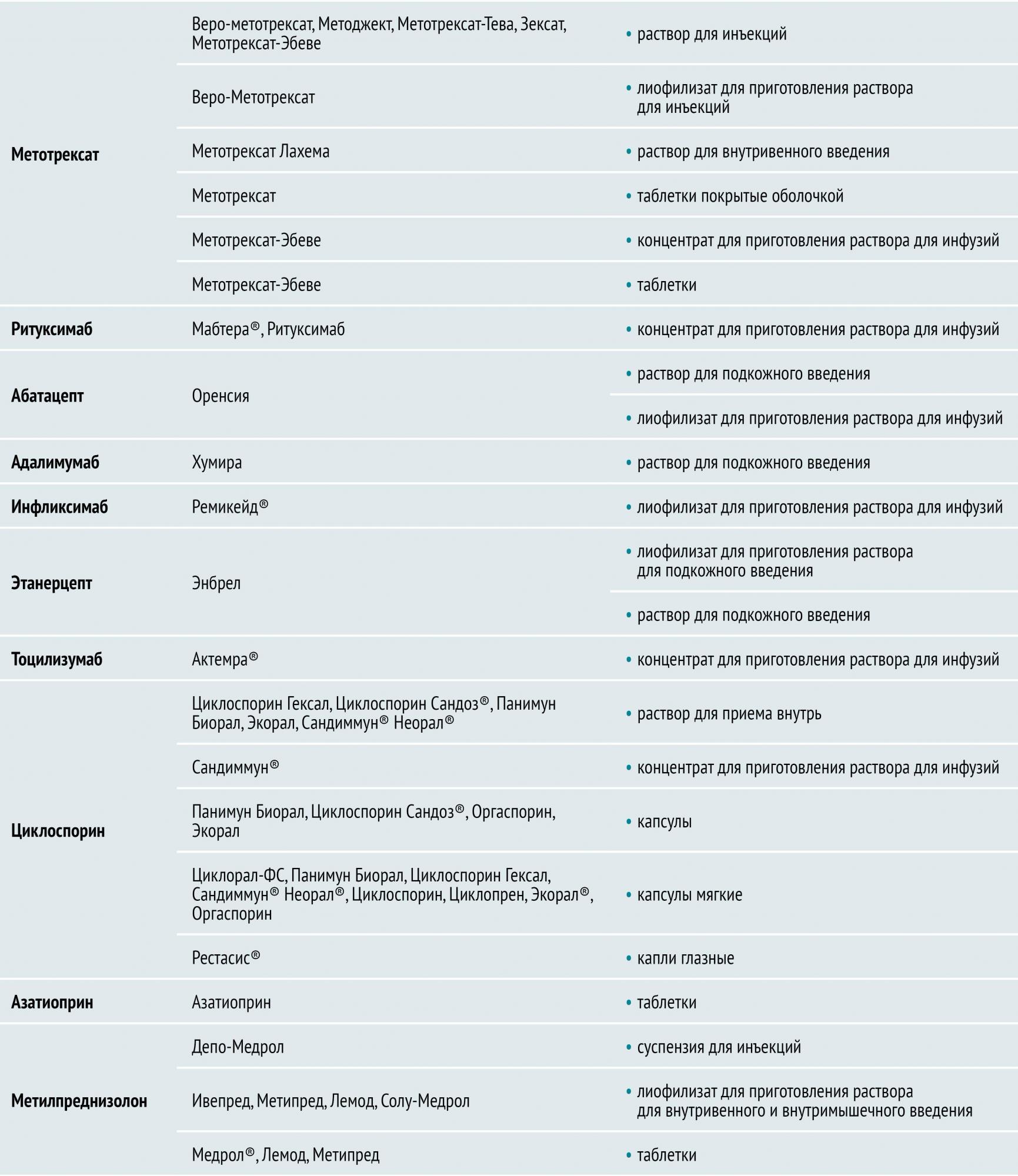
Источник
Изобретение относится к медицине, а именно к терапии больных ревматоидным артритом с вторичным остеоартрозом. Предлагаемый способ комплексного лечения включает: прием метотрексата 7-15 мг per os 1 раз в неделю, нестероидных противовоспалительных препаратов, диацереина 50 мг — 2 раза в сутки, в сочетании с воздействием низкоинтенсивным лазерным излучением, включающим накожное инфракрасное импульсное лазерное облучение коленных суставов по проекции суставной щели и надвенное облучение крови с помощью красного лазерного излучения. При осуществлении способа достигается выраженный обезболивающий, противовоспалительный эффект, снижение продолжительности утренней скованности, улучшение функциональных способностей и увеличение объема движения в пораженных суставах, а также снижение потребности в нестероидных противовоспалительных препаратах, тем самым, снижая частоту связанных с их применением побочных эффектов. 2 з.п. ф-лы, 3 табл., 2 пр.
Изобретение относится к медицине, а именно к внутренним болезням.
Ревматоидный артрит — хроническое системное воспалительное заболевание соединительной ткани с поражением преимущественно периферических суставов по типу прогрессирующего симметричного эрозивно-деструктивного полиартрита. Ревматоидный артрит поражает около 0,4-1% населения, из них от 13 до 47%, по данным разных авторов, заболевают после 50 лет, имея к этому времени в 82% случаев помимо основного заболевания несколько сопутствующих: остеоартроз, остеопороз, артериальную гипертензию, ишемическую болезнь сердца, атеросклероз и т.д.
Наряду с неуклонно прогрессирующим деструктивным поражением суставов, сопутствующие ревматоидному артриту коморбидные состояния являются одной из ведущих причин снижения качества жизни, увеличения риска инвалидизации у больных ревматоидным артритом (Michaud K., Wolfe F., 2007). Вторичный остеоартроз выступает в качестве наиболее часто встречающимся сопутствующим заболеванием при ревматоидном артрите.
В рандомизированном исследовании Jean — Pierre Valat «Изучение эффективности диацереина в симптоматическом лечении остеоартроза коленных суставов» оценивалась динамика клинических показателей: индекс WOMAC, боль по ВАШ при движении, потребность в парацетамоле, глобальная оценка пациента, переносимость и ответ пациентов согласно OMERACT-OARSI критерию. В данном исследовании оценка клинической эффективности не подтверждалась современными лабораторными показателями, которые отражают основные патогенетические процессы, происходящие при данных коморбидных состояниях. Критерием исключения больных из исследования было наличие заболеваний костно-мышечной системы. Таким образом, больные ревматоидным артритом в сочетании с вторичным остеоартрозом, что наиболее часто встречается в практике врача-ревматолога, не вошли в представленное исследование (ClinicalTrials. gov Identifier: NCT00445276).
В клиническом исследовании Pelletier JP и соавт.«Эффективность и безопасность диацереина в лечении остеоартроза коленных суставов: двойное слепое плацебо контролируемое исследование», вошедшее в группу исследований диацереина, оценивается динамика показателей клинической эффективности препарата, а также подбор наиболее эффективной дозы препарата. При этом не уточнялся генез остеоартроза, идиопатический или вторичный. Таким образом, действие препарата не рассматривалось с точки зрения единого эффективного средства не только для лечения остеоартроза, но и коморбидного состояния, являющегося причиной данного заболевания. Не проводился поиск оптимальной комплексной терапии, позволяющий усилить клинический эффект медикаментозной терапии и снизить потребность в нестероидных противовоспалительных препаратах (Arthritis Rheum. 2000 Oct; 43(10):2339-48. РМID: 11037895 [PubMed — indexed for MEDLINE] Efficacy and safety of diacerein in osteoarthritis of the knee: a double-blind, placebo-controlled trial. The Diacerein Study Group. Pelletier JP, Yaron M, Haraoui B, Cohen P, Nahir MA, Choquette D, Wigler I, Rosner IA, Beaulieu AD. Source Centre hospitalier de 1’Universite de Montréal, Hôpital Notre-Dame, Quebec, Canada.).
Проведено большое количество исследований, где доказано положительное клинико-патогенетическое влияние низкоинтенсивного лазерного излучения у больных ревматоидным артритом и остеоартрозом. Но в ходе исследований не анализировалась эффективность лазерной терапии при наличии коморбидного заболевания — вторичного остеоартроза у больных ревматоидным артритом, не использовались системные подходы в лечении, учитывая единые патогенетические механизмы развития заболеваний.
В диссертации Ревазовой А.А. «Эффективность лазерной терапии в комплексном лечении больных ревматоидным артритом» не учитывалось наличие сопутствующих заболеваний и не использовались современные антицитокиновые препараты (автореф. дис… канд. мед. наук: 14.00.05 / А.А.Ревазова; Север.-Осетин. мед. акад. — Владикавказ, 2002. — 22 с. Библиогр.: с.22. — Б.ц.).
Наиболее близким к заявленному является «Способ лечения умеренных и выраженных проявлений суставного синдрома при ревматоидном артрите» (№2198004). В представленном исследовании наряду с изучением нефармакологического способа лечения — фонофореза недостаточное внимание отводится коррекции и оптимизации фармакологической терапии ревматоидного артрита. Временное улучшение клинической картины заболевания маскирует настоящее состояние больного и способствует неконтролируемому прогрессированию заболевания. В настоящее время широкое распространение в лечении больных ревматоидным артритом отводится длительно действующим препаратам, позволяющим не только улучшить клиническую симптоматику больных, но и замедлить прогрессирование заболевания, т.е. обладающих болезнь-модифицирующим действием. Таким образом, в настоящем методе не рассмотрены вопросы фармакологической коррекции с использованием современных болезнь-контролирующих препаратов. Кроме того, учитывая большую распространенность вторичного остеоартроза у больных ревматоидным артритом, не рассмотрен возможный дополнительный вклад в клиническую картину суставного синдрома наличие данного коморбидного состояния, что необходимо учитывать в лечении основного заболевания.
Достигаемым техническим результатом является оптимизация лечения вторичного остеоартроза (ОА) при ревматоидном артрите (РА). Указанный результат возникает за счет:
— одновременного влияния на воспаленные коленные суставы и околосуставные структуры, вовлеченные в данный момент в патологический процесс и вместе с тем воздействовать на системные механизмы патогенеза ревматоидного артрита и остеоартроза;
— комплексная схема лечения достигает всех основных целей терапии больных РА с вторичным остеоартрозом: выраженного обезболивающего, противовоспалительного эффектов, снижения продолжительности утренней скованности, улучшения функциональных способностей и увеличения объема движений в пораженных суставах и практически не обладает побочными эффектами;
— снижения потребности в нестероидных противовоспалительных препаратах, тем самым, снижая частоту побочных эффектов.
Разрушение хряща при ревматоидном артрите приводит к симптомам, свойственным остеоартрозу — дистрофическим изменениям костей, разрастанию остеофитов и т.п. Таким образом, при ревматоидном артрите развивается вторичный остеоартроз. Вторичный остеоартроз способствует ухудшению основного заболевания, ускоряет прогрессирование ревматоидного артрита, что приводит к преждевременной потери трудоспособности больных.
Традиционно в лечении ревматоидного артрита используют базисные препараты (метотрексат — «золотой стандарт»), оказывающий иммуносупрессивное действие и симптоматические лекарственные средства быстрого действия (НПВП).
Таким образом, в лечении больных ревматоидным артритом не учитывается наиболее часто встречающееся коморбидное заболевание вторичный остеоартроз. Необходим поиск новых способов лечения больных ревматоидным артритом с вторичным артрозом, замедляющий прогрессирование деструкции хряща, характерного для остеоартроза, с одновременным воздействием на патогенетические механизмы, как основного, так и сопутствующего заболевания, усиливая положительный эффект базисного лечения.
В предложенной методике использовали совместное применение традиционной терапии ревматоидного артрита и сочетанного применения ингибитора интерлейкина-1 и НИЛИ, которое обладает как известно, противовоспалительным, регенераторным, замедляющим деструкцию хряща и обезболивающим действием, тем самым усиливая эффект принимаемых препаратов и снижая потребность в нестероидных противовоспалительных средствах. Именно данная комбинация позволяет оптимально воздействовать на основные патогенетические процессы, что проявляется положительной клинико-лабораторной динамикой у больных ревматоидным артритом с вторичным остеоартрозом.
Способ осуществляется следующим образом.
Больным проводится терапия, которая состоит из:
1) традиционной медикаментозной терапии:
— базисный препарат — метотрексат от 7 до 15 мг per os 1 раз в неделю длительно. Доза подбиралась с учетом активности основного заболевания.
— нестероидные противовоспалительные средства (НПВП),
2) ингибитора интерлейкина-1 (диацереин 50 мг -2 раза в сутки),
3) лазерной терапии с использованием низкоинтенсивного лазерного излучения.
Таким образом, все пациенты получали базисное лечение — метотрексат и НПВП, а также диацереин и НИЛИ. Диацереин зарегистрирован для лечения первичного и вторичного остеоартроза. Таким образом, воздействуя на вторичный остеоартроз, мы достигаем и положительный эффект на течение основного заболевания — ревматоидный артрит.
Препарат диацереин относится к группе ингибиторов интерлейкина-1. Обладает ингибирующим действием на выработку и активность интерлейкина-1. Основное патогенетическое действие диацереина и его активного метаболита реина при остеоартрозе заключается в ингибировании синтеза ИЛ-1, подавлении экспрессии рецепторов к ИЛ-1 на поверхности хондроцитов, что способствует снижению чувствительности клеток к действию этого цитокина.
Внутриклеточно метаболит блокирует активацию и транслокацию NFkB в ядро, снижая этим экспрессию NFkB-зависимых генов, включая ответственных за продукцию противовоспалительных цитокинов: ФНО-α, ИЛ-1, ИЛ-6, оксида азота и МП, способствующих усиленному разрушению компонентов хрящевого матрикса.
Методика лазерной терапия включает накожное лазерное облучение коленных суставов по проекции суставной щели и надвенное лазерное облучение крови с воздействием через кожный покров и стенку венулы сосудистого пучка в области локтевой ямки. Для накожного облучения используют инфракрасное импульсное лазерное излучение с длиной волны 0,89 мкм. Частота импульсов 80-1500 Гц, импульсная мощность 5 Вт, длительность экспозиции на поле 1-2 мин, за один сеанс суммарное время излучения не превышает 10-15 мин.
Для надвенного лазерного облучения крови использовалось красное лазерное излучение мощностью 2,5 мВт, длина волны 0,63 мкм, частота 80 Гц. Продолжительность процедуры по 1 мин слева и справа.
Лазерная терапии проводилась полупроводниковым лазерным оптическим аппаратом «Мустанг 2000» с излучающими головками МЛОК1, КЛО3.
Перед первой процедурой и по окончании курса стационарного лечения у больных определяли уровни фактора некроза опухли альфа, интерлейкины — 1,6, высокочувствительный С-реактивный белок. Оценку эффективности комплексной терапии проводили до и через 10-14 дней после начала лечения, исходя из динамики клинико-лабораторных показателей.
Нами было пролечено 33 больных вторичным остеоартрозом на фоне ревматоидного артрита.
Выбранный метод комплексного лечения с использованием ингибитора интерлейкина-1 и низкоинтенсивного лазерного излучения способствовал повышению эффективности лечения больных вторичным остеоартрозом при ревматоидном артрите, оказывая положительное влияние на течение основного заболевания на фоне базисного лечения. Подобранная схема лечения позволяет снизить частоту побочных эффектов за счет снижения потребности в нестероидных противовоспалительных препаратах. Все больные были разделены на 2 группы.
В 1 группу вошли 17 человек, которые помимо традиционной терапии, включавшей метотрексат и НПВП, получали ингибитор интерлейкина-1 в комплексе с низкоинтенсивным лазерным излучением, во 2-й группе больные (n=16) получали только традиционную медикаментозную терапию.
Динамика клинико-лабораторных показателей у больных вторичным остеоартрозом при ревматоидном артрите под влиянием лечения с использованием ингибитора интерлейкина-1 и комбинации препарата с лазерной терапией (М±m) показана на таблице ниже.
| Показатели | Больные РА в сочетании с вторичным ОА n=33, получавшие | ||
| 1 группа | 2 группа | ||
| (n=17) | (n=16) | ||
| ВАШ в покое (мм) | 1-3 день | 40,6±1,82 | 39,8±1,86 |
| 10-14 день | 24,3±1,33* | 28,2±1,72 | |
| ВАШ при движении (мм) | 1-3 день | 58,7±1,82 | 60,2±1,67 |
| 10-14 день | 37,9±1,76* | 45,8±1,82* | |
| ВАШ при пальпации (мм) | 1-3 день | 59,7±2,1 | 60,2±1,4 |
| 10-14 день | 32,8±1,5* | 47,4±1,3* | |
| Общая оценка состояния здоровья пациентом ВАШ (мм) | 1-3 день | 80,2±1,67 | 78,1±1,53 |
| 10-14 день | 50,4±1,77 | 60,2±1,33 | |
| WOMAC | 1-3 день | 125,2±2,66 | 126,2±2,42 |
| 10-14 день | 75,2±1,44* | 109,4±2,32* | |
| Lequesne | 1-3 день | 12,7±0,32 | 13,1±0,41 |
| 10-14 день | 9,1±0,42* | 10,2±0,24* | |
| Число припухших суставов | 1-3 день | 5,2±0,32 | 6,1±0,42 |
| 10-14 день | 1,1±0,42* | 3,1±0,24* | |
| Число болезненных суставов | 1-3 день | 10,2±0,32 | 11,2±0,33 |
| 10-14 день | 3,2±0,45* | 6,5±0,31* | |
| СРБ | 1-3 день | 18,36±2,16 | 19,5±2,19 |
| 10-14 день | 12,24±1,95* | 13,22±1,32* | |
| DAS28 | 1-3 день | 4,7±,045 | 5,4±0,35 |
| 10-14 день | 2,6±0,54* | 2,9±0,32* | |
| СОЭ | 1-3 день | 45,22±1,86 | 40,7±1,95* |
| 10-14 день | 32,62±1,75 | 36,5±1,97* | |
| IL -1 (пг/мл) | 1-3 день | 24,6±1,6 | 23,2±1,4 |
| 10-14 день | 19,1±1,8** | 18,6±1,2** | |
| IL-6 (пг/мл) | 1-3 день | 28,6±1,5 | 26,6±1,6 |
| 10-14 день | 15,7±0,8** | 19,2±1,2** | |
| ФНО-α (пг/мл) | 1-3 день | 26,8±1,8 | 25,2±1,3 |
| 10-14 день | 17,8±1,2** | 19,22±1,4** | |
| Р | *<0,001 | **<0,05 |
1) Индекс WOMAC (Western Ontario and McMAster Universities Osteoarthritis Index), разработанный N. Bellamy и соавт. — используют для оценки эффективности терапии остеоартроза коленных суставов, представляет собой опросник для самостоятельного заполнения его больным и содержит 24 вопроса, характеризующих боль, скованность и функциональную активность за 48 ч до момента оценки с использованием ВАШ (визуальной аналоговой шкалы).
2) Индекс Lequesne (опросник) — альго-функциональный индекс, при гонартрозе характеризует не только болевой синдром, но и тяжесть состояния больного.
3) DAS28 — показатель количественной оценки активности заболевания ревматоидный артрит, рассчитывается по формуле.
Пример №1.
Больная Л., 60 лет, страдает серопозитивным РА в течение 12 лет. В течение заболевания неоднократно проводилось лечение в профильном стационаре, где применялись современные патогенетические методы лечения, включавшие введение глюкокортикостероидов парентерально, внутрисуставно в сочетании с НПВП, болезнь контролирующих препаратов (метотрексат) и традиционные физиотерапевтические процедуры.
В амбулаторных условиях постоянно принимала поддерживающие дозы НПВП и препарат — метотрексат. Несмотря на проводимую терапию, видимого улучшения состояния не отмечала.
При осмотре отмечалась припухлость, резкая болезненность при пальпации (боль по ВАШ в покое — 7 см, при движении — 6 см) и значительное ограничение движений в проксимальных межфаланговых суставах 2-4 пальцев обеих кистей, а так же лучезапястных, локтевых, коленных и голеностопных суставах. Ограничена функция и значительно болезненные при пальпации и при движении коленные суставы.
По результатам клинико-лабораторных данных установлен диагноз: Ревматоидный артрит, серопозитвный полиартрит, активность 3, стадия 3 (эрозивный), вторичный гонартроз (R ст.2), синовит правого коленного сустава, ФНII.
Больной помимо традиционной терапии метотрексат в дозе 10 мг/неделю длительно и НПВП (диклофенак 50 мг/д) проведен курс лазерной терапии в сочетании с приемом ингибитора интерлейкина-1 диацереин (артрокер 50 мг × 2раза/день) по вышеизложенной методике. Курс лечения с использованием НИЛИ составил 14 сеансов.
После окончания терапии состояние больной заметно улучшилось: уменьшились число болезненных и число припухших суставов, боли в суставах почти полностью исчезли, что позволило отменить прием НПВП.
Данные биохимических и лабораторных методов лечения характеризовались значительной положительной динамикой (показаны на таблице ниже).
| Показатель | 1-3 день | 10-14 день |
| ВАШ в покое (мм) | 70 | 20 |
| ВАШ при движении (мм) | 60 | 30 |
| ВАШ при пальпации (мм) | 70 | 40 |
| Общая оценка состояния здоровья пациентом ВАШ (мм) | 60 | 30 |
| Утренняя скованность (мин) | 120 | 40 |
| WOMAC | 124 | 70 |
| Lequesne | 12,8 | 7 |
| DAS 28 | 5,2 | 2,3 |
| СРБ (мг/л) | 20 | 8 |
| СОЭ мм/ч | 45 | 24 |
| ФНО-α (пг/мл) | 25,2 | 17,1 |
| IL-1 (пг/мл) | 23,8 | 17,1 |
| IL-6 (пг/мл) | 27,2 | 18,6 |
| Потребность в НПВП (диклофенак) | 50 мг/день | нет |
Пример №2.
Больная А. 52 лет страдала ревматоидным артритом в течение 10 лет. Последние 4 года постоянно принимала раз в неделю метотрексат в дозе 16 мг.
Клинический диагноз: ревматоидный артрит, серопозитивный, акт II, ст. VI, вторичный полиостеоартроз, 2-сторонний гонартроз (R — ст. III) ФН II ст.
На фоне базисной патогенетической терапии метотрексат 15 мг × 1 р/неделю длительно с НПВП (найз 100 мг × 1 р/день) проведен курс лазерной терапии согласно предлагаемому способу в сочетании с приемом диацереина по 50 мг/2 раза в день в течение 14 дней. Результаты лечения представлены в таблице ниже.
Динамика показателей клинического течения заболевания
| Показатель | 1-3 день | 10-14 день |
| ВАШ в покое (мм) | 60 | 30 |
| ВАШ при движении (мм) | 70 | 40 |
| ВАШ при пальпации (мм) | 70 | 50 |
| Общая оценка состояния здоровья пациентом ВАШ (мм) | 70 | 40 |
| Утренняя скованность (мин) | 180 | 80 |
| WOMAC | 135 | 86 |
| Lequesne | 18,7 | 10,2 |
| DAS 28 | 6,2 | 3,1 |
| СРБ (мг/л) | 23 | 14 |
| СОЭ мм/ч | 54 | 28 |
| ФНО-α (пг/мл) | 28,6 | 20,4 |
| IL-1 (пг/мл) | 26,9 | 18,6 |
| IL-6 (пг/мл) | 26,5 | 20,8 |
| Потребность в НПВП нимесулид | 100 мг/день | нет |
Исходя из результатов, представленных в таблице, положительная динамика течения заболевания подтверждалась не только клиническими параметрами, но и лабораторными маркерами заболевания.
1. Способ комплексного лечения вторичного остеоартроза при ревматоидном артрите, включающий прием лекарственного препарата и воздействие физическим фактором, отличающийся тем, что в качестве лекарственных препаратов принимают метотрексат 7-15 мг per os 1 раз в неделю, нестероидные противовоспалительные препараты, диацереин 50 мг — 2 раза в сутки, а в качестве физического фактора используют воздействие низкоинтенсивным лазерным излучением, включающим накожное инфракрасное импульсное лазерное облучение коленных суставов по проекции суставной щели и надвенное облучение крови с помощью красного лазерного излучения.
2. Способ комплексного лечения вторичного остеоартроза при ревматоидном артрите по п.1, отличающийся тем, что накожное облучение проводят с частотой импульсов 80-1500 Гц, импульсной мощностью 5 Вт, длительностью экспозиции на поле 1-2 мин, суммарным временем излучения за один сеанс не более 10-15 мин.
3. Способ комплексного лечения вторичного остеоартроза при ревматоидном артрите по п.1, отличающийся тем, что надвенное облучение крови проводят с экспозицией 1 минута, с мощностью 2,5 мВт, частотой 80 Гц.
Источник